+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 7m5v | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
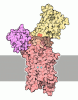
| タイトル | human ATP13A2 in the AMPPNP-bound occluded state | |||||||||
 要素 要素 | Polyamine-transporting ATPase 13A2 | |||||||||
 キーワード キーワード | TRANSPORT PROTEIN / ion transport occluded state / MEMBRANE PROTEIN | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報polyamine transmembrane transporter activity / polyamine transmembrane transport / spermine transmembrane transport / : / ABC-type polyamine transporter activity / regulation of autophagosome size / extracellular exosome biogenesis / regulation of chaperone-mediated autophagy / negative regulation of lysosomal protein catabolic process / regulation of autophagy of mitochondrion ...polyamine transmembrane transporter activity / polyamine transmembrane transport / spermine transmembrane transport / : / ABC-type polyamine transporter activity / regulation of autophagosome size / extracellular exosome biogenesis / regulation of chaperone-mediated autophagy / negative regulation of lysosomal protein catabolic process / regulation of autophagy of mitochondrion / P-type ion transporter activity / regulation of lysosomal protein catabolic process / intracellular monoatomic cation homeostasis / autophagosome-lysosome fusion / autophagosome organization / protein localization to lysosome / phosphatidic acid binding / positive regulation of exosomal secretion / multivesicular body membrane / ATPase-coupled monoatomic cation transmembrane transporter activity / intracellular zinc ion homeostasis / cupric ion binding / regulation of protein localization to nucleus / regulation of mitochondrion organization / phosphatidylinositol-3,5-bisphosphate binding / トランスロカーゼ; 他の化合物の輸送を触媒; ヌクレオシド三リン酸の加水分解に伴う / lysosomal transport / regulation of intracellular protein transport / lipid homeostasis / cellular response to zinc ion / Ion transport by P-type ATPases / regulation of neuron apoptotic process / autophagosome membrane / regulation of macroautophagy / transport vesicle / cellular response to manganese ion / multivesicular body / lysosomal lumen / autophagosome / positive regulation of protein secretion / autophagy / intracellular calcium ion homeostasis / late endosome membrane / late endosome / manganese ion binding / cellular response to oxidative stress / vesicle / monoatomic ion transmembrane transport / intracellular iron ion homeostasis / neuron projection / lysosome / lysosomal membrane / neuronal cell body / positive regulation of gene expression / ATP hydrolysis activity / zinc ion binding / ATP binding / membrane 類似検索 - 分子機能 | |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 | 電子顕微鏡法 / 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.9 Å | |||||||||
 データ登録者 データ登録者 | Lee, K.P.K. | |||||||||
| 資金援助 | 1件
| |||||||||
 引用 引用 |  ジャーナル: Mol Cell / 年: 2021 ジャーナル: Mol Cell / 年: 2021タイトル: Structural mechanisms for gating and ion selectivity of the human polyamine transporter ATP13A2. 著者: Jordan Tillinghast / Sydney Drury / Darren Bowser / Alana Benn / Kenneth Pak Kin Lee /  要旨: Mutations in ATP13A2, also known as PARK9, cause a rare monogenic form of juvenile-onset Parkinson's disease named Kufor-Rakeb syndrome and other neurodegenerative diseases. ATP13A2 encodes a ...Mutations in ATP13A2, also known as PARK9, cause a rare monogenic form of juvenile-onset Parkinson's disease named Kufor-Rakeb syndrome and other neurodegenerative diseases. ATP13A2 encodes a neuroprotective P5B P-type ATPase highly enriched in the brain that mediates selective import of spermine ions from lysosomes into the cytosol via an unknown mechanism. Here we present three structures of human ATP13A2 bound to an ATP analog or to spermine in the presence of phosphomimetics determined by cryoelectron microscopy. ATP13A2 autophosphorylation opens a lysosome luminal gate to reveal a narrow lumen access channel that holds a spermine ion in its entrance. ATP13A2's architecture suggests physical principles underlying selective polyamine transport and anticipates a "pump-channel" intermediate that could function as a counter-cation conduit to facilitate lysosome acidification. Our findings establish a firm foundation to understand ATP13A2 mutations associated with disease and bring us closer to realizing ATP13A2's potential in neuroprotective therapy. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  7m5v.cif.gz 7m5v.cif.gz | 372.3 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb7m5v.ent.gz pdb7m5v.ent.gz | 300.9 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  7m5v.json.gz 7m5v.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  7m5v_validation.pdf.gz 7m5v_validation.pdf.gz | 1.2 MB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  7m5v_full_validation.pdf.gz 7m5v_full_validation.pdf.gz | 1.2 MB | 表示 | |
| XML形式データ |  7m5v_validation.xml.gz 7m5v_validation.xml.gz | 38.4 KB | 表示 | |
| CIF形式データ |  7m5v_validation.cif.gz 7m5v_validation.cif.gz | 56.1 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/m5/7m5v https://data.pdbj.org/pub/pdb/validation_reports/m5/7m5v ftp://data.pdbj.org/pub/pdb/validation_reports/m5/7m5v ftp://data.pdbj.org/pub/pdb/validation_reports/m5/7m5v | HTTPS FTP |
-関連構造データ
| 関連構造データ |  23683MC  7m5xC  7m5yC M: このデータのモデリングに利用したマップデータ C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
-タンパク質 , 1種, 1分子 A
| #1: タンパク質 | 分子量: 129819.945 Da / 分子数: 1 / 由来タイプ: 組換発現 / 由来: (組換発現)  Homo sapiens (ヒト) / 遺伝子: ATP13A2, PARK9 / 発現宿主: Homo sapiens (ヒト) / 遺伝子: ATP13A2, PARK9 / 発現宿主:  Homo sapiens (ヒト) Homo sapiens (ヒト)参照: UniProt: Q9NQ11, トランスロカーゼ; 他の化合物の輸送を触媒; ヌクレオシド三リン酸の加水分解に伴う |
|---|
-糖 , 2種, 2分子 


| #4: 糖 | ChemComp-LMT / |
|---|---|
| #8: 糖 | ChemComp-NAG / |
-非ポリマー , 8種, 28分子 











| #2: 化合物 | ChemComp-MG / | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| #3: 化合物 | ChemComp-1DO / #5: 化合物 | ChemComp-Y01 / #6: 化合物 | ChemComp-D10 / #7: 化合物 | #9: 化合物 | ChemComp-ANP / | #10: 化合物 | ChemComp-EUJ / ( | #11: 水 | ChemComp-HOH / | |
-詳細
| 研究の焦点であるリガンドがあるか | Y |
|---|---|
| Has protein modification | Y |
-実験情報
-実験
| 実験 | 手法: 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法: 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 | 名称: Transport protein in an occluded state / タイプ: COMPLEX / Entity ID: #1 / 由来: RECOMBINANT |
|---|---|
| 分子量 | 値: 0.13 MDa / 実験値: NO |
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 由来(組換発現) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 緩衝液 | pH: 7.5 |
| 試料 | 包埋: NO / シャドウイング: NO / 染色: NO / 凍結: YES |
| 急速凍結 | 凍結剤: ETHANE |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TITAN KRIOS |
| 電子銃 | 電子線源:  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2500 nm / 最小 デフォーカス(公称値): 500 nm |
| 撮影 | 電子線照射量: 76 e/Å2 フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) |
- 解析
解析
| ソフトウェア |
| ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| CTF補正 | タイプ: PHASE FLIPPING AND AMPLITUDE CORRECTION | ||||||||||||||||||||||||
| 対称性 | 点対称性: C1 (非対称) | ||||||||||||||||||||||||
| 3次元再構成 | 解像度: 2.9 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 515611 / 対称性のタイプ: POINT | ||||||||||||||||||||||||
| 精密化 | 交差検証法: NONE 立体化学のターゲット値: GeoStd + Monomer Library + CDL v1.2 | ||||||||||||||||||||||||
| 原子変位パラメータ | Biso mean: 69.06 Å2 | ||||||||||||||||||||||||
| 拘束条件 |
|
 ムービー
ムービー コントローラー
コントローラー





 PDBj
PDBj