+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 6br6 | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
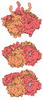
| タイトル | N2 neuraminidase in complex with a novel antiviral compound | ||||||||||||
 要素 要素 | Neuraminidase | ||||||||||||
 キーワード キーワード | HYDROLASE / Complex | ||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報exo-alpha-sialidase / exo-alpha-sialidase activity / viral budding from plasma membrane / carbohydrate metabolic process / host cell plasma membrane / virion membrane / membrane / metal ion binding 類似検索 - 分子機能 | ||||||||||||
| 生物種 |   Influenza A virus (A型インフルエンザウイルス) Influenza A virus (A型インフルエンザウイルス) | ||||||||||||
| 手法 |  X線回折 / X線回折 /  シンクロトロン / シンクロトロン /  分子置換 / 解像度: 2.03983884352 Å 分子置換 / 解像度: 2.03983884352 Å | ||||||||||||
 データ登録者 データ登録者 | Li, L.H. / Ve, T. / Pascolutti, M. / Hadhazi, A. / Bailly, B. / Thomson, R.J. / Gao, G.F. / von Itzstein, M. | ||||||||||||
| 資金援助 |  オーストラリア, 1件 オーストラリア, 1件
| ||||||||||||
 引用 引用 |  ジャーナル: ChemMedChem / 年: 2018 ジャーナル: ChemMedChem / 年: 2018タイトル: A Sulfonozanamivir Analogue Has Potent Anti-influenza Virus Activity. 著者: Hadhazi, A. / Li, L. / Bailly, B. / Maggioni, A. / Martin, G. / Dirr, L. / Dyason, J.C. / Thomson, R.J. / Gao, G.F. / Borbas, A. / Ve, T. / Pascolutti, M. / von Itzstein, M. | ||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  6br6.cif.gz 6br6.cif.gz | 193.9 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb6br6.ent.gz pdb6br6.ent.gz | 143.8 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  6br6.json.gz 6br6.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/br/6br6 https://data.pdbj.org/pub/pdb/validation_reports/br/6br6 ftp://data.pdbj.org/pub/pdb/validation_reports/br/6br6 ftp://data.pdbj.org/pub/pdb/validation_reports/br/6br6 | HTTPS FTP |
|---|
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 |
| ||||||||||||
| 2 | 
| ||||||||||||
| 単位格子 |
| ||||||||||||
| Components on special symmetry positions |
|
- 要素
要素
-タンパク質 , 1種, 1分子 A
| #1: タンパク質 | 分子量: 42793.816 Da / 分子数: 1 / 断片: residues 83-469 / 由来タイプ: 組換発現 由来: (組換発現)   Influenza A virus (A型インフルエンザウイルス) Influenza A virus (A型インフルエンザウイルス)遺伝子: NA 発現宿主:  参照: UniProt: C6KNH8, UniProt: E0UY46*PLUS, exo-alpha-sialidase |
|---|
-糖 , 3種, 3分子 
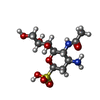

| #2: 多糖 | alpha-D-mannopyranose-(1-2)-alpha-D-mannopyranose-(1-2)-alpha-D-mannopyranose-(1-3)-beta-D- ...alpha-D-mannopyranose-(1-2)-alpha-D-mannopyranose-(1-2)-alpha-D-mannopyranose-(1-3)-beta-D-mannopyranose-(1-4)-2-acetamido-2-deoxy-beta-D-glucopyranose-(1-4)-2-acetamido-2-deoxy-beta-D-glucopyranose |
|---|---|
| #3: 糖 | ChemComp-NAG / |
| #7: 糖 | ChemComp-E3M / ( |
-非ポリマー , 4種, 180分子 






| #4: 化合物 | ChemComp-NI / |
|---|---|
| #5: 化合物 | ChemComp-CA / |
| #6: 化合物 | ChemComp-GOL / |
| #8: 水 | ChemComp-HOH / |
-詳細
| Has protein modification | Y |
|---|
-実験情報
-実験
| 実験 | 手法:  X線回折 / 使用した結晶の数: 1 X線回折 / 使用した結晶の数: 1 |
|---|
- 試料調製
試料調製
| 結晶 | マシュー密度: 2.41 Å3/Da / 溶媒含有率: 49.01 % |
|---|---|
| 結晶化 | 温度: 293 K / 手法: 蒸気拡散法 / pH: 8 / 詳細: 0.1M Tris, pH 8.0 20% PEG 400 |
-データ収集
| 回折 | 平均測定温度: 100 K |
|---|---|
| 放射光源 | 由来:  シンクロトロン / サイト: シンクロトロン / サイト:  Australian Synchrotron Australian Synchrotron  / ビームライン: MX1 / 波長: 0.979 Å / ビームライン: MX1 / 波長: 0.979 Å |
| 検出器 | タイプ: ADSC QUANTUM 210r / 検出器: CCD / 日付: 2017年6月17日 |
| 放射 | プロトコル: SINGLE WAVELENGTH / 単色(M)・ラウエ(L): M / 散乱光タイプ: x-ray |
| 放射波長 | 波長: 0.979 Å / 相対比: 1 |
| 反射 | 解像度: 2.039→48.504 Å / Num. obs: 27261 / % possible obs: 99.8 % / 冗長度: 19.1 % / Biso Wilson estimate: 24.5909164613 Å2 / Rmerge(I) obs: 0.213 / Rpim(I) all: 0.05 / Rrim(I) all: 0.218 / Net I/σ(I): 12.2 |
| 反射 シェル | 解像度: 2.04→2.1 Å / 冗長度: 18 % / Rmerge(I) obs: 1.388 / Mean I/σ(I) obs: 2.5 / Num. unique obs: 2037 / CC1/2: 0.89 / Rpim(I) all: 0.33 / Rrim(I) all: 1.428 / % possible all: 97.9 |
- 解析
解析
| ソフトウェア |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 構造決定の手法:  分子置換 / 解像度: 2.03983884352→48.5034449271 Å / SU ML: 0.190801918556 / 交差検証法: FREE R-VALUE / σ(F): 1.33486887768 / 位相誤差: 24.9412090444 分子置換 / 解像度: 2.03983884352→48.5034449271 Å / SU ML: 0.190801918556 / 交差検証法: FREE R-VALUE / σ(F): 1.33486887768 / 位相誤差: 24.9412090444
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 溶媒の処理 | 減衰半径: 0.9 Å / VDWプローブ半径: 1.11 Å | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子変位パラメータ | Biso mean: 34.1537623306 Å2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化ステップ | サイクル: LAST / 解像度: 2.03983884352→48.5034449271 Å
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 拘束条件 |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LS精密化 シェル |
|
 ムービー
ムービー コントローラー
コントローラー














 PDBj
PDBj