+ Open data
Open data
- Basic information
Basic information
| Entry | Database: PDB / ID: 5thp | ||||||
|---|---|---|---|---|---|---|---|
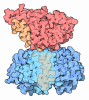
| Title | Rhodocetin in complex with the integrin alpha2-A domain | ||||||
 Components Components |
| ||||||
 Keywords Keywords | CELL ADHESION / C-type lectin / integrin / venom / coagulation | ||||||
| Function / homology |  Function and homology information Function and homology informationcollagen receptor activity / substrate-dependent cell migration / positive regulation of transmission of nerve impulse / response to parathyroid hormone / collagen binding involved in cell-matrix adhesion / integrin alpha2-beta1 complex / hypotonic response / positive regulation of cell projection organization / Regulation of MITF-M-dependent genes involved in extracellular matrix, focal adhesion and epithelial-to-mesenchymal transition / skin morphogenesis ...collagen receptor activity / substrate-dependent cell migration / positive regulation of transmission of nerve impulse / response to parathyroid hormone / collagen binding involved in cell-matrix adhesion / integrin alpha2-beta1 complex / hypotonic response / positive regulation of cell projection organization / Regulation of MITF-M-dependent genes involved in extracellular matrix, focal adhesion and epithelial-to-mesenchymal transition / skin morphogenesis / CHL1 interactions / response to L-ascorbic acid / collagen-activated signaling pathway / positive regulation of smooth muscle contraction / Laminin interactions / basal part of cell / Platelet Adhesion to exposed collagen / hepatocyte differentiation / positive regulation of phagocytosis, engulfment / focal adhesion assembly / mammary gland development / heparan sulfate proteoglycan binding / mesodermal cell differentiation / positive regulation of positive chemotaxis / positive regulation of leukocyte migration / response to amine / integrin complex / cell adhesion mediated by integrin / MET activates PTK2 signaling / positive regulation of smooth muscle cell migration / Syndecan interactions / response to muscle activity / cell-substrate adhesion / positive regulation of collagen biosynthetic process / positive regulation of epithelial cell migration / ECM proteoglycans / Integrin cell surface interactions / detection of mechanical stimulus involved in sensory perception of pain / collagen binding / laminin binding / extracellular matrix organization / positive regulation of smooth muscle cell proliferation / positive regulation of cell adhesion / axon terminus / animal organ morphogenesis / cell-matrix adhesion / integrin-mediated signaling pathway / positive regulation of translation / cellular response to estradiol stimulus / female pregnancy / cellular response to mechanical stimulus / cell-cell adhesion / integrin binding / blood coagulation / amyloid-beta binding / toxin activity / virus receptor activity / signaling receptor activity / response to hypoxia / cell adhesion / response to xenobiotic stimulus / external side of plasma membrane / focal adhesion / protein-containing complex binding / perinuclear region of cytoplasm / cell surface / extracellular region / metal ion binding / plasma membrane Similarity search - Function | ||||||
| Biological species |  Homo sapiens (human) Homo sapiens (human) Calloselasma rhodostoma (Malayan pit viper) Calloselasma rhodostoma (Malayan pit viper) | ||||||
| Method |  X-RAY DIFFRACTION / X-RAY DIFFRACTION /  SYNCHROTRON / SYNCHROTRON /  MOLECULAR REPLACEMENT / Resolution: 3.006 Å MOLECULAR REPLACEMENT / Resolution: 3.006 Å | ||||||
 Authors Authors | McDougall, M. / Orriss, G.L. / Stetefeld, J. | ||||||
| Funding support |  Canada, 1items Canada, 1items
| ||||||
 Citation Citation |  Journal: PLoS Biol. / Year: 2017 Journal: PLoS Biol. / Year: 2017Title: Dramatic and concerted conformational changes enable rhodocetin to block alpha 2 beta 1 integrin selectively. Authors: Eble, J.A. / McDougall, M. / Orriss, G.L. / Niland, S. / Johanningmeier, B. / Pohlentz, G. / Meier, M. / Karrasch, S. / Estevao-Costa, M.I. / Martins Lima, A. / Stetefeld, J. | ||||||
| History |
|
- Structure visualization
Structure visualization
| Structure viewer | Molecule:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- Downloads & links
Downloads & links
- Download
Download
| PDBx/mmCIF format |  5thp.cif.gz 5thp.cif.gz | 1.1 MB | Display |  PDBx/mmCIF format PDBx/mmCIF format |
|---|---|---|---|---|
| PDB format |  pdb5thp.ent.gz pdb5thp.ent.gz | 906.8 KB | Display |  PDB format PDB format |
| PDBx/mmJSON format |  5thp.json.gz 5thp.json.gz | Tree view |  PDBx/mmJSON format PDBx/mmJSON format | |
| Others |  Other downloads Other downloads |
-Validation report
| Arichive directory |  https://data.pdbj.org/pub/pdb/validation_reports/th/5thp https://data.pdbj.org/pub/pdb/validation_reports/th/5thp ftp://data.pdbj.org/pub/pdb/validation_reports/th/5thp ftp://data.pdbj.org/pub/pdb/validation_reports/th/5thp | HTTPS FTP |
|---|
-Related structure data
| Related structure data |  3gprS S: Starting model for refinement |
|---|---|
| Similar structure data |
- Links
Links
- Assembly
Assembly
| Deposited unit | 
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 1 | 
| ||||||||
| 2 | 
| ||||||||
| 3 | 
| ||||||||
| 4 | 
| ||||||||
| 5 | 
| ||||||||
| 6 | 
| ||||||||
| Unit cell |
|
- Components
Components
-Snaclec rhodocetin subunit ... , 2 types, 12 molecules ADGJMPBEHKNQ
| #1: Protein | Mass: 15741.510 Da / Num. of mol.: 6 / Source method: isolated from a natural source Source: (natural)  Calloselasma rhodostoma (Malayan pit viper) Calloselasma rhodostoma (Malayan pit viper)References: UniProt: D2YW39 #2: Protein | Mass: 14875.982 Da / Num. of mol.: 6 / Source method: isolated from a natural source Source: (natural)  Calloselasma rhodostoma (Malayan pit viper) Calloselasma rhodostoma (Malayan pit viper)References: UniProt: D2YW40 |
|---|
-Protein , 1 types, 6 molecules CFILOR
| #3: Protein | Mass: 23737.738 Da / Num. of mol.: 6 / Fragment: UNP residues 170-366 Source method: isolated from a genetically manipulated source Source: (gene. exp.)  Homo sapiens (human) / Gene: ITGA2, CD49B / Production host: Homo sapiens (human) / Gene: ITGA2, CD49B / Production host:  |
|---|
-Non-polymers , 6 types, 308 molecules 










| #4: Chemical | ChemComp-NA / #5: Chemical | ChemComp-CL / #6: Chemical | ChemComp-GOL / #7: Chemical | ChemComp-MG / #8: Chemical | ChemComp-SO4 / #9: Water | ChemComp-HOH / | |
|---|
-Details
| Has protein modification | Y |
|---|
-Experimental details
-Experiment
| Experiment | Method:  X-RAY DIFFRACTION / Number of used crystals: 1 X-RAY DIFFRACTION / Number of used crystals: 1 |
|---|
- Sample preparation
Sample preparation
| Crystal | Density Matthews: 3.29 Å3/Da / Density % sol: 62.67 % |
|---|---|
| Crystal grow | Temperature: 293 K / Method: vapor diffusion, hanging drop / pH: 8 / Details: 0.1M Tris pH 8.0, 2.65M Ammonium Sulfate |
-Data collection
| Diffraction | Mean temperature: 100 K |
|---|---|
| Diffraction source | Source:  SYNCHROTRON / Site: SYNCHROTRON / Site:  CLSI CLSI  / Beamline: 08ID-1 / Wavelength: 0.97949 Å / Beamline: 08ID-1 / Wavelength: 0.97949 Å |
| Detector | Type: RAYONIX MX-300 / Detector: CCD / Date: Jan 11, 2011 |
| Radiation | Protocol: SINGLE WAVELENGTH / Monochromatic (M) / Laue (L): M / Scattering type: x-ray |
| Radiation wavelength | Wavelength: 0.97949 Å / Relative weight: 1 |
| Reflection | Resolution: 3.006→19.87 Å / Num. obs: 83038 / % possible obs: 99.3 % / Redundancy: 5.3 % / Net I/σ(I): 11.9 |
- Processing
Processing
| Software |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Refinement | Method to determine structure:  MOLECULAR REPLACEMENT MOLECULAR REPLACEMENTStarting model: 3GPR Resolution: 3.006→19.867 Å / Cross valid method: FREE R-VALUE / σ(F): 1.34 / Phase error: 29.52 / Stereochemistry target values: TWIN_LSQ_F
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solvent computation | Shrinkage radii: 0.9 Å / VDW probe radii: 1.11 Å / Solvent model: FLAT BULK SOLVENT MODEL | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement step | Cycle: LAST / Resolution: 3.006→19.867 Å
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refine LS restraints |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LS refinement shell |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement TLS params. | Method: refined / Refine-ID: X-RAY DIFFRACTION
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement TLS group |
|
 Movie
Movie Controller
Controller























 PDBj
PDBj