+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 5l0a | ||||||
|---|---|---|---|---|---|---|---|
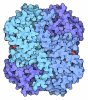
| タイトル | Human muscle fructose-1,6-bisphosphatase E69Q mutant in active R-state in complex with fructose-1,6-bisphosphate | ||||||
 要素 要素 | Fructose-1,6-bisphosphatase isozyme 2 | ||||||
 キーワード キーワード | HYDROLASE / carbohydrate metabolism / glyconeogenesis / muscle izoenzyme / FBPase / R-state / Leucine lock / E69Q / fructose-1 / 6-bisphosphate | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報fructose-bisphosphatase / fructose 1,6-bisphosphate 1-phosphatase activity / fructose 1,6-bisphosphate metabolic process / fructose 6-phosphate metabolic process / fructose metabolic process / Gluconeogenesis / anchoring junction / gluconeogenesis / Z disc / extracellular exosome ...fructose-bisphosphatase / fructose 1,6-bisphosphate 1-phosphatase activity / fructose 1,6-bisphosphate metabolic process / fructose 6-phosphate metabolic process / fructose metabolic process / Gluconeogenesis / anchoring junction / gluconeogenesis / Z disc / extracellular exosome / metal ion binding / identical protein binding / nucleus / plasma membrane / cytoplasm / cytosol 類似検索 - 分子機能 | ||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | ||||||
| 手法 |  X線回折 / X線回折 /  シンクロトロン / シンクロトロン /  分子置換 / 解像度: 2.302 Å 分子置換 / 解像度: 2.302 Å | ||||||
 データ登録者 データ登録者 | Barciszewski, J. / Wisniewski, J. / Kolodziejczyk, R. / Dzugaj, A. / Jaskolski, M. / Rakus, D. | ||||||
| 資金援助 |  ポーランド, 1件 ポーランド, 1件
| ||||||
 引用 引用 |  ジャーナル: To Be Published ジャーナル: To Be Publishedタイトル: Structural studies of human muscle FBPase 著者: Barciszewski, J. / Szpotkowski, K. / Wisniewski, J. / Kolodziejczyk, R. / Jaskolski, M. / Rakus, D. / Dzugaj, A. #1:  ジャーナル: Acta Crystallogr. D Biol. Crystallogr. / 年: 2011 ジャーナル: Acta Crystallogr. D Biol. Crystallogr. / 年: 2011タイトル: Structure of E69Q mutant of human muscle fructose-1,6-bisphosphatase. 著者: Zarzycki, M. / Kolodziejczyk, R. / Maciaszczyk-Dziubinska, E. / Wysocki, R. / Jaskolski, M. / Dzugaj, A. #2:  ジャーナル: PLoS ONE / 年: 2013 ジャーナル: PLoS ONE / 年: 2013タイトル: Crystal structures of human muscle fructose-1,6-bisphosphatase: novel quaternary states, enhanced AMP affinity, and allosteric signal transmission pathway. 著者: Shi, R. / Chen, Z.Y. / Zhu, D.W. / Li, C. / Shan, Y. / Xu, G. / Lin, S.X. #3:  ジャーナル: Acta Crystallogr D Struct Biol / 年: 2016 ジャーナル: Acta Crystallogr D Struct Biol / 年: 2016タイトル: T-to-R switch of muscle fructose-1,6-bisphosphatase involves fundamental changes of secondary and quaternary structure. 著者: Barciszewski, J. / Wisniewski, J. / Kolodziejczyk, R. / Jaskolski, M. / Rakus, D. / Dzugaj, A. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  5l0a.cif.gz 5l0a.cif.gz | 170.5 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb5l0a.ent.gz pdb5l0a.ent.gz | 138.7 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  5l0a.json.gz 5l0a.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/l0/5l0a https://data.pdbj.org/pub/pdb/validation_reports/l0/5l0a ftp://data.pdbj.org/pub/pdb/validation_reports/l0/5l0a ftp://data.pdbj.org/pub/pdb/validation_reports/l0/5l0a | HTTPS FTP |
|---|
-関連構造データ
| 関連構造データ |  5k54C  5k55C  5k56C  5et5S S: 精密化の開始モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | |
| 実験データセット #1 | データ参照:  10.18150/repod.3968588 / データの種類: diffraction image data 10.18150/repod.3968588 / データの種類: diffraction image data |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 1 | 
| ||||||||
| 単位格子 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 36665.910 Da / 分子数: 1 / 由来タイプ: 組換発現 詳細: Gaps in the sequence indicate residues that were not modeled because of poor electron density 由来: (組換発現)  Homo sapiens (ヒト) / 組織: skeletal muscle / 遺伝子: FBP2 / プラスミド: pkk223-3 / 発現宿主: Homo sapiens (ヒト) / 組織: skeletal muscle / 遺伝子: FBP2 / プラスミド: pkk223-3 / 発現宿主:  |
|---|---|
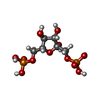
| #2: 糖 | ChemComp-FBP / |
| #3: 水 | ChemComp-HOH / |
-実験情報
-実験
| 実験 | 手法:  X線回折 / 使用した結晶の数: 1 X線回折 / 使用した結晶の数: 1 |
|---|
- 試料調製
試料調製
| 結晶 | マシュー密度: 2.09 Å3/Da / 溶媒含有率: 41.23 % |
|---|---|
| 結晶化 | 温度: 292 K / 手法: 蒸気拡散法, ハンギングドロップ法 / pH: 7.4 詳細: 10mM magnesium chloride, 2M sodium chloride, 10%PEG6000, 10mM Tris |
-データ収集
| 回折 | 平均測定温度: 100 K |
|---|---|
| 放射光源 | 由来:  シンクロトロン / サイト: シンクロトロン / サイト:  BESSY BESSY  / ビームライン: 14.3 / 波長: 0.8943 Å / ビームライン: 14.3 / 波長: 0.8943 Å |
| 検出器 | タイプ: RAYONIX SX-165mm / 検出器: CCD / 日付: 2010年6月27日 |
| 放射 | モノクロメーター: Double Crystal Monochromator, Si-111 crystal プロトコル: SINGLE WAVELENGTH / 単色(M)・ラウエ(L): M / 散乱光タイプ: x-ray |
| 放射波長 | 波長: 0.8943 Å / 相対比: 1 |
| 反射 | 解像度: 2.3→31.03 Å / Num. obs: 13949 / % possible obs: 93.9 % / 冗長度: 8.7 % / Rmerge(I) obs: 0.076 / Net I/σ(I): 3.49 |
| 反射 シェル | 解像度: 2.3→2.38 Å / 冗長度: 5.7 % / Rmerge(I) obs: 0.622 / Mean I/σ(I) obs: 2 / % possible all: 69.5 |
- 解析
解析
| ソフトウェア |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 構造決定の手法:  分子置換 分子置換開始モデル: 5ET5 解像度: 2.302→31.027 Å / SU ML: 0.31 / 交差検証法: FREE R-VALUE / σ(F): 1.33 / 位相誤差: 32.44 / 立体化学のターゲット値: ML
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 溶媒の処理 | 減衰半径: 0.9 Å / VDWプローブ半径: 1.11 Å / 溶媒モデル: FLAT BULK SOLVENT MODEL | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化ステップ | サイクル: LAST / 解像度: 2.302→31.027 Å
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 拘束条件 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LS精密化 シェル |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化 TLS | 手法: refined / Refine-ID: X-RAY DIFFRACTION
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化 TLSグループ |
|
 ムービー
ムービー コントローラー
コントローラー





















 PDBj
PDBj