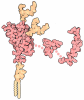
Entry Database : PDB / ID : 5ctdTitle Crystal structure of the type IX collagen NC2 hetero-trimerization domain with a guest fragment a2a1a1 of type I collagen Collagen alpha-1(I) chain,Collagen alpha-1(IX) chain Collagen alpha-1(I) chain,Collagen alpha-3(IX) chain Collagen alpha-2(I) chain,Collagen alpha-2(IX) chain Keywords / / / / / Function / homology Function Domain/homology Component
/ / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / Biological species Homo sapiens (human)Method / / / Resolution : 1.5991 Å Authors Boudko, S.P. / Bachinger, H.P. Funding support Organization Grant number Country Shriners Hospitals for Children
Journal : Sci Rep / Year : 2016Title : Structural insight for chain selection and stagger control in collagen.Authors : Boudko, S.P. / Bachinger, H.P. History Deposition Jul 23, 2015 Deposition site / Processing site Revision 1.0 Aug 3, 2016 Provider / Type Revision 1.1 Jul 12, 2017 Group / Derived calculations / Category / pdbx_struct_oper_listItem _citation.country / _citation.journal_abbrev ... _citation.country / _citation.journal_abbrev / _citation.journal_id_CSD / _citation.journal_id_ISSN / _citation.journal_volume / _citation.page_first / _citation.page_last / _citation.pdbx_database_id_DOI / _citation.pdbx_database_id_PubMed / _citation.title / _citation.year / _pdbx_struct_oper_list.symmetry_operation Revision 1.2 Nov 13, 2024 Group / Database references / Structure summaryCategory chem_comp_atom / chem_comp_bond ... chem_comp_atom / chem_comp_bond / database_2 / pdbx_entry_details / pdbx_modification_feature Item / _database_2.pdbx_database_accession
Show all Show less
 Yorodumi
Yorodumi Open data
Open data Basic information
Basic information Components
Components Keywords
Keywords Function and homology information
Function and homology information Homo sapiens (human)
Homo sapiens (human) X-RAY DIFFRACTION /
X-RAY DIFFRACTION /  SYNCHROTRON /
SYNCHROTRON /  MAD / Resolution: 1.5991 Å
MAD / Resolution: 1.5991 Å  Authors
Authors United States, 1items
United States, 1items  Citation
Citation Journal: Sci Rep / Year: 2016
Journal: Sci Rep / Year: 2016 Structure visualization
Structure visualization Molmil
Molmil Jmol/JSmol
Jmol/JSmol Downloads & links
Downloads & links Download
Download 5ctd.cif.gz
5ctd.cif.gz PDBx/mmCIF format
PDBx/mmCIF format pdb5ctd.ent.gz
pdb5ctd.ent.gz PDB format
PDB format 5ctd.json.gz
5ctd.json.gz PDBx/mmJSON format
PDBx/mmJSON format Other downloads
Other downloads https://data.pdbj.org/pub/pdb/validation_reports/ct/5ctd
https://data.pdbj.org/pub/pdb/validation_reports/ct/5ctd ftp://data.pdbj.org/pub/pdb/validation_reports/ct/5ctd
ftp://data.pdbj.org/pub/pdb/validation_reports/ct/5ctd Links
Links Assembly
Assembly
 Components
Components Homo sapiens (human) / Gene: COL1A1, COL9A1 / Plasmid: pET22b(+) / Production host:
Homo sapiens (human) / Gene: COL1A1, COL9A1 / Plasmid: pET22b(+) / Production host: 
 Homo sapiens (human) / Gene: COL1A2, COL9A2 / Plasmid: pET22b(+) / Production host:
Homo sapiens (human) / Gene: COL1A2, COL9A2 / Plasmid: pET22b(+) / Production host: 
 Homo sapiens (human) / Gene: COL1A1, COL9A3 / Plasmid: pET22b(+) / Production host:
Homo sapiens (human) / Gene: COL1A1, COL9A3 / Plasmid: pET22b(+) / Production host: 
 X-RAY DIFFRACTION / Number of used crystals: 1
X-RAY DIFFRACTION / Number of used crystals: 1  Sample preparation
Sample preparation SYNCHROTRON / Site:
SYNCHROTRON / Site:  ALS
ALS  / Beamline: 4.2.2 / Wavelength: 0.97872, 0.97918, 0.96487
/ Beamline: 4.2.2 / Wavelength: 0.97872, 0.97918, 0.96487 MAD
MAD Processing
Processing MAD / Resolution: 1.5991→41.532 Å / SU ML: 0.17 / Cross valid method: THROUGHOUT / σ(F): 0 / Phase error: 21.2 / Stereochemistry target values: MLHL
MAD / Resolution: 1.5991→41.532 Å / SU ML: 0.17 / Cross valid method: THROUGHOUT / σ(F): 0 / Phase error: 21.2 / Stereochemistry target values: MLHL Movie
Movie Controller
Controller















 PDBj
PDBj