[English] 日本語
 Yorodumi
Yorodumi- PDB-5cnl: Crystal structure of an IcmL-like type IV secretion system protei... -
+ Open data
Open data
- Basic information
Basic information
| Entry | Database: PDB / ID: 5cnl | ||||||
|---|---|---|---|---|---|---|---|
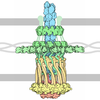
| Title | Crystal structure of an IcmL-like type IV secretion system protein (lpg0120) from Legionella pneumophila subsp. pneumophila str. Philadelphia 1 at 2.65 A resolution | ||||||
 Components Components | IcmL-like | ||||||
 Keywords Keywords | PROTEIN TRANSPORT / type IV secretion system / Structural Genomics / Joint Center for Structural Genomics / JCSG / Protein Structure Initiative / PSI-BIOLOGY | ||||||
| Function / homology | Type-IV b secretion system, inner-membrane complex component / Type-IV b secretion system, inner-membrane complex component / DI(HYDROXYETHYL)ETHER / TRIETHYLENE GLYCOL / IcmL-like Function and homology information Function and homology information | ||||||
| Biological species |  Legionella pneumophila subsp. pneumophila (bacteria) Legionella pneumophila subsp. pneumophila (bacteria) | ||||||
| Method |  X-RAY DIFFRACTION / X-RAY DIFFRACTION /  SYNCHROTRON / SYNCHROTRON /  MAD / Resolution: 2.65 Å MAD / Resolution: 2.65 Å | ||||||
 Authors Authors | Joint Center for Structural Genomics (JCSG) | ||||||
 Citation Citation |  Journal: To be published Journal: To be publishedTitle: Crystal structure of an IcmL-like type IV secretion system protein (lpg0120) from Legionella pneumophila subsp. pneumophila str. Philadelphia 1 at 2.65 A resolution Authors: Joint Center for Structural Genomics (JCSG) | ||||||
| History |
|
- Structure visualization
Structure visualization
| Structure viewer | Molecule:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- Downloads & links
Downloads & links
- Download
Download
| PDBx/mmCIF format |  5cnl.cif.gz 5cnl.cif.gz | 129.4 KB | Display |  PDBx/mmCIF format PDBx/mmCIF format |
|---|---|---|---|---|
| PDB format |  pdb5cnl.ent.gz pdb5cnl.ent.gz | 100.2 KB | Display |  PDB format PDB format |
| PDBx/mmJSON format |  5cnl.json.gz 5cnl.json.gz | Tree view |  PDBx/mmJSON format PDBx/mmJSON format | |
| Others |  Other downloads Other downloads |
-Validation report
| Arichive directory |  https://data.pdbj.org/pub/pdb/validation_reports/cn/5cnl https://data.pdbj.org/pub/pdb/validation_reports/cn/5cnl ftp://data.pdbj.org/pub/pdb/validation_reports/cn/5cnl ftp://data.pdbj.org/pub/pdb/validation_reports/cn/5cnl | HTTPS FTP |
|---|
-Related structure data
| Similar structure data | |
|---|---|
| Other databases |
- Links
Links
- Assembly
Assembly
| Deposited unit | 
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 1 | 
| ||||||||
| 2 | 
| ||||||||
| 3 | 
| ||||||||
| Unit cell |
| ||||||||
| Components on special symmetry positions |
|
- Components
Components
| #1: Protein | Mass: 17305.326 Da / Num. of mol.: 2 Source method: isolated from a genetically manipulated source Source: (gene. exp.)  Legionella pneumophila subsp. pneumophila (bacteria) Legionella pneumophila subsp. pneumophila (bacteria)Strain: Philadelphia 1 / ATCC 33152 / DSM 7513 / Gene: lpg0120 / Plasmid: SpeedET / Production host:  #2: Chemical | #3: Chemical | #4: Chemical | ChemComp-SO4 / #5: Water | ChemComp-HOH / | Has protein modification | Y | Sequence details | THE CONSTRUCT (23-176) WAS EXPRESSED WITH A PURIFICATION TAG MGSDKIHHHHHHENLYFQG. THE TAG WAS ...THE CONSTRUCT (23-176) WAS EXPRESSED WITH A PURIFICATI | |
|---|
-Experimental details
-Experiment
| Experiment | Method:  X-RAY DIFFRACTION / Number of used crystals: 1 X-RAY DIFFRACTION / Number of used crystals: 1 |
|---|
- Sample preparation
Sample preparation
| Crystal | Density Matthews: 3.22 Å3/Da / Density % sol: 61.75 % |
|---|---|
| Crystal grow | Temperature: 293 K / Method: vapor diffusion, sitting drop / pH: 7.5 Details: 0.085M HEPES pH 7.5, 15% glycerol, 1.7% polyethylene glycol 400, 1.7M ammonium sulfate |
-Data collection
| Diffraction | Mean temperature: 100 K | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Diffraction source | Source:  SYNCHROTRON / Site: SYNCHROTRON / Site:  SSRL SSRL  / Beamline: BL14-1 / Wavelength: 0.95369,0.9793,0.9791 / Beamline: BL14-1 / Wavelength: 0.95369,0.9793,0.9791 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Detector | Type: MARMOSAIC 325 mm CCD / Detector: CCD / Date: Mar 25, 2015 Details: Vertical focusing mirror; double crystal Si(111) monochromator | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radiation | Monochromator: double crystal Si(111) / Protocol: MAD / Monochromatic (M) / Laue (L): M / Scattering type: x-ray | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radiation wavelength |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Reflection | Resolution: 2.65→29.018 Å / Num. all: 13863 / Num. obs: 13863 / % possible obs: 99.2 % / Redundancy: 14.1 % / Rpim(I) all: 0.041 / Rrim(I) all: 0.155 / Rsym value: 0.149 / Net I/av σ(I): 4.786 / Net I/σ(I): 14.6 / Num. measured all: 194866 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Reflection shell |
|
-Phasing
| Phasing | Method:  MAD MAD |
|---|
- Processing
Processing
| Software |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Refinement | Method to determine structure:  MAD / Resolution: 2.65→29.018 Å / Cor.coef. Fo:Fc: 0.9464 / Cor.coef. Fo:Fc free: 0.9328 / Occupancy max: 1 / Occupancy min: 0.5 / Cross valid method: THROUGHOUT / σ(F): 0 MAD / Resolution: 2.65→29.018 Å / Cor.coef. Fo:Fc: 0.9464 / Cor.coef. Fo:Fc free: 0.9328 / Occupancy max: 1 / Occupancy min: 0.5 / Cross valid method: THROUGHOUT / σ(F): 0 Details: 1. A MET-INHIBITION PROTOCOL WAS USED FOR SELENOMETHIONINE INCORPORATION DURING PROTEIN EXPRESSION. THE OCCUPANCY OF THE SE ATOMS IN THE MSE RESIDUES WAS REDUCED TO 0.75 FOR THE REDUCED ...Details: 1. A MET-INHIBITION PROTOCOL WAS USED FOR SELENOMETHIONINE INCORPORATION DURING PROTEIN EXPRESSION. THE OCCUPANCY OF THE SE ATOMS IN THE MSE RESIDUES WAS REDUCED TO 0.75 FOR THE REDUCED SCATTERING POWER DUE TO PARTIAL S-MET INCORPORATION. 2. THE MAD PHASES WERE USED AS RESTRAINTS DURING REFINEMENT. CONDITIONS. 3. PEG AND SO4 MODELED WERE PRESENT IN CRYO CONDITION. 4. ATOM RECORDS CONTAIN SUM OF TLS AND RESIDUAL B FACTORS. ANISOU RECORDS CONTAIN SUM OF TLS AND RESIDUAL U FACTORS. 5. NCS RESTRAINTS WERE APPLIED USING BUSTER'S LSSR RESTRAINT REPRESENTATION (-AUTONCS).
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Displacement parameters | Biso max: 180.13 Å2 / Biso mean: 69.9986 Å2 / Biso min: 34.91 Å2
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refine analyze | Luzzati coordinate error obs: 0.401 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement step | Cycle: LAST / Resolution: 2.65→29.018 Å
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refine LS restraints |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LS refinement shell | Resolution: 2.65→2.86 Å / Total num. of bins used: 7
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement TLS params. | Method: refined / Refine-ID: X-RAY DIFFRACTION
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement TLS group |
|
 Movie
Movie Controller
Controller












 PDBj
PDBj