| 登録情報 | データベース: PDB / ID: 4gen
|
|---|
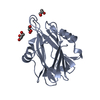
| タイトル | Crystal structure of Zucchini (monomer) |
|---|
 要素 要素 | Mitochondrial cardiolipin hydrolase |
|---|
 キーワード キーワード | HYDROLASE / piRNA / Phospholipase D / Nuclease |
|---|
| 機能・相同性 |  機能・相同性情報 機能・相同性情報
Synthesis of PA / cardiolipin hydrolase activity / oocyte karyosome formation / primary piRNA processing / dorsal appendage formation / RNA endonuclease activity producing 5'-phosphomonoesters, hydrolytic mechanism / piRNA processing / cytoplasmic side of mitochondrial outer membrane / 加水分解酵素; エステル加水分解酵素; リン酸ジエステル加水分解酵素 / P granule ...Synthesis of PA / cardiolipin hydrolase activity / oocyte karyosome formation / primary piRNA processing / dorsal appendage formation / RNA endonuclease activity producing 5'-phosphomonoesters, hydrolytic mechanism / piRNA processing / cytoplasmic side of mitochondrial outer membrane / 加水分解酵素; エステル加水分解酵素; リン酸ジエステル加水分解酵素 / P granule / regulatory ncRNA-mediated gene silencing / oogenesis / lipid catabolic process / mitochondrion / identical protein binding類似検索 - 分子機能 : / Phospholipase D-like domain / PLD-like domain / Endonuclease Chain A / Endonuclease; Chain A / 2-Layer Sandwich / Alpha Beta類似検索 - ドメイン・相同性 |
|---|
| 生物種 |   Drosophila melanogaster (キイロショウジョウバエ) Drosophila melanogaster (キイロショウジョウバエ) |
|---|
| 手法 |  X線回折 / X線回折 /  シンクロトロン / シンクロトロン /  多波長異常分散 / 解像度: 2.2 Å 多波長異常分散 / 解像度: 2.2 Å |
|---|
 データ登録者 データ登録者 | Nishimasu, H. / Fukuhara, S. / Ishitani, R. / Nureki, O. |
|---|
 引用 引用 |  ジャーナル: Nature / 年: 2012 ジャーナル: Nature / 年: 2012
タイトル: Structure and function of Zucchini endoribonuclease in piRNA biogenesis
著者: Nishimasu, H. / Ishizu, H. / Saito, K. / Fukuhara, S. / Kamatani, M.K. / Bonnefond, L. / Matsumoto, N. / Nishizawa, T. / Nakanaga, K. / Aoki, J. / Ishitani, R. / Siomi, H. / Siomi, M.C. / Nureki, O. |
|---|
| 履歴 | | 登録 | 2012年8月2日 | 登録サイト: RCSB / 処理サイト: PDBJ |
|---|
| 改定 1.0 | 2012年10月17日 | Provider: repository / タイプ: Initial release |
|---|
| 改定 1.1 | 2013年3月27日 | Group: Database references |
|---|
| 改定 1.2 | 2017年11月15日 | Group: Refinement description / カテゴリ: software
Item: _software.classification / _software.contact_author ..._software.classification / _software.contact_author / _software.contact_author_email / _software.date / _software.language / _software.location / _software.name / _software.type / _software.version |
|---|
| 改定 1.3 | 2024年11月20日 | Group: Data collection / Database references ...Data collection / Database references / Derived calculations / Structure summary
カテゴリ: chem_comp_atom / chem_comp_bond ...chem_comp_atom / chem_comp_bond / database_2 / pdbx_entry_details / pdbx_modification_feature / struct_conn / struct_ref_seq_dif / struct_site
Item: _database_2.pdbx_DOI / _database_2.pdbx_database_accession ..._database_2.pdbx_DOI / _database_2.pdbx_database_accession / _struct_conn.pdbx_leaving_atom_flag / _struct_ref_seq_dif.details / _struct_site.pdbx_auth_asym_id / _struct_site.pdbx_auth_comp_id / _struct_site.pdbx_auth_seq_id |
|---|
|
|---|
 データを開く
データを開く 基本情報
基本情報 要素
要素 キーワード
キーワード 機能・相同性情報
機能・相同性情報
 X線回折 /
X線回折 /  シンクロトロン /
シンクロトロン /  多波長異常分散 / 解像度: 2.2 Å
多波長異常分散 / 解像度: 2.2 Å  データ登録者
データ登録者 引用
引用 ジャーナル: Nature / 年: 2012
ジャーナル: Nature / 年: 2012 構造の表示
構造の表示 Molmil
Molmil Jmol/JSmol
Jmol/JSmol ダウンロードとリンク
ダウンロードとリンク ダウンロード
ダウンロード 4gen.cif.gz
4gen.cif.gz PDBx/mmCIF形式
PDBx/mmCIF形式 pdb4gen.ent.gz
pdb4gen.ent.gz PDB形式
PDB形式 4gen.json.gz
4gen.json.gz PDBx/mmJSON形式
PDBx/mmJSON形式 その他のダウンロード
その他のダウンロード 4gen_validation.pdf.gz
4gen_validation.pdf.gz wwPDB検証レポート
wwPDB検証レポート 4gen_full_validation.pdf.gz
4gen_full_validation.pdf.gz 4gen_validation.xml.gz
4gen_validation.xml.gz 4gen_validation.cif.gz
4gen_validation.cif.gz https://data.pdbj.org/pub/pdb/validation_reports/ge/4gen
https://data.pdbj.org/pub/pdb/validation_reports/ge/4gen ftp://data.pdbj.org/pub/pdb/validation_reports/ge/4gen
ftp://data.pdbj.org/pub/pdb/validation_reports/ge/4gen リンク
リンク 集合体
集合体
 要素
要素

 X線回折 / 使用した結晶の数: 1
X線回折 / 使用した結晶の数: 1  試料調製
試料調製 シンクロトロン / サイト:
シンクロトロン / サイト:  SPring-8
SPring-8  / ビームライン: BL32XU / 波長: 0.9793, 0.9800
/ ビームライン: BL32XU / 波長: 0.9793, 0.9800 解析
解析 多波長異常分散 / 解像度: 2.2→37.48 Å / Occupancy max: 1 / Occupancy min: 1 / FOM work R set: 0.8077 / SU ML: 0.63 / σ(F): 1.49 / 位相誤差: 26.58 / 立体化学のターゲット値: ML
多波長異常分散 / 解像度: 2.2→37.48 Å / Occupancy max: 1 / Occupancy min: 1 / FOM work R set: 0.8077 / SU ML: 0.63 / σ(F): 1.49 / 位相誤差: 26.58 / 立体化学のターゲット値: ML ムービー
ムービー コントローラー
コントローラー














 PDBj
PDBj


