+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 4av2 | ||||||
|---|---|---|---|---|---|---|---|
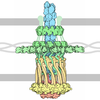
| タイトル | Single particle electron microscopy of PilQ dodecameric complexes from Neisseria meningitidis. | ||||||
 要素 要素 |
| ||||||
 キーワード キーワード | PROTEIN TRANSPORT / OUTER MEMBRANE PROTEIN / PILUS BIOGENESIS | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報 | ||||||
| 生物種 |  NEISSERIA MENINGITIDIS MC58 (髄膜炎菌) NEISSERIA MENINGITIDIS MC58 (髄膜炎菌) | ||||||
| 手法 | 電子顕微鏡法 / 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 26 Å | ||||||
 データ登録者 データ登録者 | Berry, J.L. / Phelan, M.M. / Collins, R.F. / Adomavicius, T. / Tonjum, T. / Frye, S.A. / Bird, L. / Owens, R. / Ford, R.C. / Lian, L.Y. / Derrick, J.P. | ||||||
 引用 引用 |  ジャーナル: PLoS Pathog / 年: 2012 ジャーナル: PLoS Pathog / 年: 2012タイトル: Structure and assembly of a trans-periplasmic channel for type IV pili in Neisseria meningitidis. 著者: Jamie-Lee Berry / Marie M Phelan / Richard F Collins / Tomas Adomavicius / Tone Tønjum / Stefan A Frye / Louise Bird / Ray Owens / Robert C Ford / Lu-Yun Lian / Jeremy P Derrick /  要旨: Type IV pili are polymeric fibers which protrude from the cell surface and play a critical role in adhesion and invasion by pathogenic bacteria. The secretion of pili across the periplasm and outer ...Type IV pili are polymeric fibers which protrude from the cell surface and play a critical role in adhesion and invasion by pathogenic bacteria. The secretion of pili across the periplasm and outer membrane is mediated by a specialized secretin protein, PilQ, but the way in which this large channel is formed is unknown. Using NMR, we derived the structures of the periplasmic domains from N. meningitidis PilQ: the N-terminus is shown to consist of two β-domains, which are unique to the type IV pilus-dependent secretins. The structure of the second β-domain revealed an eight-stranded β-sandwich structure which is a novel variant of the HSP20-like fold. The central part of PilQ consists of two α/β fold domains: the structure of the first of these is similar to domains from other secretins, but with an additional α-helix which links it to the second α/β domain. We also determined the structure of the entire PilQ dodecamer by cryoelectron microscopy: it forms a cage-like structure, enclosing a cavity which is approximately 55 Å in internal diameter at its largest extent. Specific regions were identified in the density map which corresponded to the individual PilQ domains: this allowed us to dock them into the cryoelectron microscopy density map, and hence reconstruct the entire PilQ assembly which spans the periplasm. We also show that the C-terminal domain from the lipoprotein PilP, which is essential for pilus assembly, binds specifically to the first α/β domain in PilQ and use NMR chemical shift mapping to generate a model for the PilP:PilQ complex. We conclude that passage of the pilus fiber requires disassembly of both the membrane-spanning and the β-domain regions in PilQ, and that PilP plays an important role in stabilising the PilQ assembly during secretion, through its anchorage in the inner membrane. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  4av2.cif.gz 4av2.cif.gz | 808.7 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb4av2.ent.gz pdb4av2.ent.gz | 610.6 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  4av2.json.gz 4av2.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  4av2_validation.pdf.gz 4av2_validation.pdf.gz | 901.9 KB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  4av2_full_validation.pdf.gz 4av2_full_validation.pdf.gz | 1.4 MB | 表示 | |
| XML形式データ |  4av2_validation.xml.gz 4av2_validation.xml.gz | 181.4 KB | 表示 | |
| CIF形式データ |  4av2_validation.cif.gz 4av2_validation.cif.gz | 241.9 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/av/4av2 https://data.pdbj.org/pub/pdb/validation_reports/av/4av2 ftp://data.pdbj.org/pub/pdb/validation_reports/av/4av2 ftp://data.pdbj.org/pub/pdb/validation_reports/av/4av2 | HTTPS FTP |
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 80129.922 Da / 分子数: 12 / 由来タイプ: 天然 / 由来: (天然)  NEISSERIA MENINGITIDIS MC58 (髄膜炎菌) / 参照: UniProt: Q70M91 NEISSERIA MENINGITIDIS MC58 (髄膜炎菌) / 参照: UniProt: Q70M91#2: タンパク質 | 分子量: 20087.498 Da / 分子数: 12 / 由来タイプ: 天然 / 由来: (天然)  NEISSERIA MENINGITIDIS MC58 (髄膜炎菌) / 参照: UniProt: Q7DD77 NEISSERIA MENINGITIDIS MC58 (髄膜炎菌) / 参照: UniProt: Q7DD77 |
|---|
-実験情報
-実験
| 実験 | 手法: 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法: 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 | 名称: OUTER MEMBRANE PROTEIN PILQ FROM NEISSERIA MENINGITIDIS タイプ: COMPLEX / 詳細: PILQ ISOLATED IN DETERGENT |
|---|---|
| 緩衝液 | 名称: 10 MM TRIS-HCL, PH 7.5, 150 MM NACL, 5 MM EDTA, AND 0.1% (W/V) ZWITTERGENT 3-10 pH: 7.5 詳細: 10 MM TRIS-HCL, PH 7.5, 150 MM NACL, 5 MM EDTA, AND 0.1% (W/V) ZWITTERGENT 3-10 |
| 試料 | 濃度: 1 mg/ml / 包埋: NO / シャドウイング: NO / 染色: NO / 凍結: YES |
| 試料支持 | 詳細: HOLEY CARBON |
| 急速凍結 | 装置: FEI VITROBOT MARK III / 凍結剤: ETHANE 詳細: VITRIFICATION 1 -- CRYOGEN- ETHANE, HUMIDITY- 90, TEMPERATURE- 100K, INSTRUMENT- FEI VITROBOT MARK III, METHOD- BOTH SIDES OF THE GRID WERE BRIEFLY BLOTTED DRY WITH WHATMAN NO. 1 FILTER PAPER ...詳細: VITRIFICATION 1 -- CRYOGEN- ETHANE, HUMIDITY- 90, TEMPERATURE- 100K, INSTRUMENT- FEI VITROBOT MARK III, METHOD- BOTH SIDES OF THE GRID WERE BRIEFLY BLOTTED DRY WITH WHATMAN NO. 1 FILTER PAPER IN A HUMIDITY-CONTROLLED CHAMBER USING A VITROBOT (FEI) DEVICE (90PERCENT RELATIVE HUMIDITY), AND THE GRID WAS THEN PLUNGED INTO LIQUID ETHANE MAINTAINED AT LESS THAN 100K |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Tecnai F20 / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TECNAI F20 / 日付: 2007年11月27日 |
| 電子銃 | 電子線源:  FIELD EMISSION GUN / 加速電圧: 200 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 200 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD / 倍率(公称値): 33000 X / 倍率(補正後): 33112 X / 最大 デフォーカス(公称値): 5100 nm / 最小 デフォーカス(公称値): 1200 nm / Cs: 2 mm |
| 試料ホルダ | 温度: 97 K |
| 撮影 | 電子線照射量: 4 e/Å2 フィルム・検出器のモデル: GATAN ULTRASCAN 4000 (4k x 4k) |
| 画像スキャン | デジタル画像の数: 55 |
- 解析
解析
| EMソフトウェア | 名称: EMAN / カテゴリ: 3次元再構成 | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| CTF補正 | 詳細: CTFFIT EACH MICROGRAPH | ||||||||||||
| 対称性 | 点対称性: C12 (12回回転対称) | ||||||||||||
| 3次元再構成 | 手法: EMAN / 解像度: 26 Å / 粒子像の数: 25303 / ピクセルサイズ(公称値): 4.53 Å / ピクセルサイズ(実測値): 4.53 Å / 倍率補正: 33113 詳細: SUBMISSION BASED ON EXPERIMENTAL DATA FROM EMDB EMD-2105. (DEPOSITION ID: 10821). 対称性のタイプ: POINT | ||||||||||||
| 原子モデル構築 | プロトコル: OTHER / 空間: RECIPROCAL / 詳細: METHOD--LOCAL CORRELATION | ||||||||||||
| 精密化 | 最高解像度: 26 Å | ||||||||||||
| 精密化ステップ | サイクル: LAST / 最高解像度: 26 Å
|
 ムービー
ムービー コントローラー
コントローラー













 PDBj
PDBj