+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 3jd4 | ||||||
|---|---|---|---|---|---|---|---|
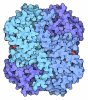
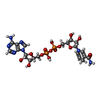
| タイトル | Glutamate dehydrogenase in complex with NADH and GTP, closed conformation | ||||||
 要素 要素 | Glutamate dehydrogenase 1, mitochondrial | ||||||
 キーワード キーワード | OXIDOREDUCTASE / glutamate metabolism / mitochondria | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報glutamate dehydrogenase [NAD(P)+] activity / tricarboxylic acid metabolic process / glutamate dehydrogenase [NAD(P)+] / glutamate dehydrogenase (NAD+) activity / glutamate dehydrogenase (NADP+) activity / L-glutamate catabolic process / glutamine metabolic process / mitochondrial inner membrane / GTP binding / endoplasmic reticulum ...glutamate dehydrogenase [NAD(P)+] activity / tricarboxylic acid metabolic process / glutamate dehydrogenase [NAD(P)+] / glutamate dehydrogenase (NAD+) activity / glutamate dehydrogenase (NADP+) activity / L-glutamate catabolic process / glutamine metabolic process / mitochondrial inner membrane / GTP binding / endoplasmic reticulum / mitochondrion / ATP binding / identical protein binding 類似検索 - 分子機能 | ||||||
| 生物種 |  | ||||||
| 手法 | 電子顕微鏡法 / 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.4 Å | ||||||
 データ登録者 データ登録者 | Borgnia, M.J. / Banerjee, S. / Merk, A. / Matthies, D. / Bartesaghi, A. / Rao, P. / Pierson, J. / Earl, L.A. / Falconieri, V. / Subramaniam, S. / Milne, J.L.S. | ||||||
 引用 引用 |  ジャーナル: Mol Pharmacol / 年: 2016 ジャーナル: Mol Pharmacol / 年: 2016タイトル: Using Cryo-EM to Map Small Ligands on Dynamic Metabolic Enzymes: Studies with Glutamate Dehydrogenase. 著者: Mario J Borgnia / Soojay Banerjee / Alan Merk / Doreen Matthies / Alberto Bartesaghi / Prashant Rao / Jason Pierson / Lesley A Earl / Veronica Falconieri / Sriram Subramaniam / Jacqueline L S Milne /  要旨: Cryo-electron microscopy (cryo-EM) methods are now being used to determine structures at near-atomic resolution and have great promise in molecular pharmacology, especially in the context of mapping ...Cryo-electron microscopy (cryo-EM) methods are now being used to determine structures at near-atomic resolution and have great promise in molecular pharmacology, especially in the context of mapping the binding of small-molecule ligands to protein complexes that display conformational flexibility. We illustrate this here using glutamate dehydrogenase (GDH), a 336-kDa metabolic enzyme that catalyzes the oxidative deamination of glutamate. Dysregulation of GDH leads to a variety of metabolic and neurologic disorders. Here, we report near-atomic resolution cryo-EM structures, at resolutions ranging from 3.2 Å to 3.6 Å for GDH complexes, including complexes for which crystal structures are not available. We show that the binding of the coenzyme NADH alone or in concert with GTP results in a binary mixture in which the enzyme is in either an "open" or "closed" state. Whereas the structure of NADH in the active site is similar between the open and closed states, it is unexpectedly different at the regulatory site. Our studies thus demonstrate that even in instances when there is considerable structural information available from X-ray crystallography, cryo-EM methods can provide useful complementary insights into regulatory mechanisms for dynamic protein complexes. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  3jd4.cif.gz 3jd4.cif.gz | 558.7 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb3jd4.ent.gz pdb3jd4.ent.gz | 464.3 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  3jd4.json.gz 3jd4.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  3jd4_validation.pdf.gz 3jd4_validation.pdf.gz | 2.2 MB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  3jd4_full_validation.pdf.gz 3jd4_full_validation.pdf.gz | 2.2 MB | 表示 | |
| XML形式データ |  3jd4_validation.xml.gz 3jd4_validation.xml.gz | 90.8 KB | 表示 | |
| CIF形式データ |  3jd4_validation.cif.gz 3jd4_validation.cif.gz | 132.2 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/jd/3jd4 https://data.pdbj.org/pub/pdb/validation_reports/jd/3jd4 ftp://data.pdbj.org/pub/pdb/validation_reports/jd/3jd4 ftp://data.pdbj.org/pub/pdb/validation_reports/jd/3jd4 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  6633MC  6630C  6631C  6632C  6634C  6635C  3jczC  3jd0C  3jd1C  3jd2C  3jd3C M: このデータのモデリングに利用したマップデータ C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 55802.258 Da / 分子数: 6 / 断片: UNP residues 58-558 / 由来タイプ: 天然 / 由来: (天然)  #2: 化合物 | ChemComp-NAI / #3: 化合物 | ChemComp-GTP / Has protein modification | N | |
|---|
-実験情報
-実験
| 実験 | 手法: 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法: 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 |
| |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 分子量 | 値: 0.347 MDa / 実験値: NO | |||||||||||||||
| 緩衝液 | 名称: 100 mM potassium phosphate, 0.1% n-octyl glucopyranoside, 20 mM NADH pH: 6.8 詳細: 100 mM potassium phosphate, 0.1% n-octyl glucopyranoside, 20 mM NADH | |||||||||||||||
| 試料 | 濃度: 2 mg/ml / 包埋: NO / シャドウイング: NO / 染色: NO / 凍結: YES | |||||||||||||||
| 試料支持 | 詳細: 200 mesh Quantifoil R2/2 grids (Quantifoil Micro Tools) | |||||||||||||||
| 急速凍結 | 装置: FEI VITROBOT MARK IV / 凍結剤: ETHANE / Temp: 90 K / 湿度: 90 % 詳細: Blot for 3-6 seconds before plunging into liquid ethane (FEI VITROBOT MARK IV). 手法: blot for 3-6 seconds before plunging |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TITAN KRIOS / 日付: 2014年7月27日 |
| 電子銃 | 電子線源:  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD / 倍率(補正後): 78426 X / 最大 デフォーカス(公称値): 5000 nm / 最小 デフォーカス(公称値): 1000 nm / Cs: 2.7 mm |
| 試料ホルダ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER |
| 撮影 | 電子線照射量: 45 e/Å2 フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) |
| 電子光学装置 | エネルギーフィルター名称: GIF Quantum / エネルギーフィルター 上限: 20 eV / エネルギーフィルター 下限: 0 eV |
| 画像スキャン | デジタル画像の数: 1588 |
- 解析
解析
| EMソフトウェア |
| ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| CTF補正 | 詳細: Each micrograph | ||||||||||||||||||||||||||||||||||||
| 対称性 | 点対称性: D3 (2回x3回 2面回転対称) | ||||||||||||||||||||||||||||||||||||
| 3次元再構成 | 解像度: 3.4 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 20429 / ピクセルサイズ(公称値): 0.63754 Å / ピクセルサイズ(実測値): 0.63754 Å / 詳細: (Single particle--Applied symmetry: D3) / 対称性のタイプ: POINT | ||||||||||||||||||||||||||||||||||||
| 原子モデル構築 | プロトコル: FLEXIBLE FIT / 空間: REAL / 詳細: REFINEMENT PROTOCOL--flexible | ||||||||||||||||||||||||||||||||||||
| 原子モデル構築 | PDB-ID: 3MW9 3mw9 PDB chain-ID: A / Accession code: 3MW9 / Source name: PDB / タイプ: experimental model | ||||||||||||||||||||||||||||||||||||
| 精密化ステップ | サイクル: LAST
| ||||||||||||||||||||||||||||||||||||
| 拘束条件 |
|
 ムービー
ムービー コントローラー
コントローラー













 PDBj
PDBj