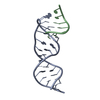
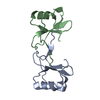
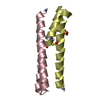
登録情報 データベース : PDB / ID : 2lgpタイトル Solution structure of LA45 from LDLR Low-density lipoprotein receptor キーワード / 機能・相同性 分子機能 ドメイン・相同性 構成要素
/ / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / 生物種 Homo sapiens (ヒト)手法 / Model details closest to the average, model 2 データ登録者 Guttman, M. / Komives, E.A. ジャーナル : Biochemistry / 年 : 2011タイトル : The Structure, Dynamics, and Binding of the LA45 Module Pair of the Low-Density Lipoprotein Receptor Suggest an Important Role for LA4 in Ligand Release.著者 : Guttman, M. / Komives, E.A. 履歴 登録 2011年8月1日 登録サイト / 処理サイト 改定 1.0 2011年11月30日 Provider / タイプ 改定 1.1 2012年1月4日 Group 改定 1.2 2023年6月14日 Group Data collection / Database references ... Data collection / Database references / Derived calculations / Other カテゴリ database_2 / pdbx_database_status ... database_2 / pdbx_database_status / pdbx_nmr_software / pdbx_nmr_spectrometer / pdbx_struct_conn_angle / struct_conn / struct_ref_seq_dif / struct_site Item _database_2.pdbx_DOI / _database_2.pdbx_database_accession ... _database_2.pdbx_DOI / _database_2.pdbx_database_accession / _pdbx_database_status.status_code_nmr_data / _pdbx_nmr_software.name / _pdbx_nmr_spectrometer.model / _pdbx_struct_conn_angle.ptnr1_auth_comp_id / _pdbx_struct_conn_angle.ptnr1_auth_seq_id / _pdbx_struct_conn_angle.ptnr1_label_atom_id / _pdbx_struct_conn_angle.ptnr1_label_comp_id / _pdbx_struct_conn_angle.ptnr1_label_seq_id / _pdbx_struct_conn_angle.ptnr3_auth_comp_id / _pdbx_struct_conn_angle.ptnr3_auth_seq_id / _pdbx_struct_conn_angle.ptnr3_label_atom_id / _pdbx_struct_conn_angle.ptnr3_label_comp_id / _pdbx_struct_conn_angle.ptnr3_label_seq_id / _pdbx_struct_conn_angle.value / _struct_conn.pdbx_dist_value / _struct_conn.ptnr1_auth_comp_id / _struct_conn.ptnr1_auth_seq_id / _struct_conn.ptnr1_label_atom_id / _struct_conn.ptnr1_label_comp_id / _struct_conn.ptnr1_label_seq_id / _struct_conn.ptnr2_auth_seq_id / _struct_conn.ptnr2_label_asym_id / _struct_ref_seq_dif.details / _struct_site.pdbx_auth_asym_id / _struct_site.pdbx_auth_comp_id / _struct_site.pdbx_auth_seq_id 改定 1.3 2024年10月30日 Group / Database references / Structure summaryカテゴリ chem_comp_atom / chem_comp_bond ... chem_comp_atom / chem_comp_bond / database_2 / pdbx_entry_details / pdbx_modification_feature Item
すべて表示 表示を減らす
 データを開く
データを開く 基本情報
基本情報 要素
要素 キーワード
キーワード 機能・相同性情報
機能・相同性情報 Homo sapiens (ヒト)
Homo sapiens (ヒト) データ登録者
データ登録者 引用
引用 ジャーナル: Biochemistry / 年: 2011
ジャーナル: Biochemistry / 年: 2011 構造の表示
構造の表示 Molmil
Molmil Jmol/JSmol
Jmol/JSmol ダウンロードとリンク
ダウンロードとリンク ダウンロード
ダウンロード 2lgp.cif.gz
2lgp.cif.gz PDBx/mmCIF形式
PDBx/mmCIF形式 pdb2lgp.ent.gz
pdb2lgp.ent.gz PDB形式
PDB形式 2lgp.json.gz
2lgp.json.gz PDBx/mmJSON形式
PDBx/mmJSON形式 その他のダウンロード
その他のダウンロード 2lgp_validation.pdf.gz
2lgp_validation.pdf.gz wwPDB検証レポート
wwPDB検証レポート 2lgp_full_validation.pdf.gz
2lgp_full_validation.pdf.gz 2lgp_validation.xml.gz
2lgp_validation.xml.gz 2lgp_validation.cif.gz
2lgp_validation.cif.gz https://data.pdbj.org/pub/pdb/validation_reports/lg/2lgp
https://data.pdbj.org/pub/pdb/validation_reports/lg/2lgp ftp://data.pdbj.org/pub/pdb/validation_reports/lg/2lgp
ftp://data.pdbj.org/pub/pdb/validation_reports/lg/2lgp リンク
リンク 集合体
集合体
 要素
要素 Homo sapiens (ヒト) / 遺伝子: LDLR / 発現宿主: CELL-FREE SYNTHESIS (未定義) / 参照: UniProt: P01130
Homo sapiens (ヒト) / 遺伝子: LDLR / 発現宿主: CELL-FREE SYNTHESIS (未定義) / 参照: UniProt: P01130 試料調製
試料調製 解析
解析 ムービー
ムービー コントローラー
コントローラー








 PDBj
PDBj













 HSQC
HSQC