+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 2ldb | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
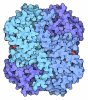
| タイトル | STRUCTURE DETERMINATION AND REFINEMENT OF BACILLUS STEAROTHERMOPHILUS LACTATE DEHYDROGENASE | |||||||||
 要素 要素 | L-LACTATE DEHYDROGENASE | |||||||||
 キーワード キーワード | OXIDOREDUCTASE(CHOH(D)-NAD(A)) | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報L-lactate dehydrogenase / L-lactate dehydrogenase (NAD+) activity / lactate metabolic process / glycolytic process / NAD binding / cytoplasm 類似検索 - 分子機能 | |||||||||
| 生物種 |   Geobacillus stearothermophilus (バクテリア) Geobacillus stearothermophilus (バクテリア) | |||||||||
| 手法 |  X線回折 / 解像度: 3 Å X線回折 / 解像度: 3 Å | |||||||||
 データ登録者 データ登録者 | Piontek, K. / Rossmann, M.G. | |||||||||
 引用 引用 |  ジャーナル: Proteins / 年: 1990 ジャーナル: Proteins / 年: 1990タイトル: Structure determination and refinement of Bacillus stearothermophilus lactate dehydrogenase. 著者: Piontek, K. / Chakrabarti, P. / Schar, H.P. / Rossmann, M.G. / Zuber, H. #1:  ジャーナル: Hoppe-Seyler's Z.Physiol.Chem. / 年: 1987 ジャーナル: Hoppe-Seyler's Z.Physiol.Chem. / 年: 1987タイトル: Nucleotide Sequences of Lactate Dehydrogenase Genes from the Thermophilic Bacteria Bacillus Stearothermophilus, B. Caldolyticus and B. Caldotenax 著者: Zuelli, F. / Weber, H. / Zuber, H. #2:  ジャーナル: J.Mol.Biol. / 年: 1982 ジャーナル: J.Mol.Biol. / 年: 1982タイトル: Crystallization of Lactate Dehydrogenase from Bacillus Stearothermophilus 著者: Schaer, H.-P. / Zuber, H. / Rossmann, M.G. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  2ldb.cif.gz 2ldb.cif.gz | 249.3 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb2ldb.ent.gz pdb2ldb.ent.gz | 196.9 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  2ldb.json.gz 2ldb.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/ld/2ldb https://data.pdbj.org/pub/pdb/validation_reports/ld/2ldb ftp://data.pdbj.org/pub/pdb/validation_reports/ld/2ldb ftp://data.pdbj.org/pub/pdb/validation_reports/ld/2ldb | HTTPS FTP |
|---|
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 |
| ||||||||||||||||
| 単位格子 |
| ||||||||||||||||
| Atom site foot note | 1: RESIDUE PRO 139 IS A CIS PROLINE. | ||||||||||||||||
| 非結晶学的対称性 (NCS) | NCS oper:
| ||||||||||||||||
| 詳細 | NON-CRYSTALLOGRAPHIC SYMMETRY TRANSFORMATIONS CORRESPONDING TO THE THREE ORTHOGONAL MOLECULAR TWO-FOLD SYMMETRY AXES ARE PRESENTED ON THE *MTRIX* RECORDS BELOW. |
- 要素
要素
| #1: タンパク質 | 分子量: 34902.723 Da / 分子数: 4 / 由来タイプ: 組換発現 由来: (組換発現)   Geobacillus stearothermophilus (バクテリア) Geobacillus stearothermophilus (バクテリア)参照: UniProt: P00344, L-lactate dehydrogenase #2: 化合物 | ChemComp-SO4 / #3: 化合物 | ChemComp-NAD / #4: 糖 | #5: 水 | ChemComp-HOH / | Has protein modification | N | 配列の詳細 | THE RESIDUES IN THIS ENTRY ARE NUMBERED SEQUENTIALLY FROM 15 - 331. SEE C. ABAD-ZAPATERO, J. P. ...THE RESIDUES IN THIS ENTRY ARE NUMBERED SEQUENTIAL | |
|---|
-実験情報
-実験
| 実験 | 手法:  X線回折 X線回折 |
|---|
- 試料調製
試料調製
| 結晶 | マシュー密度: 2.78 Å3/Da / 溶媒含有率: 55.71 % | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
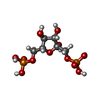
| 結晶化 | 詳細: THE ENZYME WAS COCRYSTALLIZED IN THE PRESENCE OF THE COENZYME NAD AND THE ACTIVATOR FBP. THE NAD MOLECULE IS SITUATED AT THE LDH COENZYME BINDING SITE. ONE FBP MOLECULE BINDS ACROSS THE P- ...詳細: THE ENZYME WAS COCRYSTALLIZED IN THE PRESENCE OF THE COENZYME NAD AND THE ACTIVATOR FBP. THE NAD MOLECULE IS SITUATED AT THE LDH COENZYME BINDING SITE. ONE FBP MOLECULE BINDS ACROSS THE P-AXIS. THE P-AXIS INTERSECTS THE ACTIVATOR MOLECULE GIVING RISE TO A STATISTICAL DISORDER (OCCUPANCY 0.5) AS FBP HAS ONLY PSEUDO-TWO-FOLD SYMMETRY. ONE SULFATE (SO4 3) BINDS AT THE SUBSTRATE BINDING SITE. ANOTHER SULFATE (SO4 4) IS CLOSE TO THE R-AXIS INTERFACE. | |||||||||||||||||||||||||
| 結晶化 | *PLUS pH: 7.8 / 手法: 蒸気拡散法詳細: taken from Schar, H-P. et al (1982). J. Mol. Biol., 154, 349-353. | |||||||||||||||||||||||||
| 溶液の組成 | *PLUS
|
-データ収集
| 反射 | *PLUS 最高解像度: 3 Å / 最低解像度: 50 Å / Num. obs: 24793 / % possible obs: 79.8 % / Observed criterion σ(I): 2 / Num. measured all: 76407 / Rmerge(I) obs: 0.109 |
|---|
- 解析
解析
| ソフトウェア | 名称: PROLSQ / 分類: 精密化 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 解像度: 3→6 Å / Rfactor obs: 0.26 詳細: THE ASSIGNMENT OF DONOR AND ACCEPTOR WAS ARBITRARY FOR THE FOLLOWING HYDROGEN BONDS NO7 NAD 1 O3 SO4 3 O3 SO4 3 OD1 ASP 46 O4 SO4 4 O LYS 74 O3 SO4 4 O ALA 45 O3 SO4 4 O GLY 43 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化ステップ | サイクル: LAST / 解像度: 3→6 Å
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 拘束条件 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ソフトウェア | *PLUS 名称: PROLSQ / 分類: refinement | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化 | *PLUS Num. reflection obs: 21007 / Rfactor obs: 0.26 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 溶媒の処理 | *PLUS | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子変位パラメータ | *PLUS |
 ムービー
ムービー コントローラー
コントローラー














 PDBj
PDBj