+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 1px2 | ||||||
|---|---|---|---|---|---|---|---|
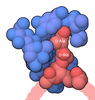
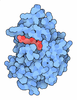
| タイトル | Crystal Structure of Rat Synapsin I C Domain Complexed to Ca.ATP (Form 1) | ||||||
 要素 要素 | Synapsin I | ||||||
 キーワード キーワード | MEMBRANE PROTEIN / ATP binding / ATP grasp / calcium (II) ion | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報synaptic vesicle cycle / synaptic vesicle clustering / Serotonin Neurotransmitter Release Cycle / Dopamine Neurotransmitter Release Cycle / extrinsic component of synaptic vesicle membrane / synaptonemal complex / neurotransmitter secretion / regulation of synaptic vesicle cycle / presynaptic active zone / regulation of synaptic vesicle exocytosis ...synaptic vesicle cycle / synaptic vesicle clustering / Serotonin Neurotransmitter Release Cycle / Dopamine Neurotransmitter Release Cycle / extrinsic component of synaptic vesicle membrane / synaptonemal complex / neurotransmitter secretion / regulation of synaptic vesicle cycle / presynaptic active zone / regulation of synaptic vesicle exocytosis / neuron development / synapse organization / Schaffer collateral - CA1 synapse / terminal bouton / calcium-dependent protein binding / synaptic vesicle / synaptic vesicle membrane / presynapse / actin binding / cell body / cytoskeleton / postsynaptic density / axon / synapse / dendrite / protein kinase binding / Golgi apparatus / ATP binding / identical protein binding 類似検索 - 分子機能 | ||||||
| 生物種 |  | ||||||
| 手法 |  X線回折 / X線回折 /  シンクロトロン / シンクロトロン /  分子置換 / 解像度: 2.23 Å 分子置換 / 解像度: 2.23 Å | ||||||
 データ登録者 データ登録者 | Brautigam, C.A. / Chelliah, Y. / Deisenhofer, J. | ||||||
 引用 引用 |  ジャーナル: J.Biol.Chem. / 年: 2004 ジャーナル: J.Biol.Chem. / 年: 2004タイトル: Tetramerization and ATP binding by a protein comprising the A, B, and C domains of rat synapsin I. 著者: Brautigam, C.A. / Chelliah, Y. / Deisenhofer, J. #1:  ジャーナル: Embo J. / 年: 1998 ジャーナル: Embo J. / 年: 1998タイトル: Synapsin I is structurally similar to ATP-utilizing enzymes 著者: Esser, L. / Wang, C.R. / Hosaka, M. / Smagula, C.S. / Sudhof, T.C. / Deisenhofer, J. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  1px2.cif.gz 1px2.cif.gz | 144.6 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb1px2.ent.gz pdb1px2.ent.gz | 110.4 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  1px2.json.gz 1px2.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  1px2_validation.pdf.gz 1px2_validation.pdf.gz | 1.6 MB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  1px2_full_validation.pdf.gz 1px2_full_validation.pdf.gz | 1.6 MB | 表示 | |
| XML形式データ |  1px2_validation.xml.gz 1px2_validation.xml.gz | 27 KB | 表示 | |
| CIF形式データ |  1px2_validation.cif.gz 1px2_validation.cif.gz | 38.3 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/px/1px2 https://data.pdbj.org/pub/pdb/validation_reports/px/1px2 ftp://data.pdbj.org/pub/pdb/validation_reports/px/1px2 ftp://data.pdbj.org/pub/pdb/validation_reports/px/1px2 | HTTPS FTP |
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 1 | 
| ||||||||
| 単位格子 |
| ||||||||
| 詳細 | The second half of the (presumably) biological tetramer is generated by the twofold axis: -y + 1, -x + 1, -z + 1/6 |
- 要素
要素
| #1: タンパク質 | 分子量: 45539.398 Da / 分子数: 2 / 断片: A, B, & C domains / 由来タイプ: 組換発現 / 由来: (組換発現)   #2: 化合物 | #3: 化合物 | #4: 水 | ChemComp-HOH / | |
|---|
-実験情報
-実験
| 実験 | 手法:  X線回折 / 使用した結晶の数: 1 X線回折 / 使用した結晶の数: 1 |
|---|
- 試料調製
試料調製
| 結晶 | マシュー密度: 2.23 Å3/Da / 溶媒含有率: 44.89 % | ||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 結晶化 | 温度: 299 K / 手法: 蒸気拡散法, ハンギングドロップ法 / pH: 7.5 詳細: PEGMME 5K, Tris, NaCl, Ca.ATP, EDTA, pH 7.5, VAPOR DIFFUSION, HANGING DROP, temperature 299K | ||||||||||||||||||||||||||||||||||||||||||
| 結晶化 | *PLUS 手法: 蒸気拡散法, ハンギングドロップ法 | ||||||||||||||||||||||||||||||||||||||||||
| 溶液の組成 | *PLUS
|
-データ収集
| 回折 | 平均測定温度: 93 K |
|---|---|
| 放射光源 | 由来:  シンクロトロン / サイト: シンクロトロン / サイト:  CHESS CHESS  / ビームライン: F1 / 波長: 0.942 Å / ビームライン: F1 / 波長: 0.942 Å |
| 検出器 | タイプ: ADSC QUANTUM 4 / 検出器: CCD / 日付: 2000年7月2日 |
| 放射 | モノクロメーター: Horizontally bent Si(111), with monochromatic mirrors of Rh-coated Si プロトコル: SINGLE WAVELENGTH / 単色(M)・ラウエ(L): M / 散乱光タイプ: x-ray |
| 放射波長 | 波長: 0.942 Å / 相対比: 1 |
| 反射 | 解像度: 2.23→40 Å / Num. all: 41721 / Num. obs: 41721 / % possible obs: 99.8 % / 冗長度: 11.2 % / Biso Wilson estimate: 28.5 Å2 / Rsym value: 0.082 / Net I/σ(I): 29.9 |
| 反射 シェル | 解像度: 2.23→2.31 Å / 冗長度: 9 % / Mean I/σ(I) obs: 6.1 / Num. unique all: 4060 / Rsym value: 0.391 / % possible all: 100 |
| 反射 | *PLUS 最低解像度: 20 Å / Num. obs: 40542 / Num. measured all: 467389 / Rmerge(I) obs: 0.082 |
| 反射 シェル | *PLUS % possible obs: 100 % / Rmerge(I) obs: 0.391 |
- 解析
解析
| ソフトウェア |
| |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 構造決定の手法:  分子置換 分子置換開始モデル: PDB entry 1AUX, Ca and ATP-gamma-S removed 解像度: 2.23→20 Å / Rfactor Rfree error: 0.005 / Isotropic thermal model: Restrained / 交差検証法: THROUGHOUT / σ(F): 0 / 立体化学のターゲット値: modified Engh & Huber 詳細: Although the A, B, and C domains of rat synapsin I were included in crystallization, only the C domain was observed. Some residues have side chains that are set to occupancies of 0.00 due to disorder.
| |||||||||||||||||||||||||
| 溶媒の処理 | 溶媒モデル: flat model / Bsol: 40.9992 Å2 / ksol: 0.326988 e/Å3 | |||||||||||||||||||||||||
| 原子変位パラメータ | Biso mean: 39.2 Å2
| |||||||||||||||||||||||||
| Refine analyze |
| |||||||||||||||||||||||||
| 精密化ステップ | サイクル: LAST / 解像度: 2.23→20 Å
| |||||||||||||||||||||||||
| 拘束条件 |
| |||||||||||||||||||||||||
| LS精密化 シェル | 解像度: 2.23→2.37 Å / Rfactor Rfree error: 0.017
| |||||||||||||||||||||||||
| 精密化 | *PLUS % reflection Rfree: 5 % / Rfactor Rfree: 0.24 | |||||||||||||||||||||||||
| 溶媒の処理 | *PLUS | |||||||||||||||||||||||||
| 原子変位パラメータ | *PLUS | |||||||||||||||||||||||||
| 拘束条件 | *PLUS
|
 ムービー
ムービー コントローラー
コントローラー















 PDBj
PDBj