+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-9802 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Nucleosome bound to C-terminal ELYS fragment | |||||||||
 マップデータ マップデータ | The structure of the nucleosome bound to C-terminal ELYS fragment. | |||||||||
 試料 試料 |
| |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
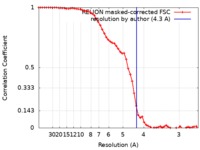
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 4.3 Å | |||||||||
 データ登録者 データ登録者 | Kobayashi W / Takizawa Y / Aihara M / Negishi L / Ishii H / Kurumizaka H | |||||||||
 引用 引用 |  ジャーナル: Commun Biol / 年: 2019 ジャーナル: Commun Biol / 年: 2019タイトル: Structural and biochemical analyses of the nuclear pore complex component ELYS identify residues responsible for nucleosome binding. 著者: Wataru Kobayashi / Yoshimasa Takizawa / Maya Aihara / Lumi Negishi / Hajime Ishii / Hitoshi Kurumizaka /  要旨: The nuclear pore complex embedded within the nuclear envelope is the essential architecture for trafficking macromolecules, such as proteins and RNAs, between the cytoplasm and nucleus. The nuclear ...The nuclear pore complex embedded within the nuclear envelope is the essential architecture for trafficking macromolecules, such as proteins and RNAs, between the cytoplasm and nucleus. The nuclear pore complex assembly occurs on chromatin in the post-mitotic phase of the cell cycle. ELYS (MEL-28/AHCTF1) binds to the nucleosome, which is the basic chromatin unit, and promotes assembly of the complex around the chromosomes in cells. Here we show that the Arg-Arg-Lys (RRK) stretch of the C-terminal ELYS region plays an essential role in the nucleosome binding. The cryo-EM structure and the crosslinking mass spectrometry reveal that the ELYS C-terminal region directly binds to the acidic patch of the nucleosome. These results provide mechanistic insight into the ELYS-nucleosome interaction, which promotes the post-mitotic nuclear pore complex formation around chromosomes in cells. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_9802.map.gz emd_9802.map.gz | 1.5 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-9802-v30.xml emd-9802-v30.xml emd-9802.xml emd-9802.xml | 10.3 KB 10.3 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_9802_fsc.xml emd_9802_fsc.xml | 5.8 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_9802.png emd_9802.png | 91.2 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-9802 http://ftp.pdbj.org/pub/emdb/structures/EMD-9802 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-9802 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-9802 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_9802_validation.pdf.gz emd_9802_validation.pdf.gz | 78.8 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_9802_full_validation.pdf.gz emd_9802_full_validation.pdf.gz | 78 KB | 表示 | |
| XML形式データ |  emd_9802_validation.xml.gz emd_9802_validation.xml.gz | 492 B | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-9802 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-9802 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-9802 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-9802 | HTTPS FTP |
-関連構造データ
| 類似構造データ |
|---|
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_9802.map.gz / 形式: CCP4 / 大きさ: 15.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_9802.map.gz / 形式: CCP4 / 大きさ: 15.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | The structure of the nucleosome bound to C-terminal ELYS fragment. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.32 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Nucleosome bound to C-terminal ELYS fragment
| 全体 | 名称: Nucleosome bound to C-terminal ELYS fragment |
|---|---|
| 要素 |
|
-超分子 #1: Nucleosome bound to C-terminal ELYS fragment
| 超分子 | 名称: Nucleosome bound to C-terminal ELYS fragment / タイプ: complex / ID: 1 / 親要素: 0 |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 組換発現 | 生物種:  組換プラスミド: pGEX6P-1-xELYS(2299-2408), pET15b-H3.1, pET15b-H4, pET15b-H2A, pET15b-H2B, pGEM-T-Easy-(Widom 601 145 base-pair) |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.5 |
|---|---|
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TALOS ARCTICA |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 QUANTUM (4k x 4k) 検出モード: COUNTING / デジタル化 - 画像ごとのフレーム数: 1-40 / 撮影したグリッド数: 1 / 実像数: 2408 / 平均露光時間: 10.0 sec. / 平均電子線量: 1.4 e/Å2 |
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 50.0 µm / 照射モード: OTHER / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm |
| 試料ステージ | ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Talos Arctica / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 精密化 | プロトコル: RIGID BODY FIT |
|---|
 ムービー
ムービー コントローラー
コントローラー
























 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)