+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-8925 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
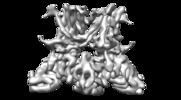
| タイトル | Cryo-EM structure of mouse TRPV3-Y564A | |||||||||
 マップデータ マップデータ | primary map | |||||||||
 試料 試料 |
| |||||||||
| 生物種 |  | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 6.5 Å | |||||||||
 データ登録者 データ登録者 | Singh AK / McGoldrick LL / Sobolevsky AI | |||||||||
 引用 引用 |  ジャーナル: Nat Struct Mol Biol / 年: 2018 ジャーナル: Nat Struct Mol Biol / 年: 2018タイトル: Structure and gating mechanism of the transient receptor potential channel TRPV3. 著者: Appu K Singh / Luke L McGoldrick / Alexander I Sobolevsky /  要旨: Transient receptor potential vanilloid subfamily member 3 (TRPV3) channel plays a crucial role in skin physiology and pathophysiology. Mutations in TRPV3 are associated with various skin diseases, ...Transient receptor potential vanilloid subfamily member 3 (TRPV3) channel plays a crucial role in skin physiology and pathophysiology. Mutations in TRPV3 are associated with various skin diseases, including Olmsted syndrome, atopic dermatitis, and rosacea. Here we present the cryo-electron microscopy structures of full-length mouse TRPV3 in the closed apo and agonist-bound open states. The agonist binds three allosteric sites distal to the pore. Channel opening is accompanied by conformational changes in both the outer pore and the intracellular gate. The gate is formed by the pore-lining S6 helices that undergo local α-to-π helical transitions, elongate, rotate, and splay apart in the open state. In the closed state, the shorter S6 segments are entirely α-helical, expose their nonpolar surfaces to the pore, and hydrophobically seal the ion permeation pathway. These findings further illuminate TRP channel activation and can aid in the design of drugs for the treatment of inflammatory skin conditions, itch, and pain. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_8925.map.gz emd_8925.map.gz | 8.3 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-8925-v30.xml emd-8925-v30.xml emd-8925.xml emd-8925.xml | 10.2 KB 10.2 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_8925.png emd_8925.png | 98.4 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-8925 http://ftp.pdbj.org/pub/emdb/structures/EMD-8925 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-8925 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-8925 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_8925_validation.pdf.gz emd_8925_validation.pdf.gz | 78.4 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_8925_full_validation.pdf.gz emd_8925_full_validation.pdf.gz | 77.6 KB | 表示 | |
| XML形式データ |  emd_8925_validation.xml.gz emd_8925_validation.xml.gz | 494 B | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-8925 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-8925 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-8925 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-8925 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_8925.map.gz / 形式: CCP4 / 大きさ: 30.5 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_8925.map.gz / 形式: CCP4 / 大きさ: 30.5 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | primary map | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.98 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : TRPV3
| 全体 | 名称: TRPV3 |
|---|---|
| 要素 |
|
-超分子 #1: TRPV3
| 超分子 | 名称: TRPV3 / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  |
| 組換発現 | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
-分子 #1: TRPV3-Y564A
| 分子 | 名称: TRPV3-Y564A / タイプ: protein_or_peptide / ID: 1 / 光学異性体: DEXTRO |
|---|---|
| 由来(天然) | 生物種:  |
| 組換発現 | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 配列 | 文字列: mgahskemap lmgkrttapg gnpvvltekr padltptkks ahffleiegf epnptvtkts ppifskpmds nirqclsgnc ddmdspqspq ddvtetpsnp nspsanlake eqrqkkkrlk krifaavseg cveelrellq dlqdlcrrrr gldvpdflmh kltasdtgkt ...文字列: mgahskemap lmgkrttapg gnpvvltekr padltptkks ahffleiegf epnptvtkts ppifskpmds nirqclsgnc ddmdspqspq ddvtetpsnp nspsanlake eqrqkkkrlk krifaavseg cveelrellq dlqdlcrrrr gldvpdflmh kltasdtgkt clmkallnin pntkeivril lafaeendil drfinaeyte eayegqtaln iaierrqgdi tavliaagad vnahakgvff npkyqhegfy fgetplalaa ctnqpeivql lmeneqtdit sqdsrgnnil halvtvaedf ktqndfvkrm ydmillrsgn weletmrnnd gltplqlaak mgkaeilkyi lsreikekpl rslsrkftdw aygpvsssly dltnvdtttd nsvleiivyn tnidnrheml tleplhtllh tkwkkfakym fflsfcfyff ynitltlvsy yrprededlp hplalthkms wlqllgrmfv liwatcisvk egiaifllrp sdlqsilsda wfhfvffvqa vlvilsvfly lfaykeylac lvlamalgwa nmlaytrgfq smgmysvmiq kvilhdvlkf lfvyilfllg fgvalaslie kcskdkkdcs sygsfsdavl elfkltiglg dlniqqnsty pilflfllit yviltfvlll nmlialmget venvskeser iwrlqrarti lefekmlpew lrsrfrmgel ckvadedfrl clrinevkwt ewkthvsfln edpgpirrta dlnkiqdssr snskttlyaf deldefpets v |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 4.0 mg/mL | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 8 構成要素:
| ||||||||||||
| グリッド | 材質: GOLD / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY | ||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277 K |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TECNAI F30 |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 平均電子線量: 67.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: SPOT SCAN / 撮影モード: BRIGHT FIELD |
| 実験機器 |  モデル: Tecnai F30 / 画像提供: FEI Company |
- 画像解析
画像解析
| 初期モデル | モデルのタイプ: EMDB MAP EMDB ID: |
|---|---|
| 最終 再構成 | 解像度のタイプ: BY AUTHOR / 解像度: 6.5 Å / 解像度の算出法: FSC 0.143 CUT-OFF / ソフトウェア - 名称: RELION / 使用した粒子像数: 44661 |
| 初期 角度割当 | タイプ: ANGULAR RECONSTITUTION |
| 最終 角度割当 | タイプ: ANGULAR RECONSTITUTION |
 ムービー
ムービー コントローラー
コントローラー
















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)





















