+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-6213 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | CryoEM reconstruction of Kaposi's sarcoma-associated herpesvirus mutant with C-terminal half of SCP truncated (KSHV-SCPN86) | |||||||||
 マップデータ マップデータ | CryoEM reconstruction of KSHV-SCPN86 mutant. The capsid structure is essentially identical to that of wild-type KSHV. | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | herpesvirus / gammaherpesvirus / the smallest capsid protein / cementing protein | |||||||||
| 生物種 |   Human herpesvirus 8 (ヘルペスウイルス) Human herpesvirus 8 (ヘルペスウイルス) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 7.4 Å | |||||||||
 データ登録者 データ登録者 | Dai XH / Gong DY / Xiao YC / Wu TT / Sun R / Zhou ZH | |||||||||
 引用 引用 |  ジャーナル: Proc Natl Acad Sci U S A / 年: 2015 ジャーナル: Proc Natl Acad Sci U S A / 年: 2015タイトル: CryoEM and mutagenesis reveal that the smallest capsid protein cements and stabilizes Kaposi's sarcoma-associated herpesvirus capsid. 著者: Xinghong Dai / Danyang Gong / Yuchen Xiao / Ting-Ting Wu / Ren Sun / Z Hong Zhou /  要旨: With just one eighth the size of the major capsid protein (MCP), the smallest capsid protein (SCP) of human tumor herpesviruses--Kaposi's sarcoma-associated herpesvirus (KSHV) and Epstein-Barr virus ...With just one eighth the size of the major capsid protein (MCP), the smallest capsid protein (SCP) of human tumor herpesviruses--Kaposi's sarcoma-associated herpesvirus (KSHV) and Epstein-Barr virus (EBV)--is vital to capsid assembly, yet its mechanism of action is unknown. Here, by cryoEM of KSHV at 6-Å resolution, we show that SCP forms a crown on each hexon and uses a kinked helix to cross-link neighboring MCP subunits. SCP-null mutation decreased viral titer by 1,000 times and impaired but did not fully abolish capsid assembly, indicating an important but nonessential role of SCP. By truncating the C-terminal half of SCP and performing cryoEM reconstruction, we demonstrate that SCP's N-terminal half is responsible for the observed structure and function whereas the C-terminal half is flexible and dispensable. Serial truncations further highlight the critical importance of the N-terminal 10 aa, and cryoEM reconstruction of the one with six residues truncated localizes the N terminus of SCP in the cryoEM density map and enables us to construct a pseudoatomic model of SCP. Fitting of this SCP model and a homology model for the MCP upper domain into the cryoEM map reveals that SCP binds MCP largely via hydrophobic interactions and the kinked helix of SCP bridges over neighboring MCPs to form noncovalent cross-links. These data support a mechanistic model that tumor herpesvirus SCP reinforces the capsid for genome packaging, thus acting as a cementing protein similar to those found in many bacteriophages. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_6213.map.gz emd_6213.map.gz | 387.1 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-6213-v30.xml emd-6213-v30.xml emd-6213.xml emd-6213.xml | 9.6 KB 9.6 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_6213.tif emd_6213.tif | 633.7 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-6213 http://ftp.pdbj.org/pub/emdb/structures/EMD-6213 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-6213 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-6213 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_6213_validation.pdf.gz emd_6213_validation.pdf.gz | 78.4 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_6213_full_validation.pdf.gz emd_6213_full_validation.pdf.gz | 77.5 KB | 表示 | |
| XML形式データ |  emd_6213_validation.xml.gz emd_6213_validation.xml.gz | 493 B | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-6213 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-6213 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-6213 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-6213 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_6213.map.gz / 形式: CCP4 / 大きさ: 1.4 GB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_6213.map.gz / 形式: CCP4 / 大きさ: 1.4 GB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | CryoEM reconstruction of KSHV-SCPN86 mutant. The capsid structure is essentially identical to that of wild-type KSHV. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 2.06 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
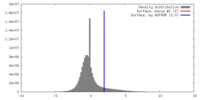
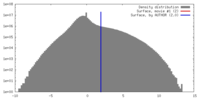
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Kaposi's sarcoma-associated herpesvirus (KSHV) mutant with the C-...
| 全体 | 名称: Kaposi's sarcoma-associated herpesvirus (KSHV) mutant with the C-terminal half of the smallest capsid protein (SCP) truncated |
|---|---|
| 要素 |
|
-超分子 #1000: Kaposi's sarcoma-associated herpesvirus (KSHV) mutant with the C-...
| 超分子 | 名称: Kaposi's sarcoma-associated herpesvirus (KSHV) mutant with the C-terminal half of the smallest capsid protein (SCP) truncated タイプ: sample / ID: 1000 / 集合状態: icosahedral virus / Number unique components: 1 |
|---|
-超分子 #1: Human herpesvirus 8
| 超分子 | 名称: Human herpesvirus 8 / タイプ: virus / ID: 1 / Name.synonym: Kaposi's sarcoma-associated herpesvirus 詳細: The smallest capsid protein (SCP) of the virus is truncated at residue number 86. NCBI-ID: 37296 / 生物種: Human herpesvirus 8 / Sci species strain: BAC16 / データベース: NCBI / ウイルスタイプ: VIRION / ウイルス・単離状態: STRAIN / ウイルス・エンベロープ: Yes / ウイルス・中空状態: No / Syn species name: Kaposi's sarcoma-associated herpesvirus |
|---|---|
| 宿主 | 生物種:  Homo sapiens (ヒト) / 別称: VERTEBRATES Homo sapiens (ヒト) / 別称: VERTEBRATES |
| ウイルス殻 | Shell ID: 1 / 名称: capsid / 直径: 1350 Å / T番号(三角分割数): 16 |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.4 / 詳細: PBS |
|---|---|
| グリッド | 詳細: Quantifoil R2/1-Cu200 |
| 凍結 | 凍結剤: ETHANE / 装置: HOMEMADE PLUNGER |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 詳細 | K2 camera super-resolution mode |
| 日付 | 2013年11月5日 |
| 撮影 | カテゴリ: CCD / フィルム・検出器のモデル: GATAN K2 (4k x 4k) / デジタル化 - サンプリング間隔: 5.0 µm / 実像数: 1184 / 平均電子線量: 25 e/Å2 / ビット/ピクセル: 16 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 倍率(補正後): 48500 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 3.0 µm / 最小 デフォーカス(公称値): 0.5 µm / 倍率(公称値): 14000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| CTF補正 | 詳細: Each Particle |
|---|---|
| 最終 再構成 | アルゴリズム: OTHER / 解像度のタイプ: BY AUTHOR / 解像度: 7.4 Å / 解像度の算出法: OTHER / ソフトウェア - 名称: IMIRS, EMAN1 / 使用した粒子像数: 1500 |
 ムービー
ムービー コントローラー
コントローラー














 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)