+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-5197 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM reconstruction of human mTORC1 | |||||||||
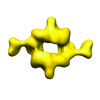
 マップデータ マップデータ | Density map of human mTORC1 resolution filtered to 26 Angstroms | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Kinase complex / metabolic role | |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 26.0 Å | |||||||||
 データ登録者 データ登録者 | Yip CK / Murata K / Walz T / Sabataini DM / Kang SA | |||||||||
 引用 引用 |  ジャーナル: Mol Cell / 年: 2010 ジャーナル: Mol Cell / 年: 2010タイトル: Structure of the human mTOR complex I and its implications for rapamycin inhibition. 著者: Calvin K Yip / Kazuyoshi Murata / Thomas Walz / David M Sabatini / Seong A Kang /  要旨: The mammalian target of rapamycin complex 1 (mTORC1) regulates cell growth in response to the nutrient and energy status of the cell, and its deregulation is common in human cancers. Little is known ...The mammalian target of rapamycin complex 1 (mTORC1) regulates cell growth in response to the nutrient and energy status of the cell, and its deregulation is common in human cancers. Little is known about the overall architecture and subunit organization of this essential signaling complex. We have determined the three-dimensional (3D) structure of the fully assembled human mTORC1 by cryo-electron microscopy (cryo-EM). Our analyses reveal that mTORC1 is an obligate dimer with an overall rhomboid shape and a central cavity. The dimeric interfaces are formed by interlocking interactions between the mTOR and raptor subunits. Extended incubation with FKBP12-rapamycin compromises the structural integrity of mTORC1 in a stepwise manner, leading us to propose a model in which rapamycin inhibits mTORC1-mediated phosphorylation of 4E-BP1 and S6K1 through different mechanisms. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_5197.map.gz emd_5197.map.gz | 4.1 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-5197-v30.xml emd-5197-v30.xml emd-5197.xml emd-5197.xml | 13.1 KB 13.1 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_5197_1.tif emd_5197_1.tif | 1.5 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-5197 http://ftp.pdbj.org/pub/emdb/structures/EMD-5197 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-5197 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-5197 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_5197_validation.pdf.gz emd_5197_validation.pdf.gz | 78.4 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_5197_full_validation.pdf.gz emd_5197_full_validation.pdf.gz | 77.5 KB | 表示 | |
| XML形式データ |  emd_5197_validation.xml.gz emd_5197_validation.xml.gz | 494 B | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-5197 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-5197 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-5197 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-5197 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_5197.map.gz / 形式: CCP4 / 大きさ: 7.8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_5197.map.gz / 形式: CCP4 / 大きさ: 7.8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Density map of human mTORC1 resolution filtered to 26 Angstroms | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 4.1 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Purified human mTORC1
| 全体 | 名称: Purified human mTORC1 |
|---|---|
| 要素 |
|
-超分子 #1000: Purified human mTORC1
| 超分子 | 名称: Purified human mTORC1 / タイプ: sample / ID: 1000 / 集合状態: dimer of heterotetramer / Number unique components: 4 |
|---|---|
| 分子量 | 理論値: 1.0 MDa |
-分子 #1: mTOR
| 分子 | 名称: mTOR / タイプ: protein_or_peptide / ID: 1 / Name.synonym: mTOR / コピー数: 2 / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) / 別称: human / 細胞: HEK-293T / 細胞中の位置: cytoplasm Homo sapiens (ヒト) / 別称: human / 細胞: HEK-293T / 細胞中の位置: cytoplasm |
| 分子量 | 理論値: 289 KDa |
| 組換発現 | 生物種: Mammalian cells |
-分子 #2: raptor
| 分子 | 名称: raptor / タイプ: protein_or_peptide / ID: 2 / Name.synonym: raptor / コピー数: 2 / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) / 別称: human / 細胞: HEK-293T / 細胞中の位置: cytoplasm Homo sapiens (ヒト) / 別称: human / 細胞: HEK-293T / 細胞中の位置: cytoplasm |
| 分子量 | 理論値: 150 KDa |
| 組換発現 | 生物種: Mammalian cells |
-分子 #3: mLST8
| 分子 | 名称: mLST8 / タイプ: protein_or_peptide / ID: 3 / Name.synonym: mLST8 / コピー数: 2 / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) / 別称: Human / 細胞: HEK-293T / 細胞中の位置: cytoplasm Homo sapiens (ヒト) / 別称: Human / 細胞: HEK-293T / 細胞中の位置: cytoplasm |
| 分子量 | 実験値: 36 KDa / 理論値: 36 KDa |
| 組換発現 | 生物種: Mammalian cells |
-分子 #4: PRAS40
| 分子 | 名称: PRAS40 / タイプ: protein_or_peptide / ID: 4 / Name.synonym: PRAS40 / コピー数: 2 / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) / 別称: Human / 細胞: HEK-293T / 細胞中の位置: cytoplasm Homo sapiens (ヒト) / 別称: Human / 細胞: HEK-293T / 細胞中の位置: cytoplasm |
| 分子量 | 実験値: 27 KDa / 理論値: 27 KDa |
| 組換発現 | 生物種: Mammalian cells |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.02 mg/mL |
|---|---|
| 緩衝液 | pH: 7.5 / 詳細: 50mM HEPES, 150mM NaCl |
| グリッド | 詳細: 400 mesh Quantifoil R1.2/1.3 |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 85 % / 装置: OTHER / 詳細: Vitrification instrument: Vitrobot / 手法: Blot for 2 seconds before plunging |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TECNAI F20 |
|---|---|
| 日付 | 2008年3月12日 |
| 撮影 | カテゴリ: FILM / フィルム・検出器のモデル: KODAK SO-163 FILM / デジタル化 - スキャナー: ZEISS SCAI / デジタル化 - サンプリング間隔: 21 µm / 実像数: 323 |
| Tilt angle min | 0 |
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 倍率(補正後): 51159 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 1.4 mm / 最大 デフォーカス(公称値): 6.0 µm / 最小 デフォーカス(公称値): 2.5 µm / 倍率(公称値): 52000 |
| 試料ステージ | 試料ホルダー: Side entry liquid nitrogen-cooled cryo specimen holder 試料ホルダーモデル: GATAN LIQUID NITROGEN / Tilt angle max: 45 |
| 実験機器 |  モデル: Tecnai F20 / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 初期モデル | PDB ID: Chain - Chain ID: A |
|---|---|
| 詳細 | PDBEntryID_givenInChain. Protocol: manual docking. model was manually docked into density map using Chimera |
| 精密化 | 空間: REAL / プロトコル: RIGID BODY FIT / 当てはまり具合の基準: rigid body |
 ムービー
ムービー コントローラー
コントローラー










 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)






















