+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Vibrio cholerae DdmD apo complex | |||||||||
 マップデータ マップデータ | Unsharpened map | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Helicase / Nuclease / Complex / Effector / IMMUNE SYSTEM | |||||||||
| 機能・相同性 | Helicase/UvrB N-terminal domain-containing protein 機能・相同性情報 機能・相同性情報 | |||||||||
| 生物種 |  | |||||||||
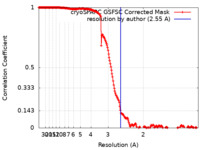
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.55 Å | |||||||||
 データ登録者 データ登録者 | Loeff L / Jinek M | |||||||||
| 資金援助 | European Union, 1件
| |||||||||
 引用 引用 |  ジャーナル: Science / 年: 2024 ジャーナル: Science / 年: 2024タイトル: Molecular mechanism of plasmid elimination by the DdmDE defense system. 著者: Luuk Loeff / David W Adams / Christelle Chanez / Sandrine Stutzmann / Laurie Righi / Melanie Blokesch / Martin Jinek /  要旨: Seventh-pandemic strains contain two pathogenicity islands that encode the DNA defense modules DdmABC and DdmDE. In this study, we used cryogenic electron microscopy to determine the mechanistic ...Seventh-pandemic strains contain two pathogenicity islands that encode the DNA defense modules DdmABC and DdmDE. In this study, we used cryogenic electron microscopy to determine the mechanistic basis for plasmid defense by DdmDE. The helicase-nuclease DdmD adopts an autoinhibited dimeric architecture. The prokaryotic Argonaute protein DdmE uses a DNA guide to target plasmid DNA. The structure of the DdmDE complex, validated by in vivo mutational studies, shows that DNA binding by DdmE triggers disassembly of the DdmD dimer and loading of monomeric DdmD onto the nontarget DNA strand. In vitro studies indicate that DdmD translocates in the 5'-to-3' direction, while partially degrading the plasmid DNA. These findings provide critical insights into the mechanism of DdmDE systems in plasmid elimination. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_50090.map.gz emd_50090.map.gz | 361.6 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-50090-v30.xml emd-50090-v30.xml emd-50090.xml emd-50090.xml | 18.9 KB 18.9 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_50090_fsc.xml emd_50090_fsc.xml | 19 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_50090.png emd_50090.png | 165.5 KB | ||
| マスクデータ |  emd_50090_msk_1.map emd_50090_msk_1.map | 729 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-50090.cif.gz emd-50090.cif.gz | 6.5 KB | ||
| その他 |  emd_50090_additional_1.map.gz emd_50090_additional_1.map.gz emd_50090_half_map_1.map.gz emd_50090_half_map_1.map.gz emd_50090_half_map_2.map.gz emd_50090_half_map_2.map.gz | 684.8 MB 675.9 MB 675.9 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-50090 http://ftp.pdbj.org/pub/emdb/structures/EMD-50090 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-50090 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-50090 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_50090_validation.pdf.gz emd_50090_validation.pdf.gz | 948.2 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_50090_full_validation.pdf.gz emd_50090_full_validation.pdf.gz | 947.7 KB | 表示 | |
| XML形式データ |  emd_50090_validation.xml.gz emd_50090_validation.xml.gz | 28.6 KB | 表示 | |
| CIF形式データ |  emd_50090_validation.cif.gz emd_50090_validation.cif.gz | 37.4 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-50090 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-50090 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-50090 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-50090 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  9ezxMC  9ezyC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_50090.map.gz / 形式: CCP4 / 大きさ: 729 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_50090.map.gz / 形式: CCP4 / 大きさ: 729 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Unsharpened map | ||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.65 Å | ||||||||||||||||||||||||||||||||||||
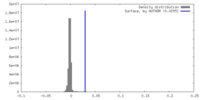
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-マスク #1
| ファイル |  emd_50090_msk_1.map emd_50090_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
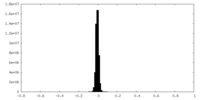
| 投影像・断面図 |
| ||||||||||||
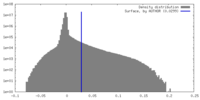
| 密度ヒストグラム |
-追加マップ: Sharpened EM map
| ファイル | emd_50090_additional_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Sharpened EM map | ||||||||||||
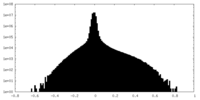
| 投影像・断面図 |
| ||||||||||||
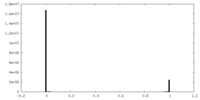
| 密度ヒストグラム |
-ハーフマップ: Half map A
| ファイル | emd_50090_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half map A | ||||||||||||
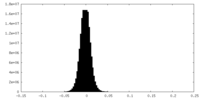
| 投影像・断面図 |
| ||||||||||||
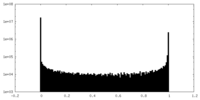
| 密度ヒストグラム |
-ハーフマップ: Half map A
| ファイル | emd_50090_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half map A | ||||||||||||
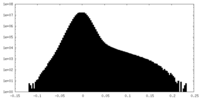
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Dimeric complex of the DdmD protein
| 全体 | 名称: Dimeric complex of the DdmD protein |
|---|---|
| 要素 |
|
-超分子 #1: Dimeric complex of the DdmD protein
| 超分子 | 名称: Dimeric complex of the DdmD protein / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 266 KDa |
-分子 #1: Helicase/UvrB N-terminal domain-containing protein
| 分子 | 名称: Helicase/UvrB N-terminal domain-containing protein / タイプ: protein_or_peptide / ID: 1 / コピー数: 2 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 136.427594 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: SNAMNVSIEE FTHFDFQLVP EPSPLDLVIT EPLKNHIEVN GVKSGALLPL PFQTGIGKTY TALNFLLQQM LEQVRSELKE ENTGKKSKR LLYYVTDSVD NVVSAKADLL KLIEKQTVKG EPRFTLEQQE YLKAQIVHLP NQSEQLLQCS DAVLNDVLIG F NLNAERDV ...文字列: SNAMNVSIEE FTHFDFQLVP EPSPLDLVIT EPLKNHIEVN GVKSGALLPL PFQTGIGKTY TALNFLLQQM LEQVRSELKE ENTGKKSKR LLYYVTDSVD NVVSAKADLL KLIEKQTVKG EPRFTLEQQE YLKAQIVHLP NQSEQLLQCS DAVLNDVLIG F NLNAERDV QAEWSAISGL RRHASNPEVK ISLNRQAGYF YRNLIDRLQK KQKGADRVLL SGSLLASVET LLPGEKIRNG SA HVAFLTT SKFLKGFHNT RSRYSPLRDL SGAVLIIDEI DKQNQVILSE LCKQQAQDLI WAIRTLRANF RDHQLESSPR YDK IEDLFE PLRERLEEFG TNWNLAFAFN TEGANLNERP VRLFSDRSFT HVSSATHKLS LKSDFLRRKN LIFSDEKVEG SLIE KHGLL TRFVNEADVI YQWFLGTMRK AVFQYWENVR GLEIEVRENR SLEGTFQEAV QSLLTHFNLQ EFESAVYESF DTRGL RQSA GGKANKLSSS KSYHHTGLKL VEVAHNQGTR DTVNCKASFL NTSPSGVLAD MVDAGAVILG ISATARADTV IHNFDF KYL NERLGNKLLS LSREQKQRVN NYYHSRRNYK DNGVVLTVKY LNSRDAFLDA LLEEYKPEAR SSHFILNHYL GIAESEQ AF VRSWLSKLLA SIKAFISSPD NRYMLSLLNR TLDTTRQNIN DFIQFCCDKW AKEFNVKTKT FFGVNADWMR LVGYDEIS K HLNTELGKVV VFSTYASMGA GKNPDYAVNL ALEGESLISV ADVTYSTQLR SDIDSIYLEK PTQLLLSDDY SHTANQLCQ FHQILSLQEN GELSPKSAEN WCRQQLMGMS RERSLQQYHQ TSDYQSAVRK YIEQAVGRAG RTSLKRKQIL LFVDSGLKEI LAEESRDPS LFSHEYVALV NKAKSAGKSI VEDRAVRRLF NLAQRNNKDG MLSIKALVHR LHNQPASKSD IQEWQDIRTQ L LRYPTVAF QPERFNRLYL QSMTKGYYRY QGNLDGDPNS FEFFDRVPYG DMVSEEDCSL ATLVQNQYVR PWFERKGFAC SW QKEANVM TPIMFTNIYK GALGEQAVEA VLTAFDFTFE EVPNSIYERF DNRVIFAGIE QPIWLDSKYW KHEGNESSEG YSS KIALVE EEFGPSKFIY VNALGDTSKP IRYLNSCFVE TSPQLAKVIE IPALIDDSNA DTNRTAVQEL IKWLHHS UniProtKB: Helicase/UvrB N-terminal domain-containing protein |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 1.5 mg/mL | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 8 構成要素:
| |||||||||
| 凍結 | 凍結剤: ETHANE / 装置: FEI VITROBOT MARK IV | |||||||||
| 詳細 | This sample was monodisperse. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | TFS KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 平均電子線量: 59.98 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 50.0 µm / 倍率(補正後): 130000 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.4 µm / 最小 デフォーカス(公称値): 1.0 µm |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 初期モデル | Chain - Source name: AlphaFold / Chain - Initial model type: in silico model / 詳細: Initial model was generated with alpha fold |
|---|---|
| 得られたモデル |  PDB-9ezx: |
 ムービー
ムービー コントローラー
コントローラー





 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)