+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Human DNA polymerase theta helicase domain tetramer, apo-form | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | DNA repair / helicase / ATPase / TRANSFERASE / DNA BINDING PROTEIN | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報single-stranded DNA endodeoxyribonuclease activity / HDR through MMEJ (alt-NHEJ) / double-strand break repair via alternative nonhomologous end joining / single-stranded DNA helicase activity / replication fork processing / site of DNA damage / negative regulation of double-strand break repair via homologous recombination / 5'-deoxyribose-5-phosphate lyase activity / error-prone translesion synthesis / somatic hypermutation of immunoglobulin genes ...single-stranded DNA endodeoxyribonuclease activity / HDR through MMEJ (alt-NHEJ) / double-strand break repair via alternative nonhomologous end joining / single-stranded DNA helicase activity / replication fork processing / site of DNA damage / negative regulation of double-strand break repair via homologous recombination / 5'-deoxyribose-5-phosphate lyase activity / error-prone translesion synthesis / somatic hypermutation of immunoglobulin genes / DNA helicase activity / base-excision repair / protein homooligomerization / RNA-directed DNA polymerase / RNA-directed DNA polymerase activity / double-strand break repair / site of double-strand break / DNA helicase / damaged DNA binding / DNA-directed DNA polymerase / DNA-directed DNA polymerase activity / DNA repair / DNA damage response / chromatin binding / Golgi apparatus / magnesium ion binding / ATP hydrolysis activity / nucleoplasm / ATP binding / identical protein binding / cytosol 類似検索 - 分子機能 | |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
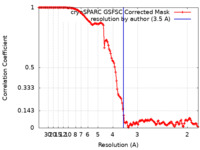
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.5 Å | |||||||||
 データ登録者 データ登録者 | Ito F / Li Z / Chen XS | |||||||||
| 資金援助 |  米国, 1件 米国, 1件
| |||||||||
 引用 引用 |  ジャーナル: bioRxiv / 年: 2024 ジャーナル: bioRxiv / 年: 2024タイトル: Structural Basis for Polθ-Helicase DNA Binding and Microhomology-Mediated End-Joining. 著者: Fumiaki Ito / Ziyuan Li / Leonid Minakhin / Htet A Khant / Richard T Pomerantz / Xiaojiang S Chen /  要旨: DNA double-strand breaks (DSBs) present a critical threat to genomic integrity, often precipitating genomic instability and oncogenesis. Repair of DSBs predominantly occurs through homologous ...DNA double-strand breaks (DSBs) present a critical threat to genomic integrity, often precipitating genomic instability and oncogenesis. Repair of DSBs predominantly occurs through homologous recombination (HR) and non-homologous end joining (NHEJ). In HR-deficient cells, DNA polymerase theta (Polθ) becomes critical for DSB repair via microhomology-mediated end joining (MMEJ), also termed theta-mediated end joining (TMEJ). Thus, Polθ is synthetically lethal with BRCA1/2 and other HR factors, underscoring its potential as a therapeutic target in HR-deficient cancers. However, the molecular mechanisms governing Polθ-mediated MMEJ remain poorly understood. Here we present a series of cryo-electron microscopy structures of the Polθ helicase domain (Polθ-hel) in complex with DNA containing 3'-overhang. The structures reveal the sequential conformations adopted by Polθ-hel during the critical phases of DNA binding, microhomology searching, and microhomology annealing. The stepwise conformational changes within the Polθ-hel subdomains and its functional dimeric state are pivotal for aligning the 3'-overhangs, facilitating the microhomology search and subsequent annealing necessary for DSB repair via MMEJ. Our findings illustrate the essential molecular switches within Polθ-hel that orchestrate the MMEJ process in DSB repair, laying the groundwork for the development of targeted therapies against the Polθ-hel. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_43818.map.gz emd_43818.map.gz | 125.3 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-43818-v30.xml emd-43818-v30.xml emd-43818.xml emd-43818.xml | 15.3 KB 15.3 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_43818_fsc.xml emd_43818_fsc.xml | 13.1 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_43818.png emd_43818.png | 89 KB | ||
| Filedesc metadata |  emd-43818.cif.gz emd-43818.cif.gz | 5.8 KB | ||
| その他 |  emd_43818_half_map_1.map.gz emd_43818_half_map_1.map.gz emd_43818_half_map_2.map.gz emd_43818_half_map_2.map.gz | 226.2 MB 226.2 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-43818 http://ftp.pdbj.org/pub/emdb/structures/EMD-43818 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-43818 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-43818 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_43818_validation.pdf.gz emd_43818_validation.pdf.gz | 929.5 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_43818_full_validation.pdf.gz emd_43818_full_validation.pdf.gz | 929.1 KB | 表示 | |
| XML形式データ |  emd_43818_validation.xml.gz emd_43818_validation.xml.gz | 22.1 KB | 表示 | |
| CIF形式データ |  emd_43818_validation.cif.gz emd_43818_validation.cif.gz | 28.6 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-43818 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-43818 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-43818 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-43818 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  9aslMC  8w0aC  9asjC  9askC  9c5qC  40760  40761 M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_43818.map.gz / 形式: CCP4 / 大きさ: 244.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_43818.map.gz / 形式: CCP4 / 大きさ: 244.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.92 Å | ||||||||||||||||||||||||||||||||||||
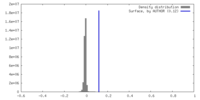
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: #2
| ファイル | emd_43818_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
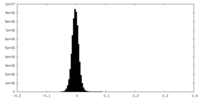
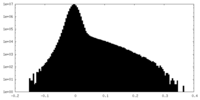
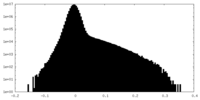
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_43818_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
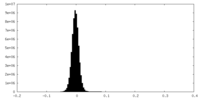
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Human DNA polymerase theta helicase domain tetramer, apo-form
| 全体 | 名称: Human DNA polymerase theta helicase domain tetramer, apo-form |
|---|---|
| 要素 |
|
-超分子 #1: Human DNA polymerase theta helicase domain tetramer, apo-form
| 超分子 | 名称: Human DNA polymerase theta helicase domain tetramer, apo-form タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 398 KDa |
-分子 #1: DNA polymerase theta
| 分子 | 名称: DNA polymerase theta / タイプ: protein_or_peptide / ID: 1 / コピー数: 4 / 光学異性体: LEVO / EC番号: DNA-directed DNA polymerase |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 99.802539 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MNLLRRSGKR RRSESGSDSF SGSGGDSSAS PQFLSGSVLS PPPGLGRCLK AAAAGECKPT VPDYERDKLL LANWGLPKAV LEKYHSFGV KKMFEWQAEC LLLGQVLEGK NLVYSAPTSA GKTLVAELLI LKRVLEMRKK ALFILPFVSV AKEKKYYLQS L FQEVGIKV ...文字列: MNLLRRSGKR RRSESGSDSF SGSGGDSSAS PQFLSGSVLS PPPGLGRCLK AAAAGECKPT VPDYERDKLL LANWGLPKAV LEKYHSFGV KKMFEWQAEC LLLGQVLEGK NLVYSAPTSA GKTLVAELLI LKRVLEMRKK ALFILPFVSV AKEKKYYLQS L FQEVGIKV DGYMGSTSPS RHFSSLDIAV CTIERANGLI NRLIEENKMD LLGMVVVDEL HMLGDSHRGY LLELLLTKIC YI TRKSASC QADLASSLSN AVQIVGMSAT LPNLELVASW LNAELYHTDF RPVPLLESVK VGNSIYDSSM KLVREFEPML QVK GDEDHV VSLCYETICD NHSVLLFCPS KKWCEKLADI IAREFYNLHH QAEGLVKPSE CPPVILEQKE LLEVMDQLRR LPSG LDSVL QKTVPWGVAF HHAGLTFEER DIIEGAFRQG LIRVLAATST LSSGVNLPAR RVIIRTPIFG GRPLDILTYK QMVGR AGRK GVDTVGESIL ICKNSEKSKG IALLQGSLKP VRSCLQRREG EEVTGSMIRA ILEIIVGGVA STSQDMHTYA ACTFLA ASM KEGKQGIQRN QESVQLGAIE ACVMWLLENE FIQSTEASDG TEGKVYHPTH LGSATLSSSL SPADTLDIFA DLQRAMK GF VLENDLHILY LVTPMFEDWT TIDWYRFFCL WEKLPTSMKR VAELVGVEEG FLARCVKGKV VARTERQHRQ MAIHKRFF T SLVLLDLISE VPLREINQKY GCNRGQIQSL QQSAAVYAGM ITVFSNRLGW HNMELLLSQF QKRLTFGIQR ELCDLVRVS LLNAQRARVL YASGFHTVAD LARANIVEVE VILKNAVPFK SARKAVDEEE EAVEERRNMR TIWVTGRKGL TEREAAALIV EEARMILQQ DLVEM UniProtKB: DNA polymerase theta |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 1 mg/mL |
|---|---|
| 緩衝液 | pH: 7.5 |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | TFS GLACIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: FEI FALCON IV (4k x 4k) 撮影したグリッド数: 1 / 実像数: 4511 / 平均露光時間: 8.0 sec. / 平均電子線量: 58.0 e/Å2 |
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 50.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.0 mm / 最大 デフォーカス(公称値): 3.0 µm / 最小 デフォーカス(公称値): 1.0 µm / 倍率(公称値): 150000 |
 ムービー
ムービー コントローラー
コントローラー












 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)