[日本語] English
 万見
万見- EMDB-43750: Human liver phosphofructokinase-1 filament in the T-state conformation -
+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Human liver phosphofructokinase-1 filament in the T-state conformation | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | PFK / glycolysis / TRANSFERASE | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報6-phosphofructokinase complex / 6-phosphofructokinase / fructose binding / 6-phosphofructokinase activity / fructose-6-phosphate binding / fructose 1,6-bisphosphate metabolic process / fructose 6-phosphate metabolic process / canonical glycolysis / Glycolysis / response to glucose ...6-phosphofructokinase complex / 6-phosphofructokinase / fructose binding / 6-phosphofructokinase activity / fructose-6-phosphate binding / fructose 1,6-bisphosphate metabolic process / fructose 6-phosphate metabolic process / canonical glycolysis / Glycolysis / response to glucose / glycolytic process / negative regulation of insulin secretion / kinase binding / secretory granule lumen / ficolin-1-rich granule lumen / Neutrophil degranulation / extracellular exosome / extracellular region / ATP binding / metal ion binding / identical protein binding / membrane / cytosol 類似検索 - 分子機能 | |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.1 Å | |||||||||
 データ登録者 データ登録者 | Lynch EM / Kollman JM / Webb BA | |||||||||
| 資金援助 |  米国, 1件 米国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2024 ジャーナル: Nat Commun / 年: 2024タイトル: Structural basis for allosteric regulation of human phosphofructokinase-1. 著者: Eric M Lynch / Heather Hansen / Lauren Salay / Madison Cooper / Stepan Timr / Justin M Kollman / Bradley A Webb /   要旨: Phosphofructokinase-1 (PFK1) catalyzes the rate-limiting step of glycolysis, committing glucose to conversion into cellular energy. PFK1 is highly regulated to respond to the changing energy needs of ...Phosphofructokinase-1 (PFK1) catalyzes the rate-limiting step of glycolysis, committing glucose to conversion into cellular energy. PFK1 is highly regulated to respond to the changing energy needs of the cell. In bacteria, the structural basis of PFK1 regulation is a textbook example of allostery; molecular signals of low and high cellular energy promote transition between an active R-state and inactive T-state conformation, respectively. Little is known, however, about the structural basis for regulation of eukaryotic PFK1. Here, we determine structures of the human liver isoform of PFK1 (PFKL) in the R- and T-state by cryoEM, providing insight into eukaryotic PFK1 allosteric regulatory mechanisms. The T-state structure reveals conformational differences between the bacterial and eukaryotic enzyme, the mechanisms of allosteric inhibition by ATP binding at multiple sites, and an autoinhibitory role of the C-terminus in stabilizing the T-state. We also determine structures of PFKL filaments that define the mechanism of higher-order assembly and demonstrate that these structures are necessary for higher-order assembly of PFKL in cells. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_43750.map.gz emd_43750.map.gz | 26.8 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-43750-v30.xml emd-43750-v30.xml emd-43750.xml emd-43750.xml | 18.2 KB 18.2 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_43750.png emd_43750.png | 76.5 KB | ||
| Filedesc metadata |  emd-43750.cif.gz emd-43750.cif.gz | 6.1 KB | ||
| その他 |  emd_43750_additional_1.map.gz emd_43750_additional_1.map.gz emd_43750_half_map_1.map.gz emd_43750_half_map_1.map.gz emd_43750_half_map_2.map.gz emd_43750_half_map_2.map.gz | 16.2 MB 226.1 MB 226.1 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-43750 http://ftp.pdbj.org/pub/emdb/structures/EMD-43750 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-43750 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-43750 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_43750_validation.pdf.gz emd_43750_validation.pdf.gz | 962.9 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_43750_full_validation.pdf.gz emd_43750_full_validation.pdf.gz | 962.5 KB | 表示 | |
| XML形式データ |  emd_43750_validation.xml.gz emd_43750_validation.xml.gz | 15.8 KB | 表示 | |
| CIF形式データ |  emd_43750_validation.cif.gz emd_43750_validation.cif.gz | 18.7 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-43750 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-43750 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-43750 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-43750 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_43750.map.gz / 形式: CCP4 / 大きさ: 244.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_43750.map.gz / 形式: CCP4 / 大きさ: 244.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.05 Å | ||||||||||||||||||||||||||||||||||||
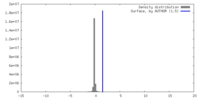
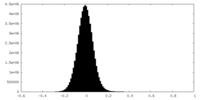
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-追加マップ: #1
| ファイル | emd_43750_additional_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
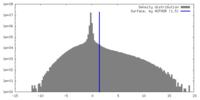
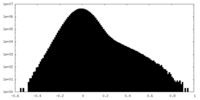
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_43750_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
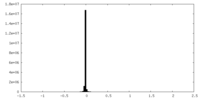
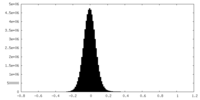
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_43750_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
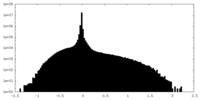
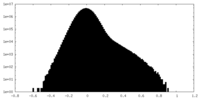
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : PFKL filament
| 全体 | 名称: PFKL filament |
|---|---|
| 要素 |
|
-超分子 #1: PFKL filament
| 超分子 | 名称: PFKL filament / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
-分子 #1: ATP-dependent 6-phosphofructokinase, liver type
| 分子 | 名称: ATP-dependent 6-phosphofructokinase, liver type / タイプ: protein_or_peptide / ID: 1 / コピー数: 8 / 光学異性体: LEVO / EC番号: 6-phosphofructokinase |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 85.120375 KDa |
| 組換発現 | 生物種:  unidentified baculovirus (ウイルス) unidentified baculovirus (ウイルス) |
| 配列 | 文字列: MAAVDLEKLR ASGAGKAIGV LTSGGDAQGM NAAVRAVTRM GIYVGAKVFL IYEGYEGLVE GGENIKQANW LSVSNIIQLG GTIIGSARC KAFTTREGRR AAAYNLVQHG ITNLCVIGGD GSLTGANIFR SEWGSLLEEL VAEGKISETT ARTYSHLNIA G LVGSIDND ...文字列: MAAVDLEKLR ASGAGKAIGV LTSGGDAQGM NAAVRAVTRM GIYVGAKVFL IYEGYEGLVE GGENIKQANW LSVSNIIQLG GTIIGSARC KAFTTREGRR AAAYNLVQHG ITNLCVIGGD GSLTGANIFR SEWGSLLEEL VAEGKISETT ARTYSHLNIA G LVGSIDND FCGTDMTIGT DSALHRIMEV IDAITTTAQS HQRTFVLEVM GRHCGYLALV SALASGADWL FIPEAPPEDG WE NFMCERL GETRSRGSRL NIIIIAEGAI DRNGKPISSS YVKDLVVQRL GFDTRVTVLG HVQRGGTPSA FDRILSSKMG MEA VMALLE ATPDTPACVV TLSGNQSVRL PLMECVQMTK EVQKAMDDKR FDEATQLRGG SFENNWNIYK LLAHQKPPKE KSNF SLAIL NVGAPAAGMN AAVRSAVRTG ISHGHTVYVV HDGFEGLAKG QVQEVGWHDV AGWLGRGGSM LGTKRTLPKG QLESI VENI RIYGIHALLV VGGFEAYEGV LQLVEARGRY EELCIVMCVI PATISNNVPG TDFSLGSDTA VNAAMESCDR IKQSAS GTK RRVFIVETMG GYCGYLATVT GIAVGADAAY VFEDPFNIHD LKVNVEHMTE KMKTDIQRGL VLRNEKCHDY YTTEFLY NL YSSEGKGVFD CRTNVLGHLQ QGGAPTPFDR NYGTKLGVKA MLWLSEKLRE VYRKGRVFAN APDSACVIGL KKKAVAFS P VTELKKDTDF EHRMPREQWW LSLRLMLKML AQYRISMAAY VSGELEHVTR RTLSMDKGF UniProtKB: ATP-dependent 6-phosphofructokinase, liver type |
-分子 #2: 1,6-di-O-phosphono-beta-D-fructofuranose
| 分子 | 名称: 1,6-di-O-phosphono-beta-D-fructofuranose / タイプ: ligand / ID: 2 / コピー数: 8 / 式: FBP |
|---|---|
| 分子量 | 理論値: 340.116 Da |
| Chemical component information |  ChemComp-FBP: |
-分子 #3: ADENOSINE-5'-TRIPHOSPHATE
| 分子 | 名称: ADENOSINE-5'-TRIPHOSPHATE / タイプ: ligand / ID: 3 / コピー数: 24 / 式: ATP |
|---|---|
| 分子量 | 理論値: 507.181 Da |
| Chemical component information |  ChemComp-ATP: |
-分子 #4: MAGNESIUM ION
| 分子 | 名称: MAGNESIUM ION / タイプ: ligand / ID: 4 / コピー数: 8 / 式: MG |
|---|---|
| 分子量 | 理論値: 24.305 Da |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.5 |
|---|---|
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 平均電子線量: 90.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.4 µm / 最小 デフォーカス(公称値): 0.8 µm / 倍率(公称値): 130000 |
| 試料ステージ | ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 初期モデル | Chain - Source name: Modeller / Chain - Initial model type: in silico model |
|---|---|
| 精密化 | 空間: REAL / プロトコル: FLEXIBLE FIT |
| 得られたモデル |  PDB-8w2j: |
 ムービー
ムービー コントローラー
コントローラー











 X (Sec.)
X (Sec.) Y (Row.)
Y (Row.) Z (Col.)
Z (Col.)