+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-3032 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of ATP-bound IstB | |||||||||
 マップデータ マップデータ | IstB decamer bound to ATP | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | AAA+ / ATPase / IS21 / DNA transposition / DNA binding / DNA remodeling | |||||||||
| 生物種 |   Geobacillus stearothermophilus (バクテリア) Geobacillus stearothermophilus (バクテリア) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 16.0 Å | |||||||||
 データ登録者 データ登録者 | Arias-Palomo E / Berger JM | |||||||||
 引用 引用 |  ジャーナル: Cell / 年: 2015 ジャーナル: Cell / 年: 2015タイトル: An Atypical AAA+ ATPase Assembly Controls Efficient Transposition through DNA Remodeling and Transposase Recruitment. 著者: Ernesto Arias-Palomo / James M Berger /  要旨: Transposons are ubiquitous genetic elements that drive genome rearrangements, evolution, and the spread of infectious disease and drug-resistance. Many transposons, such as Mu, Tn7, and IS21, require ...Transposons are ubiquitous genetic elements that drive genome rearrangements, evolution, and the spread of infectious disease and drug-resistance. Many transposons, such as Mu, Tn7, and IS21, require regulatory AAA+ ATPases for function. We use X-ray crystallography and cryo-electron microscopy to show that the ATPase subunit of IS21, IstB, assembles into a clamshell-shaped decamer that sandwiches DNA between two helical pentamers of ATP-associated AAA+ domains, sharply bending the duplex into a 180° U-turn. Biochemical studies corroborate key features of the structure and further show that the IS21 transposase, IstA, recognizes the IstB•DNA complex and promotes its disassembly by stimulating ATP hydrolysis. Collectively, these studies reveal a distinct manner of higher-order assembly and client engagement by a AAA+ ATPase and suggest a mechanistic model where IstB binding and subsequent DNA bending primes a selected insertion site for efficient transposition. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_3032.map.gz emd_3032.map.gz | 705 KB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-3032-v30.xml emd-3032-v30.xml emd-3032.xml emd-3032.xml | 8 KB 8 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_3032.png emd_3032.png | 316.9 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-3032 http://ftp.pdbj.org/pub/emdb/structures/EMD-3032 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-3032 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-3032 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_3032_validation.pdf.gz emd_3032_validation.pdf.gz | 186.6 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_3032_full_validation.pdf.gz emd_3032_full_validation.pdf.gz | 185.7 KB | 表示 | |
| XML形式データ |  emd_3032_validation.xml.gz emd_3032_validation.xml.gz | 5.4 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3032 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3032 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3032 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3032 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_3032.map.gz / 形式: CCP4 / 大きさ: 11.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_3032.map.gz / 形式: CCP4 / 大きさ: 11.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | IstB decamer bound to ATP | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 2.05 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
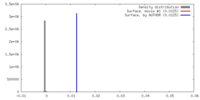
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : ATP-bound IstB decamer
| 全体 | 名称: ATP-bound IstB decamer |
|---|---|
| 要素 |
|
-超分子 #1000: ATP-bound IstB decamer
| 超分子 | 名称: ATP-bound IstB decamer / タイプ: sample / ID: 1000 / 詳細: The sample was monodisperse 集合状態: IstB oligomerizes into pentamer of dimers when bound to ATP Number unique components: 1 |
|---|---|
| 分子量 | 実験値: 290 KDa / 理論値: 290 KDa / 手法: Analytical size exclusion chromatography |
-分子 #1: IstB
| 分子 | 名称: IstB / タイプ: protein_or_peptide / ID: 1 / コピー数: 10 / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:   Geobacillus stearothermophilus (バクテリア) Geobacillus stearothermophilus (バクテリア) |
| 分子量 | 理論値: 29 KDa |
| 組換発現 | 生物種:  |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 2 mg/mL |
|---|---|
| 緩衝液 | pH: 7.5 詳細: 20 mM HEPES pH 7.5, 300 mM NaCl, 5 mM MgCl2, 1.5% glycerol, 1 mM DTT, 1 mM ATP |
| グリッド | 詳細: C-Flat 400 mesh 2/2. Open holes |
| 凍結 | 凍結剤: ETHANE / 装置: FEI VITROBOT MARK II / 手法: Blot for 4 seconds before plunging |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TECNAI F20 |
|---|---|
| 日付 | 2013年6月12日 |
| 撮影 | カテゴリ: CCD フィルム・検出器のモデル: GATAN ULTRASCAN 4000 (4k x 4k) 平均電子線量: 20 e/Å2 |
| 電子線 | 加速電圧: 120 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.5 µm / 最小 デフォーカス(公称値): 1.3 µm / 倍率(公称値): 100000 |
| 試料ステージ | 試料ホルダーモデル: GATAN LIQUID NITROGEN |
| 実験機器 |  モデル: Tecnai F20 / 画像提供: FEI Company |
- 画像解析
画像解析
| CTF補正 | 詳細: Each micrograph |
|---|---|
| 最終 再構成 | 想定した対称性 - 点群: C2 (2回回転対称) / アルゴリズム: OTHER / 解像度のタイプ: BY AUTHOR / 解像度: 16.0 Å / 解像度の算出法: OTHER / ソフトウェア - 名称: EMAN2, SPARX / 使用した粒子像数: 34064 |
 ムービー
ムービー コントローラー
コントローラー











 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)