+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Nodavirus RNA replication proto-crown from baculovirus-expressed viral protein A minus RNA1 template | |||||||||
 マップデータ マップデータ | Nodavirus RNA replication proto-crown from baculovirus-expressed viral protein A minus RNA1 template | |||||||||
 試料 試料 |
| |||||||||
| 生物種 |  Flock House virus (ウイルス) Flock House virus (ウイルス) | |||||||||
| 手法 | サブトモグラム平均法 / クライオ電子顕微鏡法 / 解像度: 12.6 Å | |||||||||
 データ登録者 データ登録者 | Zhan H / Unchwaniwala N / Rebolledo Viveros A / Pennington J / Horswill M / Broadberry R / Myers J / den Boon J / Grant T / Ahlquist P | |||||||||
| 資金援助 |  米国, 1件 米国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Proc Natl Acad Sci U S A / 年: 2023 ジャーナル: Proc Natl Acad Sci U S A / 年: 2023タイトル: Nodavirus RNA replication crown architecture reveals proto-crown precursor and viral protein A conformational switching. 著者: Hong Zhan / Nuruddin Unchwaniwala / Andrea Rebolledo-Viveros / Janice Pennington / Mark Horswill / Roma Broadberry / Jonathan Myers / Johan A den Boon / Timothy Grant / Paul Ahlquist /  要旨: Positive-strand RNA viruses replicate their genomes in virus-induced membrane vesicles, and the resulting RNA replication complexes are a major target for virus control. Nodavirus studies first ...Positive-strand RNA viruses replicate their genomes in virus-induced membrane vesicles, and the resulting RNA replication complexes are a major target for virus control. Nodavirus studies first revealed viral RNA replication proteins forming a 12-fold symmetric "crown" at the vesicle opening to the cytosol, an arrangement recently confirmed to extend to distantly related alphaviruses. Using cryoelectron microscopy (cryo-EM), we show that mature nodavirus crowns comprise two stacked 12-mer rings of multidomain viral RNA replication protein A. Each ring contains an ~19 nm circle of C-proximal polymerase domains, differentiated by strikingly diverged positions of N-proximal RNA capping/membrane binding domains. The lower ring is a "proto-crown" precursor that assembles prior to RNA template recruitment, RNA synthesis, and replication vesicle formation. In this proto-crown, the N-proximal segments interact to form a toroidal central floor, whose 3.1 Å resolution structure reveals many mechanistic details of the RNA capping/membrane binding domains. In the upper ring, cryo-EM fitting indicates that the N-proximal domains extend radially outside the polymerases, forming separated, membrane-binding "legs." The polymerase and N-proximal domains are connected by a long linker accommodating the conformational switch between the two rings and possibly also polymerase movements associated with RNA synthesis and nonsymmetric electron density in the lower center of mature crowns. The results reveal remarkable viral protein multifunctionality, conformational flexibility, and evolutionary plasticity and insights into (+)RNA virus replication and control. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_29217.map.gz emd_29217.map.gz | 64.4 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-29217-v30.xml emd-29217-v30.xml emd-29217.xml emd-29217.xml | 16.5 KB 16.5 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
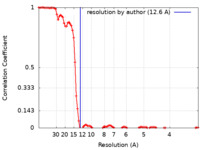
| FSC (解像度算出) |  emd_29217_fsc.xml emd_29217_fsc.xml | 9 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_29217.png emd_29217.png | 108.9 KB | ||
| その他 |  emd_29217_half_map_1.map.gz emd_29217_half_map_1.map.gz emd_29217_half_map_2.map.gz emd_29217_half_map_2.map.gz | 65 MB 65 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-29217 http://ftp.pdbj.org/pub/emdb/structures/EMD-29217 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-29217 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-29217 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_29217.map.gz / 形式: CCP4 / 大きさ: 70.2 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_29217.map.gz / 形式: CCP4 / 大きさ: 70.2 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Nodavirus RNA replication proto-crown from baculovirus-expressed viral protein A minus RNA1 template | ||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.645 Å | ||||||||||||||||||||||||||||||||||||
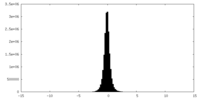
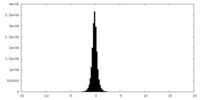
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: Nodavirus RNA replication proto-crown from baculovirus-expressed viral protein...
| ファイル | emd_29217_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Nodavirus RNA replication proto-crown from baculovirus-expressed viral protein A minus RNA1 template, unmasked and unfiltered half map1. | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
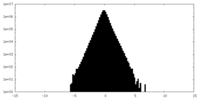
| 密度ヒストグラム |
-ハーフマップ: Nodavirus RNA replication proto-crown from baculovirus-expressed viral protein...
| ファイル | emd_29217_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Nodavirus RNA replication proto-crown from baculovirus-expressed viral protein A minus RNA1 template, unmasked and unfiltered half map2. | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
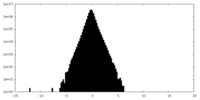
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Flock House virus
| 全体 | 名称:  Flock House virus (ウイルス) Flock House virus (ウイルス) |
|---|---|
| 要素 |
|
-超分子 #1: Flock House virus
| 超分子 | 名称: Flock House virus / タイプ: complex / ID: 1 / キメラ: Yes / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  Flock House virus (ウイルス) Flock House virus (ウイルス) |
-分子 #1: Flock House nodavirus protein A
| 分子 | 名称: Flock House nodavirus protein A / タイプ: protein_or_peptide / ID: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Flock House virus (ウイルス) Flock House virus (ウイルス) |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MTLKVILGEH QITRTELLVG IATVSGCGAV VYCISKFWGY GAIAPYPQSG GNRVTRALQR AVIDKTKTPI ETRFYPLDSL RTVTPKRVAD NGHAVSGAVR DAARRLIDES ITAVGGSKFE VNPNPNSSTG LRNHFHFAVG DLAQDFRNDT PADDAFIVGV DVDYYVTEPD ...文字列: MTLKVILGEH QITRTELLVG IATVSGCGAV VYCISKFWGY GAIAPYPQSG GNRVTRALQR AVIDKTKTPI ETRFYPLDSL RTVTPKRVAD NGHAVSGAVR DAARRLIDES ITAVGGSKFE VNPNPNSSTG LRNHFHFAVG DLAQDFRNDT PADDAFIVGV DVDYYVTEPD VLLEHMRPVV LHTFNPKKVS GFDADSPFTI KNNLVEYKVS GGAAWVHPVW DWCEAGEFIA SRVRTSWKEW FLQLPLRMIG LEKVGYHKIH HCRPWTDCPD RALVYTIPQY VIWRFNWIDT ELHVRKLKRI EYQDETKPGW NRLEYVTDKN ELLVSIGREG EHAQITIEKE KLDMLSGLSA TQSVNARLIG MGHKDPQYTS MIVQYYTGKK VVSPISPTVY KPTMPRVHWP VTSDADVPEV SARQYTLPIV SDCMMMPMIK RWETMSESIE RRVTFVANDK KPSDRIAKIA ETFVKLMNGP FKDLDPLSIE ETIERLNKPS QQLQLRAVFE MIGVKPRQLI ESFNKNEPGM KSSRIISGFP DILFILKVSR YTLAYSDIVL HAEHNEHWYY PGRNPTEIAD GVCEFVSDCD AEVIETDFSN LDGRVSSWMQ RNIAQKAMVQ AFRPEYRDEI ISFMDTIINC PAKAKRFGFR YEPGVGVKSG SPTTTPHNTQ YNGCVEFTAL TFEHPDAEPE DLFRLIGPKC GDDGLSRAII QKSINRAAKC FGLELKVERY NPEIGLCFLS RVFVDPLATT TTIQDPLRTL RKLHLTTRDP TIPLADAACD RVEGYLCTDA LTPLISDYCK MVLRLYGPTA STEQVRNQRR SRNKEKPYWL TCDGSWPQHP QDAHLMKQVL IKRTAIDEDQ VDALIGRFAA MKDVWEKITH DSEESAAACT FDEDGVAPNS VDESLPMLND AKQTRANPGT SRPHSNGGGS SHGNELPRRT EQRAQGPRQP ARLPKQGKTN GKSDGNITAG ETQRGGIPRG KGPRGGKTNT RRTPPKAGAQ PQPSNNRK |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | サブトモグラム平均法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.4 |
|---|---|
| グリッド | モデル: Quantifoil R2/2 / 材質: COPPER / メッシュ: 200 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 60 sec. |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 295 K / 装置: FEI VITROBOT MARK III |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| ソフトウェア | 名称: SerialEM (ver. 3.8) |
| 撮影 | フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) 平均電子線量: 4.86 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 100.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 3.5 µm / 最小 デフォーカス(公称値): 3.5 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー












 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)