+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of coagulation factor V short | ||||||||||||
 マップデータ マップデータ | Primary Map | ||||||||||||
 試料 試料 |
| ||||||||||||
 キーワード キーワード | BLOOD CLOTTING | ||||||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | ||||||||||||
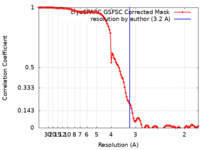
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.2 Å | ||||||||||||
 データ登録者 データ登録者 | Mohammed BM / Pelc LA / Rau MJ / Di Cera E | ||||||||||||
| 資金援助 |  米国, 3件 米国, 3件
| ||||||||||||
 引用 引用 |  ジャーナル: Blood / 年: 2023 ジャーナル: Blood / 年: 2023タイトル: Cryo-EM structure of coagulation factor V short. 著者: Bassem M Mohammed / Leslie A Pelc / Michael J Rau / Enrico Di Cera /  要旨: Coagulation factor V (fV) is the precursor of activated fV (fVa), an essential component of the prothrombinase complex required for the rapid activation of prothrombin in the penultimate step of the ...Coagulation factor V (fV) is the precursor of activated fV (fVa), an essential component of the prothrombinase complex required for the rapid activation of prothrombin in the penultimate step of the coagulation cascade. In addition, fV regulates the tissue factor pathway inhibitor α (TFPIα) and protein C pathways that inhibit the coagulation response. A recent cryogenic electron microscopy (cryo-EM) structure of fV has revealed the architecture of its A1-A2-B-A3-C1-C2 assembly but left the mechanism that keeps fV in its inactive state unresolved because of an intrinsic disorder in the B domain. A splice variant of fV, fV short, carries a large deletion of the B domain that produces constitutive fVa-like activity and unmasks epitopes for the binding of TFPIα. The cryo-EM structure of fV short was solved at 3.2 Å resolution and revealed the arrangement of the entire A1-A2-B-A3-C1-C2 assembly. The shorter B domain stretches across the entire width of the protein, making contacts with the A1, A2, and A3 domains but suspended over the C1 and C2 domains. In the portion distal to the splice site, several hydrophobic clusters and acidic residues provide a potential binding site for the basic C-terminal end of TFPIα. In fV, these epitopes may bind intramolecularly to the basic region of the B domain. The cryo-EM structure reported in this study advances our understanding of the mechanism that keeps fV in its inactive state, provides new targets for mutagenesis and facilitates future structural analysis of fV short in complex with TFPIα, protein S, and fXa. | ||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_29009.map.gz emd_29009.map.gz | 72.7 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-29009-v30.xml emd-29009-v30.xml emd-29009.xml emd-29009.xml | 17.9 KB 17.9 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_29009_fsc.xml emd_29009_fsc.xml | 11.1 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_29009.png emd_29009.png | 70 KB | ||
| マスクデータ |  emd_29009_msk_1.map emd_29009_msk_1.map | 144.7 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-29009.cif.gz emd-29009.cif.gz | 6 KB | ||
| その他 |  emd_29009_half_map_1.map.gz emd_29009_half_map_1.map.gz emd_29009_half_map_2.map.gz emd_29009_half_map_2.map.gz | 134.1 MB 134.1 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-29009 http://ftp.pdbj.org/pub/emdb/structures/EMD-29009 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-29009 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-29009 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_29009_validation.pdf.gz emd_29009_validation.pdf.gz | 916.4 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_29009_full_validation.pdf.gz emd_29009_full_validation.pdf.gz | 916 KB | 表示 | |
| XML形式データ |  emd_29009_validation.xml.gz emd_29009_validation.xml.gz | 19.6 KB | 表示 | |
| CIF形式データ |  emd_29009_validation.cif.gz emd_29009_validation.cif.gz | 25.2 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-29009 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-29009 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-29009 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-29009 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_29009.map.gz / 形式: CCP4 / 大きさ: 144.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_29009.map.gz / 形式: CCP4 / 大きさ: 144.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Primary Map | ||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.9 Å | ||||||||||||||||||||||||||||||||||||
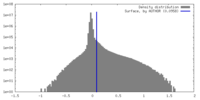
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-マスク #1
| ファイル |  emd_29009_msk_1.map emd_29009_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
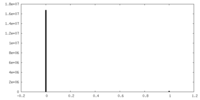
| 密度ヒストグラム |
-ハーフマップ: Half Map 1
| ファイル | emd_29009_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half Map 1 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
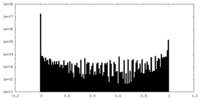
| 密度ヒストグラム |
-ハーフマップ: Half Map 2
| ファイル | emd_29009_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half Map 2 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
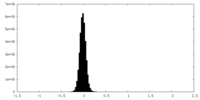
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Recombinantly expressed coagulation factor V short full length wi...
| 全体 | 名称: Recombinantly expressed coagulation factor V short full length with a c-terminus HPC4 tag |
|---|---|
| 要素 |
|
-超分子 #1: Recombinantly expressed coagulation factor V short full length wi...
| 超分子 | 名称: Recombinantly expressed coagulation factor V short full length with a c-terminus HPC4 tag タイプ: tissue / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) / 器官: Liver / 組織: Blood Homo sapiens (ヒト) / 器官: Liver / 組織: Blood |
-分子 #1: Coagulation Factor V short
| 分子 | 名称: Coagulation Factor V short / タイプ: protein_or_peptide / ID: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) / 器官: Liver / 組織: Blood Homo sapiens (ヒト) / 器官: Liver / 組織: Blood |
| 組換発現 | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 配列 | 文字列: AQLRQFYVAA QGISWSYRPE PTNSSLNLSV TSFKKIVYRE YEPYFKKEKP QSTISGLLGP TLYAEVGDII KVHFKNKADK PLSIHPQGIR YSKLSEGASY LDHTFPAEKM DDAVAPGREY TYEWSISEDS GPTHDDPPCL THIYYSHENL IEDFNSGLIG PLLICKKGTL ...文字列: AQLRQFYVAA QGISWSYRPE PTNSSLNLSV TSFKKIVYRE YEPYFKKEKP QSTISGLLGP TLYAEVGDII KVHFKNKADK PLSIHPQGIR YSKLSEGASY LDHTFPAEKM DDAVAPGREY TYEWSISEDS GPTHDDPPCL THIYYSHENL IEDFNSGLIG PLLICKKGTL TEGGTQKTFD KQIVLLFAVF DESKSWSQSS SLMYTVNGYV NGTMPDITVC AHDHISWHLL GMSSGPELFS IHFNGQVLEQ NHHKVSAITL VSATSTTANM TVGPEGKWII SSLTPKHLQA GMQAYIDIKN CPKKTRNLKK ITREQRRHMK RWEYFIAAEE VIWDYAPVIP ANMDKKYRSQ HLDNFSNQIG KHYKKVMYTQ YEDESFTKHT VNPNMKEDGI LGPIIRAQVR DTLKIVFKNM ASRPYSIYPH GVTFSPYEDE VNSSFTSGRN NTMIRAVQPG ETYTYKWNIL EFDEPTENDA QCLTRPYYSD VDIMRDIASG LIGLLLICKS RSLDRRGIQR AADIEQQAVF AVFDENKSWY LEDNINKFCE NPDEVKRDDP KFYESNIMST INGYVPESIT TLGFCFDDTV QWHFCSVGTQ NEILTIHFTG HSFIYGKRHE DTLTLFPMRG ESVTVTMDNV GTWMLTSMNS SPRSKKLRLK FRDVKCIPDD DEDSYEIFEP PESTVMATRK MHDRLEPEDE ESDADYDYQN RLAAALGIRS FRNSSLNQEE EEFNLTALAL ENGTEFVSSN TDIIVGSNYS SPSNILGQMP SPSSPTLNDT FLSKEFNPLV IVGLSKDGTD YIEIIPKEEV QSSEDDYAEI DYVPYDDPYK TDVRTNINSS RDPDNIAAWY LRSNNGNRRN YYIAAEEISW DYSEFVQRET DIEDSDDIPE DTTYKKVVFR KYLDSTFTKR DPRGEYEEHL GILGPIIRAE VDDVIQVRFK NLASRPYSLH AHGLSYEKSS EGKTYEDDSP EWFKEDNAVQ PNSSYTYVWH ATERSGPESP GSACRAWAYY SAVNPEKDIH SGLIGPLLIC QKGILHKDSN MPVDMREFVL LFMTFDEKKS WYYEKKSRSS WRLTSSEMKK SHEFHAINGM IYSLPGLKMY EQEWVRLHLL NIGGSQDIHV VHFHGQTLLE NGNKQHQLGV WPLLPGSFKT LEMKASKPGW WLLNTEVGEN QRAGMQTPFL IMDRDCRMPM GLSTGIISDS QIKASEFLGY WEPRLARLNN GGSYNAWSVE KLAAEFASKP WIQVDMQKEV IITGIQTQGA KHYLKSCYTT EFYVAYSSNQ INWQIFKGNS TRNVMYFNGN SDASTIKENQ FDPPIVARYI RISPTRAYNR PTLRLELQGC EVNGCSTPLG MENGKIENKQ ITASSFKKSW WGDYWEPFRA RLNAQGRVNA WQAKANNNKQ WLEIDLLKIK KITAIITQGC KSLSSEMYVK SYTIHYSEQG VEWKPYRLKS SMVDKIFEGN TNTKGHVKNF FNPPIISRFI RVIPKTWNQS ITLRLELFGC DIYEDQVDPR LIDGK |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.1 mg/mL | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.4 構成要素:
| ||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / 装置: FEI VITROBOT MARK IV / 詳細: 2 second blot 20 second wait time. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 特殊光学系 | 球面収差補正装置: Cs corrector |
| 撮影 | フィルム・検出器のモデル: FEI FALCON IV (4k x 4k) 検出モード: COUNTING / デジタル化 - サイズ - 横: 4096 pixel / デジタル化 - サイズ - 縦: 4096 pixel / デジタル化 - 画像ごとのフレーム数: 1-46 / 撮影したグリッド数: 1 / 実像数: 3316 / 平均露光時間: 9.36 sec. / 平均電子線量: 55.09 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 50.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 0.01 mm / 最大 デフォーカス(公称値): 2.4 µm / 最小 デフォーカス(公称値): 1.0 µm / 倍率(公称値): 75000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 精密化 | 空間: REAL / プロトコル: AB INITIO MODEL |
|---|
 ムービー
ムービー コントローラー
コントローラー








 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)