登録情報 データベース : EMDB / ID : EMD-22338タイトル Structure of the Epstein-Barr virus GPCR BILF1 in complex with human Gi 複合体 : BILF1-Gi-scFv16 complex複合体 : Gi heterotrimerタンパク質・ペプチド : Guanine nucleotide-binding protein G(i) subunit alpha-1タンパク質・ペプチド : Guanine nucleotide-binding protein G(I)/G(S)/G(T) subunit beta-1タンパク質・ペプチド : Guanine nucleotide-binding protein G(I)/G(S)/G(O) subunit gamma-2複合体 : scFv16タンパク質・ペプチド : Antibody fragment scFv16複合体 : BILF1リガンド : CHOLESTEROL HEMISUCCINATE / / / 機能・相同性 分子機能 ドメイン・相同性 構成要素
/ / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / 生物種 Homo sapiens (ヒト) / Mus musculus (ハツカネズミ) / / 手法 / / 解像度 : 3.2 Å Tsutsumi N / Qu QH / Skiniotis G / Garcia KC 資金援助 Organization Grant number 国 National Institutes of Health/National Institute Of Allergy and Infectious Diseases (NIH/NIAID) R01AI125320 Howard Hughes Medical Institute (HHMI)
ジャーナル : Immunity / 年 : 2021タイトル : Structural basis for the constitutive activity and immunomodulatory properties of the Epstein-Barr virus-encoded G protein-coupled receptor BILF1.著者 : Naotaka Tsutsumi / Qianhui Qu / Maša Mavri / Maibritt S Baggesen / Shoji Maeda / Deepa Waghray / Christian Berg / Brian K Kobilka / Mette M Rosenkilde / Georgios Skiniotis / K Christopher Garcia / 要旨 : Epstein-Barr virus (EBV) encodes a G protein-coupled receptor (GPCR) termed BILF1 that is essential for EBV-mediated immunosuppression and oncogenesis. BILF1 couples with inhibitory G protein (Gi), ... Epstein-Barr virus (EBV) encodes a G protein-coupled receptor (GPCR) termed BILF1 that is essential for EBV-mediated immunosuppression and oncogenesis. BILF1 couples with inhibitory G protein (Gi), the major intracellular signaling effector for human chemokine receptors, and exhibits constitutive signaling activity; the ligand(s) for BILF1 are unknown. We studied the origins of BILF1's constitutive activity through structure determination of BILF1 bound to the inhibitory G protein (Gi) heterotrimer. The 3.2-Å resolution cryo-electron microscopy structure revealed an extracellular loop within BILF1 that blocked the typical chemokine binding site, suggesting ligand-autonomous receptor activation. Rather, amino acid substitutions within BILF1 transmembrane regions at hallmark ligand-activated class A GPCR "microswitches" stabilized a constitutively active BILF1 conformation for Gi coupling in a ligand-independent fashion. Thus, the constitutive activity of BILF1 promotes immunosuppression and virulence independent of ligand availability, with implications for the function of GPCRs encoded by related viruses and for therapeutic targeting of EBV. 履歴 登録 2020年7月20日 - ヘッダ(付随情報) 公開 2021年7月7日 - マップ公開 2021年7月7日 - 更新 2024年10月30日 - 現状 2024年10月30日 処理サイト : RCSB / 状態 : 公開
すべて表示 表示を減らす
 データを開く
データを開く 基本情報
基本情報 マップデータ
マップデータ 試料
試料 キーワード
キーワード 機能・相同性情報
機能・相同性情報 Homo sapiens (ヒト) /
Homo sapiens (ヒト) / 
 Human gammaherpesvirus 4 (ヘルペスウイルス) /
Human gammaherpesvirus 4 (ヘルペスウイルス) /  Epstein-Barr virus (ヘルペスウイルス)
Epstein-Barr virus (ヘルペスウイルス) データ登録者
データ登録者 米国, 2件
米国, 2件  引用
引用 ジャーナル: Immunity / 年: 2021
ジャーナル: Immunity / 年: 2021


 構造の表示
構造の表示 ムービービューア
ムービービューア SurfView
SurfView Molmil
Molmil Jmol/JSmol
Jmol/JSmol ダウンロードとリンク
ダウンロードとリンク emd_22338.map.gz
emd_22338.map.gz EMDBマップデータ形式
EMDBマップデータ形式 emd-22338-v30.xml
emd-22338-v30.xml emd-22338.xml
emd-22338.xml EMDBヘッダ
EMDBヘッダ emd_22338.png
emd_22338.png emd-22338.cif.gz
emd-22338.cif.gz http://ftp.pdbj.org/pub/emdb/structures/EMD-22338
http://ftp.pdbj.org/pub/emdb/structures/EMD-22338 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-22338
ftp://ftp.pdbj.org/pub/emdb/structures/EMD-22338 emd_22338_validation.pdf.gz
emd_22338_validation.pdf.gz EMDB検証レポート
EMDB検証レポート emd_22338_full_validation.pdf.gz
emd_22338_full_validation.pdf.gz emd_22338_validation.xml.gz
emd_22338_validation.xml.gz emd_22338_validation.cif.gz
emd_22338_validation.cif.gz https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-22338
https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-22338 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-22338
ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-22338 リンク
リンク EMDB (EBI/PDBe) /
EMDB (EBI/PDBe) /  EMDataResource
EMDataResource マップ
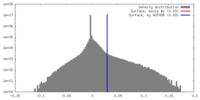
マップ ダウンロード / ファイル: emd_22338.map.gz / 形式: CCP4 / 大きさ: 40.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES)
ダウンロード / ファイル: emd_22338.map.gz / 形式: CCP4 / 大きさ: 40.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) 試料の構成要素
試料の構成要素 解析
解析 試料調製
試料調製 電子顕微鏡法
電子顕微鏡法 FIELD EMISSION GUN
FIELD EMISSION GUN
 画像解析
画像解析
 ムービー
ムービー コントローラー
コントローラー





































 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)




















 Trichoplusia ni (イラクサキンウワバ)
Trichoplusia ni (イラクサキンウワバ)
