+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-21005 | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Negative stain EM map of CODH/ACS in the closed conformation | |||||||||||||||
 マップデータ マップデータ | Negative stain map of CODH/ACS in the closed conformation | |||||||||||||||
 試料 試料 |
| |||||||||||||||
| 生物種 |  Moorella thermoacetica (バクテリア) Moorella thermoacetica (バクテリア) | |||||||||||||||
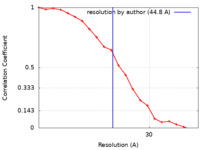
| 手法 | 単粒子再構成法 / ネガティブ染色法 / 解像度: 44.8 Å | |||||||||||||||
 データ登録者 データ登録者 | Cohen SE / Brignole EJ / Drennan CL | |||||||||||||||
| 資金援助 |  米国, 4件 米国, 4件
| |||||||||||||||
 引用 引用 |  ジャーナル: Structure / 年: 2021 ジャーナル: Structure / 年: 2021タイトル: Negative-Stain Electron Microscopy Reveals Dramatic Structural Rearrangements in Ni-Fe-S-Dependent Carbon Monoxide Dehydrogenase/Acetyl-CoA Synthase. 著者: Steven E Cohen / Edward J Brignole / Elizabeth C Wittenborn / Mehmet Can / Samuel Thompson / Stephen W Ragsdale / Catherine L Drennan /  要旨: The Ni-Fe-S-containing A-cluster of acetyl-coenzyme A (CoA) synthase (ACS) assembles acetyl-CoA from carbon monoxide (CO), a methyl group (CH), and CoA. To accomplish this feat, ACS must bind CoA and ...The Ni-Fe-S-containing A-cluster of acetyl-coenzyme A (CoA) synthase (ACS) assembles acetyl-CoA from carbon monoxide (CO), a methyl group (CH), and CoA. To accomplish this feat, ACS must bind CoA and interact with two other proteins that contribute the CO and CH, respectively: CO dehydrogenase (CODH) and corrinoid Fe-S protein (CFeSP). Previous structural data show that, in the model acetogen Moorella thermoacetica, domain 1 of ACS binds to CODH such that a 70-Å-long internal channel is created that allows CO to travel from CODH to the A-cluster. The A-cluster is largely buried and is inaccessible to CFeSP for methylation. Here we use electron microscopy to capture multiple snapshots of ACS that reveal previously uncharacterized domain motion, forming extended and hyperextended structural states. In these structural states, the A-cluster is accessible for methylation by CFeSP. | |||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_21005.map.gz emd_21005.map.gz | 953 KB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-21005-v30.xml emd-21005-v30.xml emd-21005.xml emd-21005.xml | 15.9 KB 15.9 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_21005_fsc.xml emd_21005_fsc.xml | 1.9 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_21005.png emd_21005.png | 29.3 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-21005 http://ftp.pdbj.org/pub/emdb/structures/EMD-21005 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-21005 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-21005 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_21005_validation.pdf.gz emd_21005_validation.pdf.gz | 77.8 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_21005_full_validation.pdf.gz emd_21005_full_validation.pdf.gz | 76.9 KB | 表示 | |
| XML形式データ |  emd_21005_validation.xml.gz emd_21005_validation.xml.gz | 495 B | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-21005 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-21005 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-21005 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-21005 | HTTPS FTP |
-関連構造データ
| 関連構造データ | C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_21005.map.gz / 形式: CCP4 / 大きさ: 1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_21005.map.gz / 形式: CCP4 / 大きさ: 1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Negative stain map of CODH/ACS in the closed conformation | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 7.16 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : carbon monoxide dheydrogenase/acetyl-CoA synthase tetramer
| 全体 | 名称: carbon monoxide dheydrogenase/acetyl-CoA synthase tetramer |
|---|---|
| 要素 |
|
-超分子 #1: carbon monoxide dheydrogenase/acetyl-CoA synthase tetramer
| 超分子 | 名称: carbon monoxide dheydrogenase/acetyl-CoA synthase tetramer タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  Moorella thermoacetica (バクテリア) Moorella thermoacetica (バクテリア) |
-分子 #1: Carbon monoxide dehdyrogenase
| 分子 | 名称: Carbon monoxide dehdyrogenase / タイプ: protein_or_peptide / ID: 1 / 光学異性体: LEVO / EC番号: anaerobic carbon monoxide dehydrogenase |
|---|---|
| 由来(天然) | 生物種:  Moorella thermoacetica (バクテリア) Moorella thermoacetica (バクテリア) |
| 配列 | 文字列: MPRFRDLSHN CRPSEAPRVM EPKNRDRTVD PAVLEMLVKS KDDKVITAFD RFVAQQPQCK IGYEGICCR FCMAGPCRIK ATDGPGSRGI CGASAWTIVA RNVGLMILTG AAAHCEHGNH I AHALVEMA EGKAPDYSVK DEAKLKEVCR RVGIEVEGKS VLELAQEVGE ...文字列: MPRFRDLSHN CRPSEAPRVM EPKNRDRTVD PAVLEMLVKS KDDKVITAFD RFVAQQPQCK IGYEGICCR FCMAGPCRIK ATDGPGSRGI CGASAWTIVA RNVGLMILTG AAAHCEHGNH I AHALVEMA EGKAPDYSVK DEAKLKEVCR RVGIEVEGKS VLELAQEVGE KALEDFRRLK GE GEATWLM TTINEGRKEK FRTHNVVPFG IHASISELVN QAHMGMDNDP VNLVFSAIRV ALA DYTGEH IATDFSDILF GTPQPVVSEA NMGVLDPDQV NFVLHGHNPL LSEIIVQAAR EMEG EAKAA GAKGINLVGI CCTGNEVLMR QGIPLVTSFA SQELAICTGA IDAMCVDVQC IMPSI SAVA ECYHTRIITT ADNAKIPGAY HIDYQTATAI ESAKTAIRMA IEAFKERKES NRPVYI PQI KNRVVAGWSL EALTKLLATQ NAQNPIRVLN QAILDGELAG VALICGCNNL KGFQDNS HL TVMKELLKNN VFVVATGCSA QAAGKLGLLD PANVETYCGD GLKGFLKRLG EGANIEIG L PPVFHMGSCV DNSRAVDLLM AMANDLGVDT PKVPFVASAP EAMSGKAAAI GTWWVSLGV PTHVGTMPPV EGSDLIYSIL TQIASDVYGG YFIFEMDPQV AARKILDALE YRTWKLGVHK EVAERYETK LCQGY |
-分子 #2: Acetyl-CoA synthase
| 分子 | 名称: Acetyl-CoA synthase / タイプ: protein_or_peptide / ID: 2 / 光学異性体: LEVO / EC番号: CO-methylating acetyl-CoA synthase |
|---|---|
| 由来(天然) | 生物種:  Moorella thermoacetica (バクテリア) Moorella thermoacetica (バクテリア) |
| 配列 | 文字列: MTDFDKIFEG AIPEGKEPVA LFREVYHGAI TATSYAEILL NQAIRTYGPD HPVGYPDTAY YLPVIRCFS GEEVKKLGDL PPILNRKRAQ VSPVLNFENA RLAGEATWYA AEIIEALRYL K YKPDEPLL PPPWTGFIGD PVVRRFGIKM VDWTIPGEAI ILGRAKDSKA ...文字列: MTDFDKIFEG AIPEGKEPVA LFREVYHGAI TATSYAEILL NQAIRTYGPD HPVGYPDTAY YLPVIRCFS GEEVKKLGDL PPILNRKRAQ VSPVLNFENA RLAGEATWYA AEIIEALRYL K YKPDEPLL PPPWTGFIGD PVVRRFGIKM VDWTIPGEAI ILGRAKDSKA LAKIVKELMG MG FMLFICD EAVEQLLEEN VKLGIDYIAY PLGNFTQIVH AANYALRAGM MFGGVTPGAR EEQ RDYQRR RIRAFVLYLG EHDMVKTAAA FGAIFTGFPV ITDQPLPEDK QIPDWFFSVE DYDK IVQIA METRGIKLTK IKLDLPINFG PAFEGESIRK GDMYVEMGGN RTPAFELVRT VSESE ITDG KIEVIGPDID QIPEGSKLPL GILVDIYGRK MQADFEGVLE RRIHDFINYG EGLWHT GQR NINWLRVSKD AVAKGFRFKN YGEILVAKMK EEFPAIVDRV QVTIFTDEAK VKEYMEV AR EKYKERDDRM RGLTDETVDT FYSCVLCQSF APNHVCIVTP ERVGLCGAVS WLDAKASY E INHAGPNQPI PKEGEIDPIK GIWKSVNDYL YTASNRNLEQ VCLYTLMENP MTSCGCFEA IMAILPECNG IMITTRDHAG MTPSGMTFST LAGMIGGGTQ TPGFMGIGRT YIVSKKFISA DGGIARIVW MPKSLKDFLH DEFVRRSVEE GLGEDFIDKI ADETIGTTVD EILPYLEEKG H PALTMDPI M |
-実験情報
-構造解析
| 手法 | ネガティブ染色法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | .017 mg/mL | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.6 構成要素:
| |||||||||
| 染色 | タイプ: NEGATIVE / 材質: uranyl acetate 詳細: Samples were prepared by blotting protein from EM grid using filter paper, followed by multiple rounds of staining and blotting. | |||||||||
| グリッド | 材質: COPPER / メッシュ: 300 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: CONTINUOUS / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 雰囲気: AIR / 前処理 - 気圧: 0.038 kPa / 詳細: -15 mA for 60 seconds | |||||||||
| 詳細 | The sample was predominantly monodisperse, as seen by negative-stain TEM. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TECNAI F20 |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN ULTRASCAN 4000 (4k x 4k) 撮影したグリッド数: 1 / 平均露光時間: 1.0 sec. / 平均電子線量: 23.0 e/Å2 詳細: Images were collected as tilt pairs at 0 and 55 degrees. |
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.0 mm / 倍率(公称値): 62000 |
| 実験機器 |  モデル: Tecnai F20 / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー













 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)