+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-20781 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Structural basis for control of antibiotic production by bacterial hormones | |||||||||
 マップデータ マップデータ | Map file - Postprocess masked .mrc UCSF Chimera 1.11, visualization -Volume viewer step 1 -Contour level 0.0181 | |||||||||
 試料 試料 |
| |||||||||
| 生物種 |  Streptomyces coelicolor A3(2) (バクテリア) Streptomyces coelicolor A3(2) (バクテリア) | |||||||||
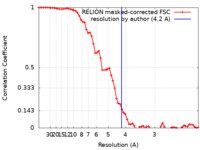
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 4.2 Å | |||||||||
 データ登録者 データ登録者 | Bhukya H | |||||||||
| 資金援助 |  英国, 2件 英国, 2件
| |||||||||
 引用 引用 |  ジャーナル: Nature / 年: 2021 ジャーナル: Nature / 年: 2021タイトル: Molecular basis for control of antibiotic production by a bacterial hormone. 著者: Shanshan Zhou / Hussain Bhukya / Nicolas Malet / Peter J Harrison / Dean Rea / Matthew J Belousoff / Hariprasad Venugopal / Paulina K Sydor / Kathryn M Styles / Lijiang Song / Max J Cryle / ...著者: Shanshan Zhou / Hussain Bhukya / Nicolas Malet / Peter J Harrison / Dean Rea / Matthew J Belousoff / Hariprasad Venugopal / Paulina K Sydor / Kathryn M Styles / Lijiang Song / Max J Cryle / Lona M Alkhalaf / Vilmos Fülöp / Gregory L Challis / Christophe Corre /   要旨: Actinobacteria produce numerous antibiotics and other specialized metabolites that have important applications in medicine and agriculture. Diffusible hormones frequently control the production of ...Actinobacteria produce numerous antibiotics and other specialized metabolites that have important applications in medicine and agriculture. Diffusible hormones frequently control the production of such metabolites by binding TetR family transcriptional repressors (TFTRs), but the molecular basis for this remains unclear. The production of methylenomycin antibiotics in Streptomyces coelicolor A3(2) is initiated by the binding of 2-alkyl-4-hydroxymethylfuran-3-carboxylic acid (AHFCA) hormones to the TFTR MmfR. Here we report the X-ray crystal structure of an MmfR-AHFCA complex, establishing the structural basis for hormone recognition. We also elucidate the mechanism for DNA release upon hormone binding through the single-particle cryo-electron microscopy structure of an MmfR-operator complex. DNA binding and release assays with MmfR mutants and synthetic AHFCA analogues define the role of individual amino acid residues and hormone functional groups in ligand recognition and DNA release. These findings will facilitate the exploitation of actinobacterial hormones and their associated TFTRs in synthetic biology and in the discovery of new antibiotics. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_20781.map.gz emd_20781.map.gz | 3.1 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-20781-v30.xml emd-20781-v30.xml emd-20781.xml emd-20781.xml | 18.3 KB 18.3 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_20781_fsc.xml emd_20781_fsc.xml | 6.5 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_20781.png emd_20781.png | 50 KB | ||
| マスクデータ |  emd_20781_msk_1.map emd_20781_msk_1.map | 22.2 MB |  マスクマップ マスクマップ | |
| その他 |  emd_20781_half_map_1.map.gz emd_20781_half_map_1.map.gz emd_20781_half_map_2.map.gz emd_20781_half_map_2.map.gz | 17.1 MB 17.1 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-20781 http://ftp.pdbj.org/pub/emdb/structures/EMD-20781 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-20781 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-20781 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_20781_validation.pdf.gz emd_20781_validation.pdf.gz | 429 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_20781_full_validation.pdf.gz emd_20781_full_validation.pdf.gz | 428.6 KB | 表示 | |
| XML形式データ |  emd_20781_validation.xml.gz emd_20781_validation.xml.gz | 12.1 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-20781 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-20781 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-20781 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-20781 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_20781.map.gz / 形式: CCP4 / 大きさ: 22.2 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_20781.map.gz / 形式: CCP4 / 大きさ: 22.2 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Map file - Postprocess masked .mrc UCSF Chimera 1.11, visualization -Volume viewer step 1 -Contour level 0.0181 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
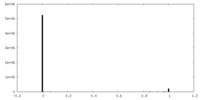
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.092 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-マスク #1
| ファイル |  emd_20781_msk_1.map emd_20781_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
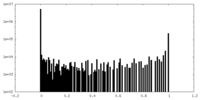
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: Half map file - run half1 class001 unfil.mrc UCSF Chimera 1.11,...
| ファイル | emd_20781_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half map file - run_half1_class001_unfil.mrc UCSF Chimera 1.11, visualization -Volume viewer step 1 -Contour level 0.017 | ||||||||||||
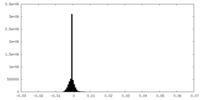
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: Half map file - run half2 class001 unfil.mrc UCSF Chimera 1.11,...
| ファイル | emd_20781_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half map file - run_half2_class001_unfil.mrc UCSF Chimera 1.11, visualization -Volume viewer step 1 -Contour level 0.017 | ||||||||||||
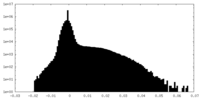
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : protein-DNA complex
| 全体 | 名称: protein-DNA complex |
|---|---|
| 要素 |
|
-超分子 #1: protein-DNA complex
| 超分子 | 名称: protein-DNA complex / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all 詳細: protein-DNA complex. two homodimers of protein bound to a double stranded DNA |
|---|---|
| 由来(天然) | 生物種:  Streptomyces coelicolor A3(2) (バクテリア) Streptomyces coelicolor A3(2) (バクテリア) |
| 組換発現 | 生物種:  |
| 分子量 | 実験値: 114 KDa |
-分子 #1: protein MmfR
| 分子 | 名称: protein MmfR / タイプ: protein_or_peptide / ID: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Streptomyces coelicolor A3(2) (バクテリア) / 株: A3(2) Streptomyces coelicolor A3(2) (バクテリア) / 株: A3(2) |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MHHHHHHGKP IPNPLLGLDS TENLYFQGID PFTMTSAQQP TPFAVRSNVP RGPHPQQERS IKTRAQILEA ASEIFASRGY RGASVKDVAE RVGMTKGAVY FHFPSKESLA IAVVEEHYAR WPAAMEEIRI QGFTPLETVE EMLHRAAQAF RDDPVMQAGA RLQSERAFID ...文字列: MHHHHHHGKP IPNPLLGLDS TENLYFQGID PFTMTSAQQP TPFAVRSNVP RGPHPQQERS IKTRAQILEA ASEIFASRGY RGASVKDVAE RVGMTKGAVY FHFPSKESLA IAVVEEHYAR WPAAMEEIRI QGFTPLETVE EMLHRAAQAF RDDPVMQAGA RLQSERAFID AELPLPYVDW THLLEVPLQD AREAGQLRAG VDPAAAARSL VAAFFGMQHV SDNLHQRADI MERWQELREL MFFALRA |
-分子 #2: synthetic DNA
| 分子 | 名称: synthetic DNA / タイプ: dna / ID: 2 / 詳細: 5'-ATACCTGCGGGAAGGTATT-3' / 分類: DNA |
|---|---|
| 由来(天然) | 生物種:  Streptomyces coelicolor A3(2) (バクテリア) Streptomyces coelicolor A3(2) (バクテリア) |
| 配列 | 文字列: ATACCTGCGG GAAGGTATT |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.08 mg/mL | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 8 構成要素:
詳細: 20 mM tris pH 8.0 and 200 mM NaCl fresh and autoclaved | |||||||||
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: COPPER | |||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK III | |||||||||
| 詳細 | protein-DNA complex |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 特殊光学系 | 位相板: VOLTA PHASE PLATE / エネルギーフィルター - スリット幅: 20 eV |
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: COUNTING / デジタル化 - 画像ごとのフレーム数: 1-50 / 撮影したグリッド数: 2 / 平均露光時間: 10.0 sec. / 平均電子線量: 50.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 50.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最小 デフォーカス(公称値): -0.0005 µm / 倍率(公称値): 165000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 精密化 | プロトコル: FLEXIBLE FIT / 温度因子: 214 |
|---|
 ムービー
ムービー コントローラー
コントローラー













 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)