+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-2015 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
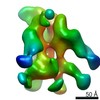
| タイトル | CryoEM map of the p97-Ufd1-Npl4 complex in the two-binding-sites conformation | |||||||||
 マップデータ マップデータ | p97-Ufd1-Npl4 complex in the two-binding-sites conformation | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | p97 / Ufd1-Npl4 / asymmetric complex / ATPase | |||||||||
| 生物種 |   | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 25.0 Å | |||||||||
 データ登録者 データ登録者 | Bebeacua C / Forster A / McKeown C / Meyer HH / Zhang X / Freemont PS | |||||||||
 引用 引用 |  ジャーナル: Proc Natl Acad Sci U S A / 年: 2012 ジャーナル: Proc Natl Acad Sci U S A / 年: 2012タイトル: Distinct conformations of the protein complex p97-Ufd1-Npl4 revealed by electron cryomicroscopy. 著者: Cecilia Bebeacua / Andreas Förster / Ciarán McKeown / Hemmo H Meyer / Xiaodong Zhang / Paul S Freemont /  要旨: p97 is a key regulator of numerous cellular pathways and associates with ubiquitin-binding adaptors to remodel ubiquitin-modified substrate proteins. How adaptor binding to p97 is coordinated and how ...p97 is a key regulator of numerous cellular pathways and associates with ubiquitin-binding adaptors to remodel ubiquitin-modified substrate proteins. How adaptor binding to p97 is coordinated and how adaptors contribute to substrate remodeling is unclear. Here we present the 3D electron cryomicroscopy reconstructions of the major Ufd1-Npl4 adaptor in complex with p97. Our reconstructions show that p97-Ufd1-Npl4 is highly dynamic and that Ufd1-Npl4 assumes distinct positions relative to the p97 ring upon addition of nucleotide. Our results suggest a model for substrate remodeling by p97 and also explains how p97-Ufd1-Npl4 could form other complexes in a hierarchical model of p97-cofactor assembly. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_2015.map.gz emd_2015.map.gz | 699.1 KB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-2015-v30.xml emd-2015-v30.xml emd-2015.xml emd-2015.xml | 11.2 KB 11.2 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd2015fig.png emd2015fig.png | 113.7 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-2015 http://ftp.pdbj.org/pub/emdb/structures/EMD-2015 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-2015 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-2015 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_2015_validation.pdf.gz emd_2015_validation.pdf.gz | 191.3 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_2015_full_validation.pdf.gz emd_2015_full_validation.pdf.gz | 190.5 KB | 表示 | |
| XML形式データ |  emd_2015_validation.xml.gz emd_2015_validation.xml.gz | 5.6 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-2015 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-2015 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-2015 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-2015 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_2015.map.gz / 形式: CCP4 / 大きさ: 7.8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_2015.map.gz / 形式: CCP4 / 大きさ: 7.8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | p97-Ufd1-Npl4 complex in the two-binding-sites conformation | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 3.53 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : p97-Ufd1-Npl4
| 全体 | 名称: p97-Ufd1-Npl4 |
|---|---|
| 要素 |
|
-超分子 #1000: p97-Ufd1-Npl4
| 超分子 | 名称: p97-Ufd1-Npl4 / タイプ: sample / ID: 1000 集合状態: One hexamer of p97 binds to one Ufd1-Npl4 dimer Number unique components: 3 |
|---|---|
| 分子量 | 実験値: 623 KDa / 理論値: 623 KDa |
-分子 #1: p97
| 分子 | 名称: p97 / タイプ: protein_or_peptide / ID: 1 / Name.synonym: p97 / 詳細: This corresponds to the p97-Ufd1-Npl4 complex / コピー数: 1 / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  |
| 組換発現 | 生物種:  |
-分子 #2: Ufd1
| 分子 | 名称: Ufd1 / タイプ: protein_or_peptide / ID: 2 / Name.synonym: Ufd1 / 詳細: This corresponds to the p97-Ufd1-Npl4 complex / コピー数: 1 / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  |
| 組換発現 | 生物種:  |
-分子 #3: Npl4
| 分子 | 名称: Npl4 / タイプ: protein_or_peptide / ID: 3 / Name.synonym: Npl4 / 詳細: This corresponds to the p97-Ufd1-Npl4 complex / コピー数: 1 / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  |
| 組換発現 | 生物種:  |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.5 mg/mL |
|---|---|
| 緩衝液 | pH: 8 / 詳細: 150 mM KCL, 25 mL Tris, 2.5 mM MgCl2 |
| グリッド | 詳細: 200 mesh copper grid |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / 装置: OTHER / 詳細: Vitrification instrument: Vitrobot / 手法: Blot for 2 seconds before plunging |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI/PHILIPS CM200FEG |
|---|---|
| アライメント法 | Legacy - 非点収差: Objective lens astigmatism was corrected at 100,000 times magnification |
| 特殊光学系 | エネルギーフィルター - 名称: FEI |
| 日付 | 2009年7月1日 |
| 撮影 | カテゴリ: CCD / フィルム・検出器のモデル: GENERIC CCD / 実像数: 100 / 平均電子線量: 10 e/Å2 |
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 倍率(補正後): 50000 / 照射モード: OTHER / 撮影モード: BRIGHT FIELD / Cs: 2.2 mm / 最大 デフォーカス(公称値): 3.0 µm / 最小 デフォーカス(公称値): 1.5 µm / 倍率(公称値): 50000 |
| 試料ステージ | 試料ホルダー: Eucentric / 試料ホルダーモデル: GATAN LIQUID NITROGEN |
- 画像解析
画像解析
| 最終 再構成 | 想定した対称性 - 点群: C1 (非対称) / アルゴリズム: OTHER / 解像度のタイプ: BY AUTHOR / 解像度: 25.0 Å / 解像度の算出法: OTHER / ソフトウェア - 名称: IMAGIC / 使用した粒子像数: 5000 |
|---|
-原子モデル構築 1
| 初期モデル | PDB ID: |
|---|---|
| ソフトウェア | 名称:  Chimera Chimera |
| 詳細 | Protocol: Rigid Body. The protomers were fitted individually and the N-domains fitted by manual docking and refined automatically |
| 精密化 | 空間: REAL / プロトコル: RIGID BODY FIT / 当てはまり具合の基準: Cross Correlation |
 ムービー
ムービー コントローラー
コントローラー