+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Wait Complex: BAM bound Darobactin-B and Extended SurA | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Outer Membrane / Complex / Chaperone / Protein Folding / Inhibitor / MEMBRANE PROTEIN | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報Bam protein complex / Gram-negative-bacterium-type cell outer membrane assembly / protein insertion into membrane / peptide binding / peptidyl-prolyl cis-trans isomerase activity / peptidylprolyl isomerase / cell outer membrane / unfolded protein binding / protein folding / outer membrane-bounded periplasmic space ...Bam protein complex / Gram-negative-bacterium-type cell outer membrane assembly / protein insertion into membrane / peptide binding / peptidyl-prolyl cis-trans isomerase activity / peptidylprolyl isomerase / cell outer membrane / unfolded protein binding / protein folding / outer membrane-bounded periplasmic space / protein-macromolecule adaptor activity / protein stabilization / response to antibiotic / cell surface / identical protein binding / membrane 類似検索 - 分子機能 | |||||||||
| 生物種 |   Photorhabdus heterorhabditis (バクテリア) Photorhabdus heterorhabditis (バクテリア) | |||||||||
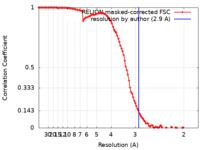
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.9 Å | |||||||||
 データ登録者 データ登録者 | Fenn KL / Ranson NA | |||||||||
| 資金援助 |  英国, 1件 英国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2024 ジャーナル: Nat Commun / 年: 2024タイトル: Outer membrane protein assembly mediated by BAM-SurA complexes. 著者: Katherine L Fenn / Jim E Horne / Joel A Crossley / Nils Böhringer / Romany J Horne / Till F Schäberle / Antonio N Calabrese / Sheena E Radford / Neil A Ranson /   要旨: The outer membrane is a formidable barrier that protects Gram-negative bacteria against environmental threats. Its integrity requires the correct folding and insertion of outer membrane proteins ...The outer membrane is a formidable barrier that protects Gram-negative bacteria against environmental threats. Its integrity requires the correct folding and insertion of outer membrane proteins (OMPs) by the membrane-embedded β-barrel assembly machinery (BAM). Unfolded OMPs are delivered to BAM by the periplasmic chaperone SurA, but how SurA and BAM work together to ensure successful OMP delivery and folding remains unclear. Here, guided by AlphaFold2 models, we use disulphide bond engineering in an attempt to trap SurA in the act of OMP delivery to BAM, and solve cryoEM structures of a series of complexes. The results suggest that SurA binds BAM at its soluble POTRA-1 domain, which may trigger conformational changes in both BAM and SurA that enable transfer of the unfolded OMP to the BAM lateral gate for insertion into the outer membrane. Mutations that disrupt the interaction between BAM and SurA result in outer membrane assembly defects, supporting the key role of SurA in outer membrane biogenesis. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_18046.map.gz emd_18046.map.gz | 7.8 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-18046-v30.xml emd-18046-v30.xml emd-18046.xml emd-18046.xml | 26.6 KB 26.6 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_18046_fsc.xml emd_18046_fsc.xml | 10.7 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_18046.png emd_18046.png | 137.2 KB | ||
| Filedesc metadata |  emd-18046.cif.gz emd-18046.cif.gz | 9.6 KB | ||
| その他 |  emd_18046_half_map_1.map.gz emd_18046_half_map_1.map.gz emd_18046_half_map_2.map.gz emd_18046_half_map_2.map.gz | 80.8 MB 80.8 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-18046 http://ftp.pdbj.org/pub/emdb/structures/EMD-18046 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-18046 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-18046 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_18046_validation.pdf.gz emd_18046_validation.pdf.gz | 788.6 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_18046_full_validation.pdf.gz emd_18046_full_validation.pdf.gz | 788.1 KB | 表示 | |
| XML形式データ |  emd_18046_validation.xml.gz emd_18046_validation.xml.gz | 17.8 KB | 表示 | |
| CIF形式データ |  emd_18046_validation.cif.gz emd_18046_validation.cif.gz | 23.5 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-18046 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-18046 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-18046 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-18046 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8pzvMC  8pz1C  8pz2C  8pzuC  8q0gC  8qp5C  8qpuC  8qpvC  8qpwC C: 同じ文献を引用 ( M: このマップから作成された原子モデル |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_18046.map.gz / 形式: CCP4 / 大きさ: 103 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_18046.map.gz / 形式: CCP4 / 大きさ: 103 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.91 Å | ||||||||||||||||||||||||||||||||||||
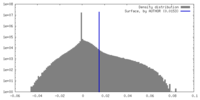
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: #2
| ファイル | emd_18046_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
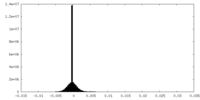
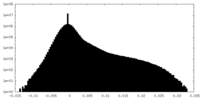
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_18046_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
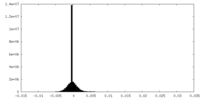
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
+全体 : Wait Complex: BAM bound Darobactin-B and Extended SurA
+超分子 #1: Wait Complex: BAM bound Darobactin-B and Extended SurA
+分子 #1: Outer membrane protein assembly factor BamA
+分子 #2: Outer membrane protein assembly factor BamB
+分子 #3: Outer membrane protein assembly factor BamC
+分子 #4: Outer membrane protein assembly factor BamD
+分子 #5: Outer membrane protein assembly factor BamE
+分子 #6: Chaperone SurA
+分子 #7: Darobactin-B
+分子 #8: MAGNESIUM ION
+分子 #9: water
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 3 mg/mL |
|---|---|
| 緩衝液 | pH: 8 |
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: COPPER / メッシュ: 300 / 前処理 - タイプ: PLASMA CLEANING / 前処理 - 時間: 60 sec. |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 90 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 特殊光学系 | エネルギーフィルター - 名称: TFS Selectris / エネルギーフィルター - スリット幅: 10 eV |
| ソフトウェア | 名称: EPU |
| 撮影 | フィルム・検出器のモデル: FEI FALCON IV (4k x 4k) 撮影したグリッド数: 1 / 実像数: 6357 / 平均電子線量: 39.8 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 3.0 µm / 最小 デフォーカス(公称値): 0.9 µm / 倍率(公称値): 130000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 初期モデル |
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| ソフトウェア | 名称: UCSF ChimeraX | ||||||||
| 精密化 | 空間: REAL / プロトコル: RIGID BODY FIT / 温度因子: 82 | ||||||||
| 得られたモデル |  PDB-8pzv: |
 ムービー
ムービー コントローラー
コントローラー



















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)