+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-10649 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of the prefusion state of canine distemper virus fusion protein ectodomain | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | fusion protein / prefusion state / VIRAL PROTEIN | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報fusion of virus membrane with host plasma membrane / viral envelope / symbiont entry into host cell / host cell plasma membrane / virion membrane / membrane / plasma membrane 類似検索 - 分子機能 | |||||||||
| 生物種 |  Canine morbillivirus (ウイルス) Canine morbillivirus (ウイルス) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 4.3 Å | |||||||||
 データ登録者 データ登録者 | Kalbermatter D / Fotiadis D | |||||||||
| 資金援助 |  スイス, 1件 スイス, 1件
| |||||||||
 引用 引用 |  ジャーナル: J Struct Biol X / 年: 2020 ジャーナル: J Struct Biol X / 年: 2020タイトル: Cryo-EM structure of the prefusion state of canine distemper virus fusion protein ectodomain. 著者: David Kalbermatter / Neeta Shrestha / Flavio M Gall / Marianne Wyss / Rainer Riedl / Philippe Plattet / Dimitrios Fotiadis /  要旨: Measles virus (MeV) and canine distemper virus (CDV), two members of the genus, are still causing important global diseases of humans and animals, respectively. To enter target cells, ...Measles virus (MeV) and canine distemper virus (CDV), two members of the genus, are still causing important global diseases of humans and animals, respectively. To enter target cells, morbilliviruses rely on an envelope-anchored machinery, which is composed of two interacting glycoproteins: a tetrameric receptor binding (H) protein and a trimeric fusion (F) protein. To execute membrane fusion, the F protein initially adopts a metastable, prefusion state that refolds into a highly stable postfusion conformation as the result of a finely coordinated activation process mediated by the H protein. Here, we employed cryo-electron microscopy (cryo-EM) and single particle reconstruction to elucidate the structure of the prefusion state of the CDV F protein ectodomain (solF) at 4.3 Å resolution. Stabilization of the prefusion solF trimer was achieved by fusing the GCNt trimerization sequence at the C-terminal protein region, and expressing and purifying the recombinant protein in the presence of a morbilliviral fusion inhibitor class compound. The three-dimensional cryo-EM map of prefusion CDV solF in complex with the inhibitor clearly shows density for the ligand at the protein binding site suggesting common mechanisms of membrane fusion activation and inhibition employed by different morbillivirus members. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_10649.map.gz emd_10649.map.gz | 2.3 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-10649-v30.xml emd-10649-v30.xml emd-10649.xml emd-10649.xml | 19.3 KB 19.3 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
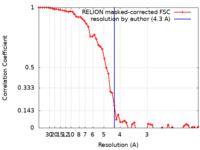
| FSC (解像度算出) |  emd_10649_fsc.xml emd_10649_fsc.xml | 5.8 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_10649.png emd_10649.png | 184.7 KB | ||
| Filedesc metadata |  emd-10649.cif.gz emd-10649.cif.gz | 6.1 KB | ||
| その他 |  emd_10649_half_map_1.map.gz emd_10649_half_map_1.map.gz emd_10649_half_map_2.map.gz emd_10649_half_map_2.map.gz | 11.9 MB 11.9 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-10649 http://ftp.pdbj.org/pub/emdb/structures/EMD-10649 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-10649 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-10649 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_10649_validation.pdf.gz emd_10649_validation.pdf.gz | 743.5 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_10649_full_validation.pdf.gz emd_10649_full_validation.pdf.gz | 743 KB | 表示 | |
| XML形式データ |  emd_10649_validation.xml.gz emd_10649_validation.xml.gz | 11.4 KB | 表示 | |
| CIF形式データ |  emd_10649_validation.cif.gz emd_10649_validation.cif.gz | 15.7 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-10649 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-10649 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-10649 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-10649 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  6xyeMC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | |
| 電子顕微鏡画像生データ |  EMPIAR-10366 (タイトル: Cryo-EM structure of the prefusion state of canine distemper virus fusion protein ectodomain EMPIAR-10366 (タイトル: Cryo-EM structure of the prefusion state of canine distemper virus fusion protein ectodomainData size: 474.1 Data #1: Unaligned multi-frame micrographs of the prefusion state of canine distemper virus fusion protein ectodomain. [micrographs - multiframe]) |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_10649.map.gz / 形式: CCP4 / 大きさ: 15.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_10649.map.gz / 形式: CCP4 / 大きさ: 15.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
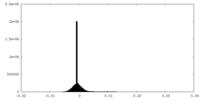
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.021 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-ハーフマップ: half map 1
| ファイル | emd_10649_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | half map 1 | ||||||||||||
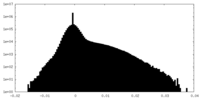
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: half map 2
| ファイル | emd_10649_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | half map 2 | ||||||||||||
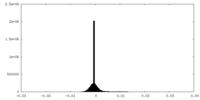
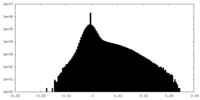
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Canine distemper virus fusion protein
| 全体 | 名称: Canine distemper virus fusion protein |
|---|---|
| 要素 |
|
-超分子 #1: Canine distemper virus fusion protein
| 超分子 | 名称: Canine distemper virus fusion protein / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  Canine morbillivirus (ウイルス) Canine morbillivirus (ウイルス) |
-分子 #1: Fusion glycoprotein F2
| 分子 | 名称: Fusion glycoprotein F2 / タイプ: protein_or_peptide / ID: 1 / コピー数: 3 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Canine morbillivirus (ウイルス) Canine morbillivirus (ウイルス) |
| 分子量 | 理論値: 10.128781 KDa |
| 組換発現 | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 配列 | 文字列: QIHWNNLSTI GIIGTDSVHY KIMTRPSHQY LVIKLMPNVS LIDNCTKAEL GEYEKLLNSV LEPINQALTL MTKNVKPLQS VGSGRRQRR UniProtKB: Fusion glycoprotein F0 |
-分子 #2: Fusion glycoprotein F1
| 分子 | 名称: Fusion glycoprotein F1 / タイプ: protein_or_peptide / ID: 2 / コピー数: 3 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Canine morbillivirus (ウイルス) Canine morbillivirus (ウイルス) |
| 分子量 | 理論値: 47.511637 KDa |
| 組換発現 | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 配列 | 文字列: FAGVVLAGAA LGVATAAQIT AGIALHQSNL NAQAIQSLRT SLEQSNKAIE EIREATQETV IAVQGVQDYV NNELVPAMQH MSCELVGQR LGLKLLRYYT ELLSIFGPSL RDPISAEISI QALSYALGGE IHKILEKLGY SGNDMIAILE SRGIKTKITH V DLPGKLII ...文字列: FAGVVLAGAA LGVATAAQIT AGIALHQSNL NAQAIQSLRT SLEQSNKAIE EIREATQETV IAVQGVQDYV NNELVPAMQH MSCELVGQR LGLKLLRYYT ELLSIFGPSL RDPISAEISI QALSYALGGE IHKILEKLGY SGNDMIAILE SRGIKTKITH V DLPGKLII LSISYPTLSE VKGVIVHRLE AVSYNIGSQE WYTTVPRYVA TNGYLISNFD ESPCVFVSES AICSQNSLYP MS PLLQQCI RGDTSSCART LVSGTMGNKF ILSKGNIVAN CASILCKCYS TGTIINQSPD KLLTFIASDT CPLVEIDGVT IQV GGRQYP DMVYESKVAL GPAISLERLD VGTNLGNALK KLDDAKVLID SSNQILETVR RSSFNFGSLL SVPILICTAL ALLL LIYCC KRRYQQTLKQ NAKVDPTFKP DLTGTSKSYV RSL UniProtKB: Fusion glycoprotein F0 |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.23 mg/mL | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.5 構成要素:
| |||||||||||||||
| グリッド | モデル: Quantifoil R2/1 / 材質: COPPER / メッシュ: 200 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 120 sec. / 前処理 - 雰囲気: AIR / 前処理 - 気圧: 0.025 kPa | |||||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277.15 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI POLARA 300 |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: COUNTING / 撮影したグリッド数: 1 / 実像数: 1604 / 平均電子線量: 73.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD |
| 試料ステージ | ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Tecnai Polara / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 初期モデル |
| ||||||
|---|---|---|---|---|---|---|---|
| 精密化 | 空間: REAL / プロトコル: RIGID BODY FIT | ||||||
| 得られたモデル |  PDB-6xye: |
 ムービー
ムービー コントローラー
コントローラー













 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)