+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-0169 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Mature CA domain hexamer from HIV-1 CA-SP1 Gag proteolytic cleavage mutant virus particles | |||||||||
 マップデータ マップデータ | Structure of the mature CA domain hexamer from HIV-1 CA-SP1 Gag proteolytic cleavage mutant virus particles | |||||||||
 試料 試料 |
| |||||||||
| 生物種 |  Homo sapiens (ヒト) / Homo sapiens (ヒト) /   Human immunodeficiency virus 1 (ヒト免疫不全ウイルス) Human immunodeficiency virus 1 (ヒト免疫不全ウイルス) | |||||||||
| 手法 | サブトモグラム平均法 / クライオ電子顕微鏡法 / 解像度: 7.9 Å | |||||||||
 データ登録者 データ登録者 | Mattei S / Tan AWK / Glass B / Mueller B / Kraeusslich HG / Briggs JAG | |||||||||
 引用 引用 |  ジャーナル: Proc Natl Acad Sci U S A / 年: 2018 ジャーナル: Proc Natl Acad Sci U S A / 年: 2018タイトル: High-resolution structures of HIV-1 Gag cleavage mutants determine structural switch for virus maturation. 著者: Simone Mattei / Aaron Tan / Bärbel Glass / Barbara Müller / Hans-Georg Kräusslich / John A G Briggs /    要旨: HIV-1 maturation occurs via multiple proteolytic cleavages of the Gag polyprotein, causing rearrangement of the virus particle required for infectivity. Cleavage results in beta-hairpin formation at ...HIV-1 maturation occurs via multiple proteolytic cleavages of the Gag polyprotein, causing rearrangement of the virus particle required for infectivity. Cleavage results in beta-hairpin formation at the N terminus of the CA (capsid) protein and loss of a six-helix bundle formed by the C terminus of CA and the neighboring SP1 peptide. How individual cleavages contribute to changes in protein structure and interactions, and how the mature, conical capsid forms, are poorly understood. Here, we employed cryoelectron tomography to determine morphology and high-resolution CA lattice structures for HIV-1 derivatives in which Gag cleavage sites are mutated. These analyses prompt us to revise current models for the crucial maturation switch. Unlike previously proposed, cleavage on either terminus of CA was sufficient, in principle, for lattice maturation, while complete processing was needed for conical capsid formation. We conclude that destabilization of the six-helix bundle, rather than beta-hairpin formation, represents the main determinant of structural maturation. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_0169.map.gz emd_0169.map.gz | 59.6 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-0169-v30.xml emd-0169-v30.xml emd-0169.xml emd-0169.xml | 14 KB 14 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_0169.png emd_0169.png | 127.4 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-0169 http://ftp.pdbj.org/pub/emdb/structures/EMD-0169 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-0169 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-0169 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_0169_validation.pdf.gz emd_0169_validation.pdf.gz | 307.6 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_0169_full_validation.pdf.gz emd_0169_full_validation.pdf.gz | 306.8 KB | 表示 | |
| XML形式データ |  emd_0169_validation.xml.gz emd_0169_validation.xml.gz | 6.2 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0169 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0169 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0169 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0169 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_0169.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_0169.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Structure of the mature CA domain hexamer from HIV-1 CA-SP1 Gag proteolytic cleavage mutant virus particles | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.35 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
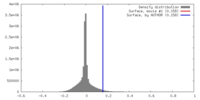
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Human immunodeficiency virus 1
| 全体 | 名称:   Human immunodeficiency virus 1 (ヒト免疫不全ウイルス) Human immunodeficiency virus 1 (ヒト免疫不全ウイルス) |
|---|---|
| 要素 |
|
-超分子 #1: Human immunodeficiency virus 1
| 超分子 | 名称: Human immunodeficiency virus 1 / タイプ: virus / ID: 1 / 親要素: 0 / 含まれる分子: all / NCBI-ID: 11676 / 生物種: Human immunodeficiency virus 1 / ウイルスタイプ: VIRION / ウイルス・単離状態: STRAIN / ウイルス・エンベロープ: Yes / ウイルス・中空状態: No |
|---|---|
| 宿主 | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| Host system | 生物種:  Homo sapiens (ヒト) / 組換細胞: HEK293T / 組換プラスミド: pCHIV Homo sapiens (ヒト) / 組換細胞: HEK293T / 組換プラスミド: pCHIV |
-分子 #1: Gag polyprotein
| 分子 | 名称: Gag polyprotein / タイプ: protein_or_peptide / ID: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 配列 | 文字列: MGARASVLSG GELDRWEKIR LRPGGKKKYK LKHIVWASRE LERFAVNPGL LETSEGCRQI LGQLQPSLQ TGSEELRSLY NTVATLYCVH QRIEIKDTKE ALDKIEEEQN KSKKKAQQAA A DTGHSNQV SQNYPIVQNI QGQMVHQAIS PRTLNAWVKV VEEKAFSPEV ...文字列: MGARASVLSG GELDRWEKIR LRPGGKKKYK LKHIVWASRE LERFAVNPGL LETSEGCRQI LGQLQPSLQ TGSEELRSLY NTVATLYCVH QRIEIKDTKE ALDKIEEEQN KSKKKAQQAA A DTGHSNQV SQNYPIVQNI QGQMVHQAIS PRTLNAWVKV VEEKAFSPEV IPMFSALSEG AT PQDLNTM LNTVGGHQAA MQMLKETINE EAAEWDRVHP VHAGPIAPGQ MREPRGSDIA GTT STLQEQ IGWMTNNPPI PVGEIYKRWI ILGLNKIVRM YSPTSILDIR QGPKEPFRDY VDRF YKTLR AEQASQEVKN WMTETLLVQN ANPDCKTILK ALGPAATLEE MMTACQGVGG PGHKA RVIA EAISQVTNSA TIMMQRGNFR NQRKIVKCFN CGKEGHTARN CRAPRKKGCW KCGKEG HQM KDCTERQANF LGKIWPSYKG RPGNFLQSRP EPTAPPEESF RSGVETTTPP QKQEPID KE LYPLTSLRSL FGNDPSSQ |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | サブトモグラム平均法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.4 |
|---|---|
| グリッド | モデル: C-flat-2/2 / 材質: COPPER / メッシュ: 300 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 雰囲気: AIR 詳細: The grid was glow discharged with a current of 20 mA |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 288.15 K / 装置: FEI VITROBOT MARK II |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 特殊光学系 | エネルギーフィルター - 名称: GIF Quantum LS / エネルギーフィルター - スリット幅: 20 eV |
| 撮影 | フィルム・検出器のモデル: GATAN K2 QUANTUM (4k x 4k) 検出モード: SUPER-RESOLUTION / デジタル化 - 画像ごとのフレーム数: 1-5 / 平均電子線量: 2.4 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 70.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 4.0 µm / 最小 デフォーカス(公称値): 2.0 µm |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー



















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)