+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 8cr2 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
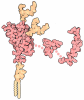
| タイトル | Homo sapiens Get1/Get2 heterotetramer (a3' deletion variant) in complex with a Get3 dimer | |||||||||
 要素 要素 |
| |||||||||
 キーワード キーワード | MEMBRANE PROTEIN / membrane protein insertion / GET pathway / tail anchored membrane protein | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報arsenite transmembrane transporter activity / membrane insertase activity / GET complex / tail-anchored membrane protein insertion into ER membrane / receptor recycling / 加水分解酵素; 酸無水物に作用 / protein insertion into ER membrane / post-translational protein targeting to endoplasmic reticulum membrane / Insertion of tail-anchored proteins into the endoplasmic reticulum membrane / B cell homeostasis ...arsenite transmembrane transporter activity / membrane insertase activity / GET complex / tail-anchored membrane protein insertion into ER membrane / receptor recycling / 加水分解酵素; 酸無水物に作用 / protein insertion into ER membrane / post-translational protein targeting to endoplasmic reticulum membrane / Insertion of tail-anchored proteins into the endoplasmic reticulum membrane / B cell homeostasis / negative regulation of proteasomal ubiquitin-dependent protein catabolic process / protein-membrane adaptor activity / vesicle-mediated transport / negative regulation of protein ubiquitination / epidermal growth factor receptor signaling pathway / defense response / protein stabilization / ubiquitin protein ligase binding / endoplasmic reticulum membrane / nucleolus / endoplasmic reticulum / signal transduction / ATP hydrolysis activity / extracellular exosome / nucleoplasm / ATP binding / membrane / nucleus / metal ion binding / cytoplasm 類似検索 - 分子機能 | |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 | 電子顕微鏡法 / 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 4.2 Å | |||||||||
 データ登録者 データ登録者 | McDowell, M.A. / Heimes, M. / Wild, K. / Sinning, I. | |||||||||
| 資金援助 |  ドイツ, 2件 ドイツ, 2件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2023 ジャーナル: Nat Commun / 年: 2023タイトル: The GET insertase exhibits conformational plasticity and induces membrane thinning. 著者: Melanie A McDowell / Michael Heimes / Giray Enkavi / Ákos Farkas / Daniel Saar / Klemens Wild / Blanche Schwappach / Ilpo Vattulainen / Irmgard Sinning /   要旨: The eukaryotic guided entry of tail-anchored proteins (GET) pathway mediates the biogenesis of tail-anchored (TA) membrane proteins at the endoplasmic reticulum. In the cytosol, the Get3 chaperone ...The eukaryotic guided entry of tail-anchored proteins (GET) pathway mediates the biogenesis of tail-anchored (TA) membrane proteins at the endoplasmic reticulum. In the cytosol, the Get3 chaperone captures the TA protein substrate and delivers it to the Get1/Get2 membrane protein complex (GET insertase), which then inserts the substrate via a membrane-embedded hydrophilic groove. Here, we present structures, atomistic simulations and functional data of human and Chaetomium thermophilum Get1/Get2/Get3. The core fold of the GET insertase is conserved throughout eukaryotes, whilst thinning of the lipid bilayer occurs in the vicinity of the hydrophilic groove to presumably lower the energetic barrier of membrane insertion. We show that the gating interaction between Get2 helix α3' and Get3 drives conformational changes in both Get3 and the Get1/Get2 membrane heterotetramer. Thus, we provide a framework to understand the conformational plasticity of the GET insertase and how it remodels its membrane environment to promote substrate insertion. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  8cr2.cif.gz 8cr2.cif.gz | 173.3 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb8cr2.ent.gz pdb8cr2.ent.gz | 130.8 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  8cr2.json.gz 8cr2.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  8cr2_validation.pdf.gz 8cr2_validation.pdf.gz | 1.2 MB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  8cr2_full_validation.pdf.gz 8cr2_full_validation.pdf.gz | 1.2 MB | 表示 | |
| XML形式データ |  8cr2_validation.xml.gz 8cr2_validation.xml.gz | 41.6 KB | 表示 | |
| CIF形式データ |  8cr2_validation.cif.gz 8cr2_validation.cif.gz | 59.9 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/cr/8cr2 https://data.pdbj.org/pub/pdb/validation_reports/cr/8cr2 ftp://data.pdbj.org/pub/pdb/validation_reports/cr/8cr2 ftp://data.pdbj.org/pub/pdb/validation_reports/cr/8cr2 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  16802MC  8cqzC  8cr1C  8oduC  8odvC M: このデータのモデリングに利用したマップデータ C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 40146.070 Da / 分子数: 2 / 由来タイプ: 組換発現 / 詳細: Get3 was expressed in E. coli / 由来: (組換発現)  Homo sapiens (ヒト) / 遺伝子: ASNA1, ARSA, TRC40 / 発現宿主: Homo sapiens (ヒト) / 遺伝子: ASNA1, ARSA, TRC40 / 発現宿主:  参照: UniProt: O43681, 加水分解酵素; 酸無水物に作用 #2: タンパク質 | 分子量: 34429.418 Da / 分子数: 2 Mutation: Truncation of 185 N-terminal residues. Residues 242-250 replaced with a GGGG linker 由来タイプ: 組換発現 詳細: Get2-Get1 was expressed as a fusion protein in S. frugiperda 由来: (組換発現)  Homo sapiens (ヒト) / 遺伝子: CAMLG, CAML, GET2, GET1, CHD5, WRB Homo sapiens (ヒト) / 遺伝子: CAMLG, CAML, GET2, GET1, CHD5, WRB発現宿主:  参照: UniProt: P49069, UniProt: O00258 #3: 化合物 | ChemComp-ZN / | 研究の焦点であるリガンドがあるか | N | |
|---|
-実験情報
-実験
| 実験 | 手法: 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法: 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 |
| ||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 分子量 |
| ||||||||||||||||||||||||||||
| 由来(天然) |
| ||||||||||||||||||||||||||||
| 由来(組換発現) |
| ||||||||||||||||||||||||||||
| 緩衝液 | pH: 7.5 | ||||||||||||||||||||||||||||
| 緩衝液成分 |
| ||||||||||||||||||||||||||||
| 試料 | 濃度: 1.2 mg/ml / 包埋: NO / シャドウイング: NO / 染色: NO / 凍結: YES / 詳細: Complex stabilised in PMAL-C8 amphipol | ||||||||||||||||||||||||||||
| 試料支持 | グリッドの材料: COPPER / グリッドのサイズ: 300 divisions/in. / グリッドのタイプ: Quantifoil R2/1 | ||||||||||||||||||||||||||||
| 急速凍結 | 装置: FEI VITROBOT MARK IV / 凍結剤: ETHANE / 湿度: 95 % / 凍結前の試料温度: 279 K |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TITAN KRIOS |
| 電子銃 | 電子線源:  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2400 nm / 最小 デフォーカス(公称値): 1200 nm / Cs: 2.7 mm |
| 試料ホルダ | 凍結剤: NITROGEN |
| 撮影 | 平均露光時間: 2.58 sec. / 電子線照射量: 53.2 e/Å2 / 検出モード: COUNTING / フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 撮影したグリッド数: 1 / 実像数: 12311 |
- 解析
解析
| ソフトウェア | 名称: PHENIX / バージョン: 1.19_4092: / 分類: 精密化 | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| EMソフトウェア |
| ||||||||||||||||||||||||||||||||||||
| CTF補正 | タイプ: PHASE FLIPPING AND AMPLITUDE CORRECTION | ||||||||||||||||||||||||||||||||||||
| 粒子像の選択 | 選択した粒子像数: 2044854 | ||||||||||||||||||||||||||||||||||||
| 対称性 | 点対称性: C1 (非対称) | ||||||||||||||||||||||||||||||||||||
| 3次元再構成 | 解像度: 4.2 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 224354 / 対称性のタイプ: POINT | ||||||||||||||||||||||||||||||||||||
| 原子モデル構築 | プロトコル: RIGID BODY FIT / 空間: REAL | ||||||||||||||||||||||||||||||||||||
| 原子モデル構築 | PDB-ID: 6SO5 Accession code: 6SO5 / Source name: PDB / タイプ: experimental model | ||||||||||||||||||||||||||||||||||||
| 拘束条件 |
|
 ムービー
ムービー コントローラー
コントローラー






 PDBj
PDBj