+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 7xsq | ||||||
|---|---|---|---|---|---|---|---|
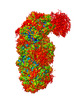
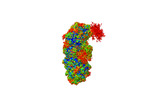
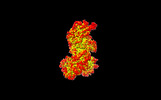
| タイトル | Structure of the Craspase | ||||||
 要素 要素 |
| ||||||
 キーワード キーワード | IMMUNE SYSTEM/RNA / IMMUNE SYSTEM-RNA complex | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報 | ||||||
| 生物種 |  Candidatus Scalindua brodae (バクテリア) Candidatus Scalindua brodae (バクテリア) | ||||||
| 手法 | 電子顕微鏡法 / 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.88 Å | ||||||
 データ登録者 データ登録者 | Feng, Y. / Zhang, L. | ||||||
| 資金援助 |  中国, 1件 中国, 1件
| ||||||
 引用 引用 |  ジャーナル: Mol Cell / 年: 2022 ジャーナル: Mol Cell / 年: 2022タイトル: Target RNA activates the protease activity of Craspase to confer antiviral defense. 著者: Xi Liu / Laixing Zhang / Hao Wang / Yu Xiu / Ling Huang / Zhengyu Gao / Ningning Li / Feixue Li / Weijia Xiong / Teng Gao / Yi Zhang / Maojun Yang / Yue Feng /  要旨: In the type III-E CRISPR-Cas system, a Cas effector (gRAMP) is associated with a TPR-CHAT to form Craspase (CRISPR-guided caspase). However, both the structural features of gRAMP and the immunity ...In the type III-E CRISPR-Cas system, a Cas effector (gRAMP) is associated with a TPR-CHAT to form Craspase (CRISPR-guided caspase). However, both the structural features of gRAMP and the immunity mechanism remain unknown for this system. Here, we report structures of gRAMP-crRNA and gRAMP:cRNA:target RNA as well as structures of Craspase and Craspase complexed with cognate target RNA (CTR) or non-cognate target RNA (NTR). Importantly, the 3' anti-tag region of NTR and CTR binds at two distinct channels in Craspase, and CTR with a non-complementary 3' anti-tag induces a marked conformational change of the TPR-CHAT, which allosterically activates its protease activity to cleave an ancillary protein Csx30. This cleavage then triggers an abortive infection as the antiviral strategy of the type III-E system. Together, our study provides crucial insights into both the catalytic mechanism of the gRAMP and the immunity mechanism of the type III-E system. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  7xsq.cif.gz 7xsq.cif.gz | 388.5 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb7xsq.ent.gz pdb7xsq.ent.gz | 301.5 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  7xsq.json.gz 7xsq.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  7xsq_validation.pdf.gz 7xsq_validation.pdf.gz | 1.2 MB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  7xsq_full_validation.pdf.gz 7xsq_full_validation.pdf.gz | 1.2 MB | 表示 | |
| XML形式データ |  7xsq_validation.xml.gz 7xsq_validation.xml.gz | 62.5 KB | 表示 | |
| CIF形式データ |  7xsq_validation.cif.gz 7xsq_validation.cif.gz | 97.3 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/xs/7xsq https://data.pdbj.org/pub/pdb/validation_reports/xs/7xsq ftp://data.pdbj.org/pub/pdb/validation_reports/xs/7xsq ftp://data.pdbj.org/pub/pdb/validation_reports/xs/7xsq | HTTPS FTP |
-関連構造データ
| 関連構造データ |  33431MC  7xsoC  7xspC  7xsrC  7xssC  7xt4C M: このデータのモデリングに利用したマップデータ C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 197823.797 Da / 分子数: 1 / 由来タイプ: 組換発現 詳細: Using a different transcription start point, the protein has additional five residues in its N-terminus. 由来: (組換発現)  Candidatus Scalindua brodae (バクテリア) Candidatus Scalindua brodae (バクテリア)遺伝子: SCABRO_02597 / 発現宿主:  | ||
|---|---|---|---|
| #2: タンパク質 | 分子量: 82549.992 Da / 分子数: 1 / 由来タイプ: 組換発現 由来: (組換発現)  Candidatus Scalindua brodae (バクテリア) Candidatus Scalindua brodae (バクテリア)遺伝子: SCABRO_02601 / 発現宿主:  | ||
| #3: RNA鎖 | 分子量: 23741.119 Da / 分子数: 1 / 由来タイプ: 組換発現 由来: (組換発現)  Candidatus Scalindua brodae (バクテリア) Candidatus Scalindua brodae (バクテリア)発現宿主:  | ||
| #4: 化合物 | ChemComp-ZN / 研究の焦点であるリガンドがあるか | Y | |
-実験情報
-実験
| 実験 | 手法: 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法: 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 |
| ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 由来(天然) |
| ||||||||||||||||||||||||
| 由来(組換発現) |
| ||||||||||||||||||||||||
| 緩衝液 | pH: 7 | ||||||||||||||||||||||||
| 試料 | 包埋: NO / シャドウイング: NO / 染色: NO / 凍結: YES | ||||||||||||||||||||||||
| 急速凍結 | 凍結剤: ETHANE |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TITAN KRIOS |
| 電子銃 | 電子線源:  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: OTHER FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: OTHER |
| 電子レンズ | モード: DARK FIELD / 最大 デフォーカス(公称値): 2000 nm / 最小 デフォーカス(公称値): 1700 nm |
| 撮影 | 電子線照射量: 50 e/Å2 / フィルム・検出器のモデル: GATAN K3 (6k x 4k) |
- 解析
解析
| ソフトウェア | 名称: PHENIX / バージョン: 1.17.1_3660: / 分類: 精密化 | ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| CTF補正 | タイプ: PHASE FLIPPING AND AMPLITUDE CORRECTION | ||||||||||||||||||||||||
| 3次元再構成 | 解像度: 2.88 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 229997 / 対称性のタイプ: POINT | ||||||||||||||||||||||||
| 拘束条件 |
|
 ムービー
ムービー コントローラー
コントローラー





 PDBj
PDBj































