+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-8185 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | aerolysin prepore cryo-EM map | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報toxin activity / host cell plasma membrane / extracellular region / identical protein binding / membrane 類似検索 - 分子機能 | |||||||||
| 生物種 |  Aeromonas hydrophila (バクテリア) Aeromonas hydrophila (バクテリア) | |||||||||
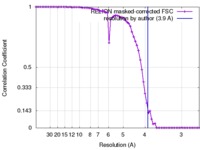
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.9 Å | |||||||||
 データ登録者 データ登録者 | Iacovache I / Zuber B | |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2016 ジャーナル: Nat Commun / 年: 2016タイトル: Cryo-EM structure of aerolysin variants reveals a novel protein fold and the pore-formation process. 著者: Ioan Iacovache / Sacha De Carlo / Nuria Cirauqui / Matteo Dal Peraro / F Gisou van der Goot / Benoît Zuber /    要旨: Owing to their pathogenical role and unique ability to exist both as soluble proteins and transmembrane complexes, pore-forming toxins (PFTs) have been a focus of microbiologists and structural ...Owing to their pathogenical role and unique ability to exist both as soluble proteins and transmembrane complexes, pore-forming toxins (PFTs) have been a focus of microbiologists and structural biologists for decades. PFTs are generally secreted as water-soluble monomers and subsequently bind the membrane of target cells. Then, they assemble into circular oligomers, which undergo conformational changes that allow membrane insertion leading to pore formation and potentially cell death. Aerolysin, produced by the human pathogen Aeromonas hydrophila, is the founding member of a major PFT family found throughout all kingdoms of life. We report cryo-electron microscopy structures of three conformational intermediates and of the final aerolysin pore, jointly providing insight into the conformational changes that allow pore formation. Moreover, the structures reveal a protein fold consisting of two concentric β-barrels, tightly kept together by hydrophobic interactions. This fold suggests a basis for the prion-like ultrastability of aerolysin pore and its stoichiometry. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_8185.map.gz emd_8185.map.gz | 4.6 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-8185-v30.xml emd-8185-v30.xml emd-8185.xml emd-8185.xml | 11.4 KB 11.4 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_8185_fsc.xml emd_8185_fsc.xml | 6.9 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_8185.png emd_8185.png | 79.6 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-8185 http://ftp.pdbj.org/pub/emdb/structures/EMD-8185 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-8185 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-8185 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_8185_validation.pdf.gz emd_8185_validation.pdf.gz | 281.3 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_8185_full_validation.pdf.gz emd_8185_full_validation.pdf.gz | 280.4 KB | 表示 | |
| XML形式データ |  emd_8185_validation.xml.gz emd_8185_validation.xml.gz | 9.6 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-8185 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-8185 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-8185 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-8185 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_8185.map.gz / 形式: CCP4 / 大きさ: 30.5 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_8185.map.gz / 形式: CCP4 / 大きさ: 30.5 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.34 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
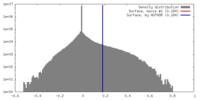
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : aerolysin prepore
| 全体 | 名称: aerolysin prepore |
|---|---|
| 要素 |
|
-超分子 #1: aerolysin prepore
| 超分子 | 名称: aerolysin prepore / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all 詳細: Aerolysin oligomer arrested in it's prepore conformation by mutagenesis (Y221G). |
|---|---|
| 由来(天然) | 生物種:  Aeromonas hydrophila (バクテリア) Aeromonas hydrophila (バクテリア) |
| 組換発現 | 生物種:  |
| 分子量 | 理論値: 350 KDa |
-分子 #1: Aerolysin
| 分子 | 名称: Aerolysin / タイプ: protein_or_peptide / ID: 1 / コピー数: 14 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Aeromonas hydrophila (バクテリア) Aeromonas hydrophila (バクテリア) |
| 分子量 | 理論値: 47.079031 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: AEPVYPDQLR LFSLGQGVCG DKYRPVNREE AQSVKSNIVG MMGQWQISGL ANGWVIMGPG YNGEIKPGTA SNTWCYPTNP VTGEIPTLS ALDIPDGDEV DVQWRLVHDS ANFIKPTSYL AHYLGYAWVG GNHSQYVGED MDVTRDGDGW VIRGNNDGGC D GYRCGDKT ...文字列: AEPVYPDQLR LFSLGQGVCG DKYRPVNREE AQSVKSNIVG MMGQWQISGL ANGWVIMGPG YNGEIKPGTA SNTWCYPTNP VTGEIPTLS ALDIPDGDEV DVQWRLVHDS ANFIKPTSYL AHYLGYAWVG GNHSQYVGED MDVTRDGDGW VIRGNNDGGC D GYRCGDKT AIKVSNFAYN LDPDSFKHGD VTQSDRQLVK TVVGWAVNDS DTPQSGYDVT LRGDTATNWS KTNTYGLSEK VT TKNKFKW PLVGETELSI EIAANQSWAS QNGGSTTTSL SQSVRPTVPA RSKIPVKIEL YKADISYPYE FKADVSYDLT LSG FLRWGG NAWYTHPDNR PNWNHTFVIG PYKDKASSIR YQWDKRYIPG EVKWWDWNWT IQQNGLSTMQ NNLARVLRPV RAGI TGDFS AESQFAGNIE IGAPVPLAA |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.4 mg/mL |
|---|---|
| 緩衝液 | pH: 7.4 |
| グリッド | モデル: Quantifoil R2/1 / 材質: COPPER / メッシュ: 300 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: GLOW DISCHARGE |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 70 % / チャンバー内温度: 295 K / 装置: FEI VITROBOT MARK IV 詳細: 30 seconds glow discharged grids, 4ul sample, 5 seconds blot. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: FEI FALCON II (4k x 4k) 検出モード: INTEGRATING / 平均露光時間: 1.0 sec. / 平均電子線量: 22.42 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 精密化 | プロトコル: FLEXIBLE FIT |
|---|---|
| 得られたモデル |  PDB-5jzh: |
 ムービー
ムービー コントローラー
コントローラー

















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)