+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-7618 | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Alpha Synuclein fibril formed by full length protein - Rod Polymorph | ||||||||||||
 マップデータ マップデータ | em-volume_P1.map | ||||||||||||
 試料 試料 |
| ||||||||||||
 キーワード キーワード | Parkinson's disease / Synucleinopathy / Amyloid aggregation / Fibril polymorphism / PROTEIN FIBRIL | ||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報negative regulation of mitochondrial electron transport, NADH to ubiquinone / neutral lipid metabolic process / regulation of acyl-CoA biosynthetic process / negative regulation of dopamine uptake involved in synaptic transmission / negative regulation of norepinephrine uptake / response to desipramine / positive regulation of SNARE complex assembly / positive regulation of hydrogen peroxide catabolic process / supramolecular fiber / regulation of synaptic vesicle recycling ...negative regulation of mitochondrial electron transport, NADH to ubiquinone / neutral lipid metabolic process / regulation of acyl-CoA biosynthetic process / negative regulation of dopamine uptake involved in synaptic transmission / negative regulation of norepinephrine uptake / response to desipramine / positive regulation of SNARE complex assembly / positive regulation of hydrogen peroxide catabolic process / supramolecular fiber / regulation of synaptic vesicle recycling / negative regulation of chaperone-mediated autophagy / regulation of reactive oxygen species biosynthetic process / positive regulation of protein localization to cell periphery / mitochondrial membrane organization / negative regulation of exocytosis / regulation of glutamate secretion / dopamine biosynthetic process / response to iron(II) ion / positive regulation of neurotransmitter secretion / regulation of macrophage activation / negative regulation of dopamine metabolic process / negative regulation of platelet-derived growth factor receptor signaling pathway / SNARE complex assembly / negative regulation of thrombin-activated receptor signaling pathway / Lewy body / regulation of locomotion / negative regulation of microtubule polymerization / positive regulation of inositol phosphate biosynthetic process / synaptic vesicle priming / regulation of norepinephrine uptake / transporter regulator activity / protein kinase inhibitor activity / synaptic vesicle transport / dopamine uptake involved in synaptic transmission / regulation of dopamine secretion / positive regulation of receptor recycling / positive regulation of exocytosis / cuprous ion binding / mitochondrial ATP synthesis coupled electron transport / nuclear outer membrane / dynein complex binding / response to magnesium ion / synaptic vesicle exocytosis / positive regulation of endocytosis / negative regulation of serotonin uptake / response to type II interferon / kinesin binding / cysteine-type endopeptidase inhibitor activity / regulation of presynapse assembly / synaptic vesicle endocytosis / alpha-tubulin binding / beta-tubulin binding / phospholipase binding / phospholipid metabolic process / supramolecular fiber organization / behavioral response to cocaine / cellular response to fibroblast growth factor stimulus / cellular response to epinephrine stimulus / inclusion body / Hsp70 protein binding / enzyme inhibitor activity / response to interleukin-1 / axon terminus / cellular response to copper ion / positive regulation of release of sequestered calcium ion into cytosol / regulation of microtubule cytoskeleton organization / SNARE binding / adult locomotory behavior / glutathione metabolic process / protein tetramerization / excitatory postsynaptic potential / protein sequestering activity / tubulin binding / phosphoprotein binding / microglial cell activation / ferrous iron binding / fatty acid metabolic process / PKR-mediated signaling / phospholipid binding / regulation of long-term neuronal synaptic plasticity / synapse organization / receptor internalization / protein destabilization / tau protein binding / enzyme activator activity / terminal bouton / positive regulation of inflammatory response / long-term synaptic potentiation / synaptic vesicle membrane / actin cytoskeleton / growth cone / actin binding / cellular response to oxidative stress / neuron apoptotic process / cell cortex / histone binding / response to lipopolysaccharide / microtubule binding / amyloid fibril formation / chemical synaptic transmission 類似検索 - 分子機能 | ||||||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | ||||||||||||
| 手法 | らせん対称体再構成法 / クライオ電子顕微鏡法 / 解像度: 3.5 Å | ||||||||||||
 データ登録者 データ登録者 | Li B / Hatami A | ||||||||||||
| 資金援助 |  米国, 3件 米国, 3件
| ||||||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2018 ジャーナル: Nat Commun / 年: 2018タイトル: Cryo-EM of full-length α-synuclein reveals fibril polymorphs with a common structural kernel. 著者: Binsen Li / Peng Ge / Kevin A Murray / Phorum Sheth / Meng Zhang / Gayatri Nair / Michael R Sawaya / Woo Shik Shin / David R Boyer / Shulin Ye / David S Eisenberg / Z Hong Zhou / Lin Jiang /  要旨: α-Synuclein (aSyn) fibrillar polymorphs have distinct in vitro and in vivo seeding activities, contributing differently to synucleinopathies. Despite numerous prior attempts, how polymorphic aSyn ...α-Synuclein (aSyn) fibrillar polymorphs have distinct in vitro and in vivo seeding activities, contributing differently to synucleinopathies. Despite numerous prior attempts, how polymorphic aSyn fibrils differ in atomic structure remains elusive. Here, we present fibril polymorphs from the full-length recombinant human aSyn and their seeding capacity and cytotoxicity in vitro. By cryo-electron microscopy helical reconstruction, we determine the structures of the two predominant species, a rod and a twister, both at 3.7 Å resolution. Our atomic models reveal that both polymorphs share a kernel structure of a bent β-arch, but differ in their inter-protofilament interfaces. Thus, different packing of the same kernel structure gives rise to distinct fibril polymorphs. Analyses of disease-related familial mutations suggest their potential contribution to the pathogenesis of synucleinopathies by altering population distribution of the fibril polymorphs. Drug design targeting amyloid fibrils in neurodegenerative diseases should consider the formation and distribution of concurrent fibril polymorphs. | ||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_7618.map.gz emd_7618.map.gz | 25.2 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-7618-v30.xml emd-7618-v30.xml emd-7618.xml emd-7618.xml | 14.7 KB 14.7 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_7618.png emd_7618.png | 215.3 KB | ||
| マスクデータ |  emd_7618_msk_1.map emd_7618_msk_1.map | 27 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-7618.cif.gz emd-7618.cif.gz | 6 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-7618 http://ftp.pdbj.org/pub/emdb/structures/EMD-7618 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-7618 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-7618 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_7618.map.gz / 形式: CCP4 / 大きさ: 27 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_7618.map.gz / 形式: CCP4 / 大きさ: 27 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | em-volume_P1.map | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.07 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
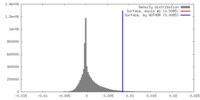
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-マスク #1
| ファイル |  emd_7618_msk_1.map emd_7618_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
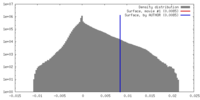
| 投影像・断面図 |
| ||||||||||||
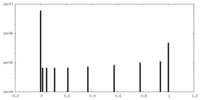
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Alpha-synuclein fibril - rod polymorph
| 全体 | 名称: Alpha-synuclein fibril - rod polymorph |
|---|---|
| 要素 |
|
-超分子 #1: Alpha-synuclein fibril - rod polymorph
| 超分子 | 名称: Alpha-synuclein fibril - rod polymorph / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
-分子 #1: Alpha-synuclein
| 分子 | 名称: Alpha-synuclein / タイプ: protein_or_peptide / ID: 1 / コピー数: 10 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 14.476108 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MDVFMKGLSK AKEGVVAAAE KTKQGVAEAA GKTKEGVLYV GSKTKEGVVH GVATVAEKTK EQVTNVGGAV VTGVTAVAQK TVEGAGSIA AATGFVKKDQ LGKNEEGAPQ EGILEDMPVD PDNEAYEMPS EEGYQDYEPE A UniProtKB: Alpha-synuclein |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | らせん対称体再構成法 |
| 試料の集合状態 | filament |
- 試料調製
試料調製
| 緩衝液 | pH: 3 / 構成要素 - 濃度: 15.0 mM / 構成要素 - 式: C16H36BrP / 構成要素 - 名称: tetrabutylphosphonium bromide |
|---|---|
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: COPPER / メッシュ: 200 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY ARRAY / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 240 sec. / 前処理 - 雰囲気: AIR 詳細: Quantifoil grid was treated with 1,2-Dichloroethane for one week, coated with additional carbon, and baken under 120kV in Camera chamber for 3 days |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 295 K / 装置: FEI VITROBOT MARK IV / 詳細: blot force: 1 blot time: 4s. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 温度 | 最低: 77.0 K / 最高: 77.0 K |
| 特殊光学系 | エネルギーフィルター - 名称: GIF Quantum LS エネルギーフィルター - エネルギー下限: -10 eV エネルギーフィルター - エネルギー上限: 10 eV |
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: COUNTING / デジタル化 - サイズ - 横: 3838 pixel / デジタル化 - サイズ - 縦: 3710 pixel / デジタル化 - 画像ごとのフレーム数: 3-20 / 撮影したグリッド数: 1 / 実像数: 1821 / 平均露光時間: 10.0 sec. / 平均電子線量: 30.0 e/Å2 / 詳細: Frame rate 5 Hz |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 50.0 µm / 最大 デフォーカス(補正後): 4.0 µm / 最小 デフォーカス(補正後): 1.5 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.7 µm / 最小 デフォーカス(公称値): 2.7 µm / 倍率(公称値): 130000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 最終 再構成 | 想定した対称性 - らせんパラメータ - Δz: 2.4 Å 想定した対称性 - らせんパラメータ - ΔΦ: 179.53 ° 想定した対称性 - らせんパラメータ - 軸対称性: C1 (非対称) アルゴリズム: BACK PROJECTION / 解像度のタイプ: BY AUTHOR / 解像度: 3.5 Å / 解像度の算出法: FSC 0.5 CUT-OFF / ソフトウェア - 名称: RELION (ver. 2.0) / 使用した粒子像数: 23830 |
|---|---|
| Segment selection | 選択した数: 182253 |
| 初期モデル | モデルのタイプ: NONE 詳細: A elongated Gaussian blob was used for initial model. |
| 最終 角度割当 | タイプ: NOT APPLICABLE / ソフトウェア - 名称: RELION (ver. 2.0) |
-原子モデル構築 1
| 精密化 | 空間: REAL / プロトコル: AB INITIO MODEL |
|---|---|
| 得られたモデル |  PDB-6cu7: |
 ムービー
ムービー コントローラー
コントローラー








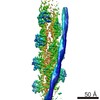






 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)