+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of KpFtsZ-ZapA complex | ||||||||||||||||||||||||||||||||||||
 マップデータ マップデータ | |||||||||||||||||||||||||||||||||||||
 試料 試料 |
| ||||||||||||||||||||||||||||||||||||
 キーワード キーワード | bacterial cell division / divisome / FtsZ / ZapA / CELL CYCLE | ||||||||||||||||||||||||||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報septin ring assembly / cell septum / division septum assembly / FtsZ-dependent cytokinesis / cell division site / protein polymerization / GTPase activity / GTP binding / plasma membrane / cytosol / cytoplasm 類似検索 - 分子機能 | ||||||||||||||||||||||||||||||||||||
| 生物種 |  Klebsiella pneumoniae (肺炎桿菌) / Klebsiella pneumoniae (肺炎桿菌) /  Klebsiella pneumoniae subsp. pneumoniae MGH 78578 (肺炎桿菌) / Klebsiella pneumoniae subsp. pneumoniae MGH 78578 (肺炎桿菌) /  Klebsiella pneumoniae 342 (肺炎桿菌) Klebsiella pneumoniae 342 (肺炎桿菌) | ||||||||||||||||||||||||||||||||||||
| 手法 | らせん対称体再構成法 / クライオ電子顕微鏡法 / 解像度: 2.73 Å | ||||||||||||||||||||||||||||||||||||
 データ登録者 データ登録者 | Fujita J / Hibino K / Kagoshima G / Kamimura N / Kato Y / Uehara R / Namba K / Uchihashi T / Matsumura H | ||||||||||||||||||||||||||||||||||||
| 資金援助 |  日本, 11件 日本, 11件
| ||||||||||||||||||||||||||||||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2025 ジャーナル: Nat Commun / 年: 2025タイトル: Structural basis for the interaction between the bacterial cell division proteins FtsZ and ZapA. 著者: Junso Fujita / Kazuki Kasai / Kota Hibino / Gota Kagoshima / Natsuki Kamimura / Shungo Tobita / Yuki Kato / Ryo Uehara / Keiichi Namba / Takayuki Uchihashi / Hiroyoshi Matsumura /  要旨: Cell division in most bacteria is regulated by the tubulin homolog FtsZ as well as ZapA, a FtsZ-associated protein. However, how FtsZ and ZapA function coordinately has remained elusive. Here we ...Cell division in most bacteria is regulated by the tubulin homolog FtsZ as well as ZapA, a FtsZ-associated protein. However, how FtsZ and ZapA function coordinately has remained elusive. Here we report the cryo-electron microscopy structure of the ZapA-FtsZ complex at 2.73 Å resolution. The complex forms an asymmetric ladder-like structure, in which the double antiparallel FtsZ protofilament on one side and a single protofilament on the other side are tethered by ZapA tetramers. In the complex, the extensive interactions of FtsZ with ZapA cause a structural change of the FtsZ protofilament, and the formation of the double FtsZ protofilament increases electrostatic repulsion. High-speed atomic force microscopy analysis revealed cooperative interactions of ZapA with FtsZ at a molecular level. Our findings not only provide a structural basis for the interaction between FtsZ and ZapA but also shed light on how ZapA binds to FtsZ protofilaments without disturbing FtsZ dynamics to promote cell division. | ||||||||||||||||||||||||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_60837.map.gz emd_60837.map.gz | 26.4 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-60837-v30.xml emd-60837-v30.xml emd-60837.xml emd-60837.xml | 24 KB 24 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_60837_fsc.xml emd_60837_fsc.xml | 10.5 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_60837.png emd_60837.png | 30 KB | ||
| マスクデータ |  emd_60837_msk_1.map emd_60837_msk_1.map | 125 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-60837.cif.gz emd-60837.cif.gz | 7.1 KB | ||
| その他 |  emd_60837_half_map_1.map.gz emd_60837_half_map_1.map.gz emd_60837_half_map_2.map.gz emd_60837_half_map_2.map.gz | 116.1 MB 116.1 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-60837 http://ftp.pdbj.org/pub/emdb/structures/EMD-60837 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-60837 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-60837 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_60837_validation.pdf.gz emd_60837_validation.pdf.gz | 1.2 MB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_60837_full_validation.pdf.gz emd_60837_full_validation.pdf.gz | 1.2 MB | 表示 | |
| XML形式データ |  emd_60837_validation.xml.gz emd_60837_validation.xml.gz | 19.5 KB | 表示 | |
| CIF形式データ |  emd_60837_validation.cif.gz emd_60837_validation.cif.gz | 25.1 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-60837 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-60837 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-60837 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-60837 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  9iskMC  9isjC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_60837.map.gz / 形式: CCP4 / 大きさ: 125 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_60837.map.gz / 形式: CCP4 / 大きさ: 125 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ボクセルのサイズ | X=Y=Z: 0.878 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : KpFtsZ-ZapA complex
| 全体 | 名称: KpFtsZ-ZapA complex |
|---|---|
| 要素 |
|
-超分子 #1: KpFtsZ-ZapA complex
| 超分子 | 名称: KpFtsZ-ZapA complex / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1-#2 |
|---|---|
| 由来(天然) | 生物種:  Klebsiella pneumoniae (肺炎桿菌) Klebsiella pneumoniae (肺炎桿菌) |
-分子 #1: Cell division protein FtsZ
| 分子 | 名称: Cell division protein FtsZ / タイプ: protein_or_peptide / ID: 1 / コピー数: 6 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Klebsiella pneumoniae subsp. pneumoniae MGH 78578 (肺炎桿菌) Klebsiella pneumoniae subsp. pneumoniae MGH 78578 (肺炎桿菌)株: ATCC 700721 / MGH 78578 |
| 分子量 | 理論値: 40.37973 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MFEPMELTND AVIKVIGVGG GGGNAVEHMV RERIEGVEFF AVNTDAQALR KTAVGQTIQI GSGITKGLGA GANPEVGRNA ADEDREALR AALDGADMVF IAAGMGGGTG TGAAPVVAEV AKDLGILTVA VVTKPFNFEG KKRMAFAEQG ITELSKHVDS L ITIPNDKL ...文字列: MFEPMELTND AVIKVIGVGG GGGNAVEHMV RERIEGVEFF AVNTDAQALR KTAVGQTIQI GSGITKGLGA GANPEVGRNA ADEDREALR AALDGADMVF IAAGMGGGTG TGAAPVVAEV AKDLGILTVA VVTKPFNFEG KKRMAFAEQG ITELSKHVDS L ITIPNDKL LKVLGRGISL LDAFGAANDV LKGAVQGIAE LITRPGLMNV DFADVRTVMS EMGYAMMGSG VASGEDRAEE AA EMAISSP LLEDIDLSGA RGVLVNITAG FDLRLDEFET VGNTIRAFAS DNATVVIGTS LDPDMNDELR VTVVATGIGM DKR PEITLV TNKQVQQPVM DRYQQHGMSP LTQEQKPAAK VVNDNTPQTA KEPDYLDIPA FLRKQAD UniProtKB: Cell division protein FtsZ |
-分子 #2: Cell division protein ZapA
| 分子 | 名称: Cell division protein ZapA / タイプ: protein_or_peptide / ID: 2 / コピー数: 8 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Klebsiella pneumoniae 342 (肺炎桿菌) / 株: 342 Klebsiella pneumoniae 342 (肺炎桿菌) / 株: 342 |
| 分子量 | 理論値: 12.609186 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MSAQPVDLQI FGRSLRVNCP PEQRDALNQA AEDLNQRLQD LKERTRVTNT EQLVFIAALN ISYELTQEKA KTRDYASSME QRIRMLQQT IEQALLEQGR ISERPGSKFE UniProtKB: Cell division protein ZapA |
-分子 #3: PHOSPHOMETHYLPHOSPHONIC ACID GUANYLATE ESTER
| 分子 | 名称: PHOSPHOMETHYLPHOSPHONIC ACID GUANYLATE ESTER / タイプ: ligand / ID: 3 / コピー数: 6 / 式: G2P |
|---|---|
| 分子量 | 理論値: 521.208 Da |
| Chemical component information | 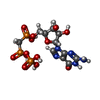 ChemComp-G2P: |
-分子 #4: MAGNESIUM ION
| 分子 | 名称: MAGNESIUM ION / タイプ: ligand / ID: 4 / コピー数: 6 / 式: MG |
|---|---|
| 分子量 | 理論値: 24.305 Da |
-分子 #5: POTASSIUM ION
| 分子 | 名称: POTASSIUM ION / タイプ: ligand / ID: 5 / コピー数: 6 / 式: K |
|---|---|
| 分子量 | 理論値: 39.098 Da |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | らせん対称体再構成法 |
| 試料の集合状態 | filament |
- 試料調製
試料調製
| 緩衝液 | pH: 7.5 構成要素:
| ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: COPPER / メッシュ: 200 / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 20 sec. / 前処理 - 雰囲気: AIR / 詳細: 20 mA | ||||||||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK IV | ||||||||||||||||||
| 詳細 | 0.3 mg/ml KpFtsZ and 0.19 mg/ml KpZapA |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | JEOL CRYO ARM 300 |
|---|---|
| 特殊光学系 | エネルギーフィルター - 名称: In-column Omega Filter エネルギーフィルター - スリット幅: 20 eV |
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 撮影したグリッド数: 1 / 平均露光時間: 2.3 sec. / 平均電子線量: 60.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.0 µm / 最小 デフォーカス(公称値): 0.5 µm / 倍率(公称値): 60000 |
| 試料ステージ | 試料ホルダーモデル: JEOL CRYOSPECPORTER / ホルダー冷却材: NITROGEN |
 ムービー
ムービー コントローラー
コントローラー








