+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | cryo-EM structure of human haemoglobin in oxy form | |||||||||
 マップデータ マップデータ | sharpened map | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Haemoglobin / OXYGEN BINDING | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報nitric oxide transport / hemoglobin alpha binding / cellular oxidant detoxification / hemoglobin binding / haptoglobin-hemoglobin complex / renal absorption / organic acid binding / hemoglobin complex / oxygen transport / Scavenging of heme from plasma ...nitric oxide transport / hemoglobin alpha binding / cellular oxidant detoxification / hemoglobin binding / haptoglobin-hemoglobin complex / renal absorption / organic acid binding / hemoglobin complex / oxygen transport / Scavenging of heme from plasma / endocytic vesicle lumen / blood vessel diameter maintenance / platelet aggregation / hydrogen peroxide catabolic process / oxygen carrier activity / Late endosomal microautophagy / carbon dioxide transport / Heme signaling / Erythrocytes take up oxygen and release carbon dioxide / Erythrocytes take up carbon dioxide and release oxygen / response to hydrogen peroxide / Cytoprotection by HMOX1 / oxygen binding / regulation of blood pressure / Chaperone Mediated Autophagy / positive regulation of nitric oxide biosynthetic process / tertiary granule lumen / Factors involved in megakaryocyte development and platelet production / ficolin-1-rich granule lumen / blood microparticle / iron ion binding / heme binding / Neutrophil degranulation / extracellular space / extracellular exosome / extracellular region / membrane / metal ion binding / cytosol 類似検索 - 分子機能 | |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
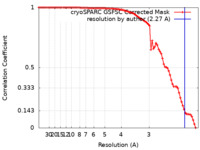
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.27 Å | |||||||||
 データ登録者 データ登録者 | Takahashi K / Lee Y / Fago A / Bautista NM / Kawamoto A / Kurisu G / Storz J / Nishizawa T / Tame JRH | |||||||||
| 資金援助 |  日本, 1件 日本, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2024 ジャーナル: Nat Commun / 年: 2024タイトル: The unique allosteric property of crocodilian haemoglobin elucidated by cryo-EM. 著者: Katsuya Takahashi / Yongchan Lee / Angela Fago / Naim M Bautista / Jay F Storz / Akihiro Kawamoto / Genji Kurisu / Tomohiro Nishizawa / Jeremy R H Tame /    要旨: The principal effect controlling the oxygen affinity of vertebrate haemoglobins (Hbs) is the allosteric switch between R and T forms with relatively high and low oxygen affinity respectively. ...The principal effect controlling the oxygen affinity of vertebrate haemoglobins (Hbs) is the allosteric switch between R and T forms with relatively high and low oxygen affinity respectively. Uniquely among jawed vertebrates, crocodilians possess Hb that shows a profound drop in oxygen affinity in the presence of bicarbonate ions. This allows them to stay underwater for extended periods by consuming almost all the oxygen present in the blood-stream, as metabolism releases carbon dioxide, whose conversion to bicarbonate and hydrogen ions is catalysed by carbonic anhydrase. Despite the apparent universal utility of bicarbonate as an allosteric regulator of Hb, this property evolved only in crocodilians. We report here the molecular structures of both human and a crocodilian Hb in the deoxy and liganded states, solved by cryo-electron microscopy. We reveal the precise interactions between two bicarbonate ions and the crocodilian protein at symmetry-related sites found only in the T state. No other known effector of vertebrate Hbs binds anywhere near these sites. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_37575.map.gz emd_37575.map.gz | 59.6 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-37575-v30.xml emd-37575-v30.xml emd-37575.xml emd-37575.xml | 18.1 KB 18.1 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_37575_fsc.xml emd_37575_fsc.xml | 8.4 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_37575.png emd_37575.png | 103.5 KB | ||
| マスクデータ |  emd_37575_msk_1.map emd_37575_msk_1.map | 64 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-37575.cif.gz emd-37575.cif.gz | 6 KB | ||
| その他 |  emd_37575_half_map_1.map.gz emd_37575_half_map_1.map.gz emd_37575_half_map_2.map.gz emd_37575_half_map_2.map.gz | 59.4 MB 59.4 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-37575 http://ftp.pdbj.org/pub/emdb/structures/EMD-37575 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-37575 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-37575 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_37575_validation.pdf.gz emd_37575_validation.pdf.gz | 803.7 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_37575_full_validation.pdf.gz emd_37575_full_validation.pdf.gz | 803.3 KB | 表示 | |
| XML形式データ |  emd_37575_validation.xml.gz emd_37575_validation.xml.gz | 16.3 KB | 表示 | |
| CIF形式データ |  emd_37575_validation.cif.gz emd_37575_validation.cif.gz | 21.1 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-37575 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-37575 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-37575 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-37575 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_37575.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_37575.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | sharpened map | ||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.02 Å | ||||||||||||||||||||||||||||||||||||
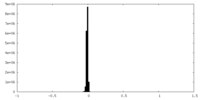
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-マスク #1
| ファイル |  emd_37575_msk_1.map emd_37575_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
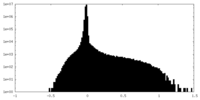
| 密度ヒストグラム |
-ハーフマップ: half map B
| ファイル | emd_37575_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | half map B | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: half map A
| ファイル | emd_37575_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | half map A | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : human haemoglobin in oxy form
| 全体 | 名称: human haemoglobin in oxy form |
|---|---|
| 要素 |
|
-超分子 #1: human haemoglobin in oxy form
| 超分子 | 名称: human haemoglobin in oxy form / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1-#2 |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 100 KDa |
-分子 #1: Hemoglobin subunit alpha
| 分子 | 名称: Hemoglobin subunit alpha / タイプ: protein_or_peptide / ID: 1 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 15.28155 KDa |
| 配列 | 文字列: MVLSPADKTN VKAAWGKVGA HAGEYGAEAL ERMFLSFPTT KTYFPHFDLS HGSAQVKGHG KKVADALTNA VAHVDDMPNA LSALSDLHA HKLRVDPVNF KLLSHCLLVT LAAHLPAEFT PAVHASLDKF LASVSTVLTS KYR UniProtKB: Hemoglobin subunit alpha |
-分子 #2: Hemoglobin subunit beta
| 分子 | 名称: Hemoglobin subunit beta / タイプ: protein_or_peptide / ID: 2 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 16.021396 KDa |
| 配列 | 文字列: MVHLTPEEKS AVTALWGKVN VDEVGGEALG RLLVVYPWTQ RFFESFGDLS TPDAVMGNPK VKAHGKKVLG AFSDGLAHLD NLKGTFATL SELHCDKLHV DPENFRLLGN VLVCVLAHHF GKEFTPPVQA AYQKVVAGVA NALAHKYH UniProtKB: Hemoglobin subunit beta |
-分子 #3: PROTOPORPHYRIN IX CONTAINING FE
| 分子 | 名称: PROTOPORPHYRIN IX CONTAINING FE / タイプ: ligand / ID: 3 / コピー数: 2 / 式: HEM |
|---|---|
| 分子量 | 理論値: 616.487 Da |
| Chemical component information |  ChemComp-HEM: |
-分子 #4: OXYGEN MOLECULE
| 分子 | 名称: OXYGEN MOLECULE / タイプ: ligand / ID: 4 / コピー数: 2 / 式: OXY |
|---|---|
| 分子量 | 理論値: 31.999 Da |
| Chemical component information |  ChemComp-O2: |
-分子 #5: water
| 分子 | 名称: water / タイプ: ligand / ID: 5 / コピー数: 123 / 式: HOH |
|---|---|
| 分子量 | 理論値: 18.015 Da |
| Chemical component information |  ChemComp-HOH: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.5 |
|---|---|
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: COPPER/RHODIUM / メッシュ: 300 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY |
| 凍結 | 凍結剤: ETHANE / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 特殊光学系 | エネルギーフィルター - 名称: GIF Bioquantum / エネルギーフィルター - スリット幅: 15 eV |
| 撮影 | フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) 平均電子線量: 60.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 1.2 µm / 最小 デフォーカス(公称値): 0.4 µm / 倍率(公称値): 165000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー




























 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)