+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-3611 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Full-length dodecameric S. typhimurium Wzz complex with associated dodecyl maltoside micelle. | |||||||||
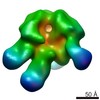
 マップデータ マップデータ | Wzz dodecamer with dodecyl maltoside micelle | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Wzz Polysaccharide Chain Length membrane protein Cryo-electron microscopy Single particle analysis / Membrane protein | |||||||||
| 機能・相同性 | Polysaccharide chain length determinant N-terminal domain / Chain length determinant protein / : / lipopolysaccharide biosynthetic process / plasma membrane / Chain length determinant protein 機能・相同性情報 機能・相同性情報 | |||||||||
| 生物種 |  | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 9.0 Å | |||||||||
 データ登録者 データ登録者 | Ford RC / Kargas V | |||||||||
 引用 引用 |  ジャーナル: Structure / 年: 2017 ジャーナル: Structure / 年: 2017タイトル: Full-length, Oligomeric Structure of Wzz Determined by Cryoelectron Microscopy Reveals Insights into Membrane-Bound States. 著者: Richard F Collins / Vasileios Kargas / Brad R Clarke / C Alistair Siebert / Daniel K Clare / Peter J Bond / Chris Whitfield / Robert C Ford /    要旨: Wzz is an integral inner membrane protein involved in regulating the length of lipopolysaccharide O-antigen glycans and essential for the virulence of many Gram-negative pathogens. In all Wzz ...Wzz is an integral inner membrane protein involved in regulating the length of lipopolysaccharide O-antigen glycans and essential for the virulence of many Gram-negative pathogens. In all Wzz homologs, the large periplasmic domain is proposed to be anchored by two transmembrane helices, but no information is available for the transmembrane and cytosolic domains. Here we have studied purified oligomeric Wzz complexes using cryoelectron microscopy and resolved the transmembrane regions within a semi-continuous detergent micelle. The transmembrane helices of each monomer display a right-handed super-helical twist, and do not interact with the neighboring transmembrane domains. Modeling, flexible fitting and multiscale simulation approaches were used to study the full-length complex and to provide explanations for the influence of the lipid bilayer on its oligomeric status. Based on structural and in silico observations, we propose a new mechanism for O-antigen chain-length regulation that invokes synergy of Wzz and its polymerase partner, Wzy. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_3611.map.gz emd_3611.map.gz | 8.3 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-3611-v30.xml emd-3611-v30.xml emd-3611.xml emd-3611.xml | 11.1 KB 11.1 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_3611.png emd_3611.png | 216 KB | ||
| Filedesc metadata |  emd-3611.cif.gz emd-3611.cif.gz | 5.4 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-3611 http://ftp.pdbj.org/pub/emdb/structures/EMD-3611 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-3611 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-3611 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_3611.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_3611.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Wzz dodecamer with dodecyl maltoside micelle | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.45 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Dodecameric complex
| 全体 | 名称: Dodecameric complex |
|---|---|
| 要素 |
|
-超分子 #1: Dodecameric complex
| 超分子 | 名称: Dodecameric complex / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 360 KDa |
-分子 #1: WzzB
| 分子 | 名称: WzzB / タイプ: protein_or_peptide / ID: 1 / コピー数: 12 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 26.760129 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: KWTSTAIITQ PDVGQIAGYN NAMNVIYGQA APKVSDLQET LIGRFSSAFS ALAETLDNQE EPEKLTIEPS VKNQQLPLTV SYVGQTAEG AQMKLAQYIQ QVDDKVNQEL ERDLKDNIAL GRKNLQDSLR TQEVVAQEQK DLRIRQIEEA LRYADEAKIT Q PQIQQTQD ...文字列: KWTSTAIITQ PDVGQIAGYN NAMNVIYGQA APKVSDLQET LIGRFSSAFS ALAETLDNQE EPEKLTIEPS VKNQQLPLTV SYVGQTAEG AQMKLAQYIQ QVDDKVNQEL ERDLKDNIAL GRKNLQDSLR TQEVVAQEQK DLRIRQIEEA LRYADEAKIT Q PQIQQTQD VTQDTMFLLG SDALKSMIQN EATRPLAFSP AYYQTKQTLL DIKNLKVTAD TVHVYRYVMK PTLPVRRDS |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.3 mg/mL |
|---|---|
| 緩衝液 | pH: 7.5 詳細: 20mM Tris pH 7.5, 150mM NaCl, 0.025% dodecyl maltoside. |
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: GOLD / メッシュ: 400 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY ARRAY / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 30 sec. / 前処理 - 雰囲気: AIR |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 95 % / チャンバー内温度: 293 K / 装置: FEI VITROBOT MARK III / 詳細: 1 x 4sec blot. |
| 詳細 | Dodecamers with C12 symmetry with a small fraction of head-to-head D12 complexes. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 平均電子線量: 2.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 初期モデル | モデルのタイプ: INSILICO MODEL |
|---|---|
| 最終 再構成 | 解像度のタイプ: BY AUTHOR / 解像度: 9.0 Å / 解像度の算出法: OTHER / 詳細: ResMap / 使用した粒子像数: 22000 |
| 初期 角度割当 | タイプ: ANGULAR RECONSTITUTION |
| 最終 角度割当 | タイプ: PROJECTION MATCHING |
 ムービー
ムービー コントローラー
コントローラー









 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)






















