+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-23995 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | CryoEM Structure of Full-Length mGlu2 Bound to Ago-PAM ADX55164 and Glutamate | |||||||||
 マップデータ マップデータ | CryoEM Map of Full-Length mGlu2 Bound to Ago-PAM ADX55164 and Glutamate | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Metabotropic Glutamate Receptor 2 (mGlu2) (mGluR2) / Family C G protein-coupled receptor (GPCR) / Heterotrimeric G protein / CryoEM structure / MEMBRANE PROTEIN / MEMBRANE PROTEIN-AGONIST complex | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報regulation of response to drug / group II metabotropic glutamate receptor activity / intracellular glutamate homeostasis / behavioral response to nicotine / negative regulation of adenylate cyclase activity / G protein-coupled glutamate receptor signaling pathway / glutamate secretion / Class C/3 (Metabotropic glutamate/pheromone receptors) / glutamate receptor activity / long-term synaptic depression ...regulation of response to drug / group II metabotropic glutamate receptor activity / intracellular glutamate homeostasis / behavioral response to nicotine / negative regulation of adenylate cyclase activity / G protein-coupled glutamate receptor signaling pathway / glutamate secretion / Class C/3 (Metabotropic glutamate/pheromone receptors) / glutamate receptor activity / long-term synaptic depression / regulation of glutamate secretion / astrocyte projection / cellular response to stress / regulation of dopamine secretion / regulation of synaptic transmission, glutamatergic / presynaptic modulation of chemical synaptic transmission / response to cocaine / calcium channel regulator activity / G protein-coupled receptor activity / presynaptic membrane / scaffold protein binding / G alpha (i) signalling events / gene expression / chemical synaptic transmission / postsynaptic membrane / positive regulation of phosphatidylinositol 3-kinase/protein kinase B signal transduction / axon / dendrite / glutamatergic synapse / plasma membrane 類似検索 - 分子機能 | |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.3 Å | |||||||||
 データ登録者 データ登録者 | Seven AB / Barros-Alvarez X | |||||||||
| 資金援助 |  米国, 1件 米国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nature / 年: 2021 ジャーナル: Nature / 年: 2021タイトル: G-protein activation by a metabotropic glutamate receptor. 著者: Alpay B Seven / Ximena Barros-Álvarez / Marine de Lapeyrière / Makaía M Papasergi-Scott / Michael J Robertson / Chensong Zhang / Robert M Nwokonko / Yang Gao / Justin G Meyerowitz / Jean- ...著者: Alpay B Seven / Ximena Barros-Álvarez / Marine de Lapeyrière / Makaía M Papasergi-Scott / Michael J Robertson / Chensong Zhang / Robert M Nwokonko / Yang Gao / Justin G Meyerowitz / Jean-Philippe Rocher / Dominik Schelshorn / Brian K Kobilka / Jesper M Mathiesen / Georgios Skiniotis /    要旨: Family C G-protein-coupled receptors (GPCRs) operate as obligate dimers with extracellular domains that recognize small ligands, leading to G-protein activation on the transmembrane (TM) domains of ...Family C G-protein-coupled receptors (GPCRs) operate as obligate dimers with extracellular domains that recognize small ligands, leading to G-protein activation on the transmembrane (TM) domains of these receptors by an unknown mechanism. Here we show structures of homodimers of the family C metabotropic glutamate receptor 2 (mGlu2) in distinct functional states and in complex with heterotrimeric G. Upon activation of the extracellular domain, the two transmembrane domains undergo extensive rearrangement in relative orientation to establish an asymmetric TM6-TM6 interface that promotes conformational changes in the cytoplasmic domain of one protomer. Nucleotide-bound G can be observed pre-coupled to inactive mGlu2, but its transition to the nucleotide-free form seems to depend on establishing the active-state TM6-TM6 interface. In contrast to family A and B GPCRs, G-protein coupling does not involve the cytoplasmic opening of TM6 but is facilitated through the coordination of intracellular loops 2 and 3, as well as a critical contribution from the C terminus of the receptor. The findings highlight the synergy of global and local conformational transitions to facilitate a new mode of G-protein activation. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_23995.map.gz emd_23995.map.gz | 296.3 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-23995-v30.xml emd-23995-v30.xml emd-23995.xml emd-23995.xml | 21.3 KB 21.3 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_23995.png emd_23995.png | 98.2 KB | ||
| Filedesc metadata |  emd-23995.cif.gz emd-23995.cif.gz | 7.4 KB | ||
| その他 |  emd_23995_additional_1.map.gz emd_23995_additional_1.map.gz | 320.5 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-23995 http://ftp.pdbj.org/pub/emdb/structures/EMD-23995 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-23995 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-23995 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  7mtrMC  7mtqC  7mtsC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | |
| 電子顕微鏡画像生データ |  EMPIAR-10978 (タイトル: CryoEM Structure of Full-Length mGlu2 Bound to Ago-PAM ADX55164 and Glutamate EMPIAR-10978 (タイトル: CryoEM Structure of Full-Length mGlu2 Bound to Ago-PAM ADX55164 and GlutamateData size: 3.5 TB Data #1: Unaligned multi-frame micrographs of Full-Length mGlu2 Bound to Ago-PAM ADX55164 and Glutamate [micrographs - multiframe]) |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_23995.map.gz / 形式: CCP4 / 大きさ: 343 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_23995.map.gz / 形式: CCP4 / 大きさ: 343 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | CryoEM Map of Full-Length mGlu2 Bound to Ago-PAM ADX55164 and Glutamate | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
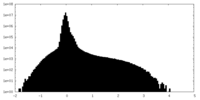
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.8677 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-追加マップ: Local and focused refinement of mGlu2 CRD and 7TM domains
| ファイル | emd_23995_additional_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Local and focused refinement of mGlu2 CRD and 7TM domains | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Full-length mGlu2 in ago-PAM and L-Glutamate bound-state
| 全体 | 名称: Full-length mGlu2 in ago-PAM and L-Glutamate bound-state |
|---|---|
| 要素 |
|
-超分子 #1: Full-length mGlu2 in ago-PAM and L-Glutamate bound-state
| 超分子 | 名称: Full-length mGlu2 in ago-PAM and L-Glutamate bound-state タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 詳細: Metabotropic glutamate receptor 2 bound to ago-PAM ADX55164 and L-Glutamate |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 191 KDa |
-分子 #1: Metabotropic glutamate receptor 2
| 分子 | 名称: Metabotropic glutamate receptor 2 / タイプ: protein_or_peptide / ID: 1 / コピー数: 2 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 93.932445 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: AEGPAKKVLT LEGDLVLGGL FPVHQKGGPA EDCGPVNEHR GIQRLEAMLF ALDRINRDPH LLPGVRLGAH ILDSCSKDTH ALEQALDFV RASLSRGADG SRHICPDGSY ATHGDAPTAI TGVIGGSYSD VSIQVANLLR LFQIPQISYA STSAKLSDKS R YDYFARTV ...文字列: AEGPAKKVLT LEGDLVLGGL FPVHQKGGPA EDCGPVNEHR GIQRLEAMLF ALDRINRDPH LLPGVRLGAH ILDSCSKDTH ALEQALDFV RASLSRGADG SRHICPDGSY ATHGDAPTAI TGVIGGSYSD VSIQVANLLR LFQIPQISYA STSAKLSDKS R YDYFARTV PPDFFQAKAM AEILRFFNWT YVSTVASEGD YGETGIEAFE LEARARNICV ATSEKVGRAM SRAAFEGVVR AL LQKPSAR VAVLFTRSED ARELLAASQR LNASFTWVAS DGWGALESVV AGSEGAAEGA ITIELASYPI SDFASYFQSL DPW NNSRNP WFREFWEQRF RCSFRQRDCA AHSLRAVPFE QESKIMFVVN AVYAMAHALH NMHRALCPNT TRLCDAMRPV NGRR LYKDF VLNVKFDAPF RPADTHNEVR FDRFGDGIGR YNIFTYLRAG SGRYRYQKVG YWAEGLTLDT SLIPWASPSA GPLPA SRCS EPCLQNEVKS VQPGEVCCWL CIPCQPYEYR LDEFTCADCG LGYWPNASLT GCFELPQEYI RWGDAWAVGP VTIACL GAL ATLFVLGVFV RHNATPVVKA SGRELCYILL GGVFLCYCMT FIFIAKPSTA VCTLRRLGLG TAFSVCYSAL LTKTNRI AR IFGGAREGAQ RPRFISPASQ VAICLALISG QLLIVVAWLV VEAPGTGKET APERREVVTL RCNHRDASML GSLAYNVL L IALCTLYAFK TRKCPENFNE AKFIGFTMYT TCIIWLAFLP IFYVTSSDYR VQTTTMCVSV SLSGSVVLGC LFAPKLHII LFQPQKNVVS HRAPTSRFGS AAARASSSLG QGSGSQFVPT VCNGREVVDS TTSSL UniProtKB: Metabotropic glutamate receptor 2 |
-分子 #2: GLUTAMIC ACID
| 分子 | 名称: GLUTAMIC ACID / タイプ: ligand / ID: 2 / コピー数: 2 / 式: GLU |
|---|---|
| 分子量 | 理論値: 147.129 Da |
| Chemical component information | 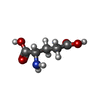 ChemComp-GLU: |
-分子 #3: 2-acetamido-2-deoxy-beta-D-glucopyranose
| 分子 | 名称: 2-acetamido-2-deoxy-beta-D-glucopyranose / タイプ: ligand / ID: 3 / コピー数: 2 / 式: NAG |
|---|---|
| 分子量 | 理論値: 221.208 Da |
| Chemical component information |  ChemComp-NAG: |
-分子 #4: 2-methoxy-6-propyl-N-(2-{4-[(1H-tetrazol-5-yl)methoxy]phenyl}ethy...
| 分子 | 名称: 2-methoxy-6-propyl-N-(2-{4-[(1H-tetrazol-5-yl)methoxy]phenyl}ethyl)thieno[2,3-d]pyrimidin-4-amine タイプ: ligand / ID: 4 / コピー数: 1 / 式: ZQY |
|---|---|
| 分子量 | 理論値: 425.507 Da |
| Chemical component information | 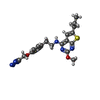 ChemComp-ZQY: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.5 |
|---|---|
| グリッド | モデル: Quantifoil R1.2/1.3 / 支持フィルム - 材質: GOLD / 支持フィルム - トポロジー: HOLEY |
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) 平均電子線量: 1.3 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 50.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.0 µm / 最小 デフォーカス(公称値): 1.0 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー











 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)