+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-11820 | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
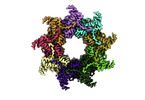
| タイトル | Nonameric cytoplasmic domain of SctV from Yersinia enterocolitica | ||||||||||||
 マップデータ マップデータ | Structure of the SctV cytoplasmic domain | ||||||||||||
 試料 試料 |
| ||||||||||||
 キーワード キーワード | T3SS / export apparatus / secretion / protein export / PROTEIN TRANSPORT | ||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報 | ||||||||||||
| 生物種 |  Yersinia enterocolitica (腸炎エルシニア) Yersinia enterocolitica (腸炎エルシニア) | ||||||||||||
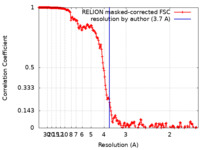
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.7 Å | ||||||||||||
 データ登録者 データ登録者 | Kuhlen L / Johnson S | ||||||||||||
| 資金援助 |  英国, 3件 英国, 3件
| ||||||||||||
 引用 引用 |  ジャーナル: PLoS One / 年: 2021 ジャーナル: PLoS One / 年: 2021タイトル: Nonameric structures of the cytoplasmic domain of FlhA and SctV in the context of the full-length protein. 著者: Lucas Kuhlen / Steven Johnson / Jerry Cao / Justin C Deme / Susan M Lea /   要旨: Type three secretion is the mechanism of protein secretion found in bacterial flagella and injectisomes. At its centre is the export apparatus (EA), a complex of five membrane proteins through which ...Type three secretion is the mechanism of protein secretion found in bacterial flagella and injectisomes. At its centre is the export apparatus (EA), a complex of five membrane proteins through which secretion substrates pass the inner membrane. While the complex formed by four of the EA proteins has been well characterised structurally, little is known about the structure of the membrane domain of the largest subunit, FlhA in flagella, SctV in injectisomes. Furthermore, the biologically relevant nonameric assembly of FlhA/SctV has been infrequently observed and differences in conformation of the cytoplasmic portion of FlhA/SctV between open and closed states have been suggested to reflect secretion system specific differences. FlhA has been shown to bind to chaperone-substrate complexes in an open state, but in previous assembled ring structures, SctV is in a closed state. Here, we identify FlhA and SctV homologues that can be recombinantly produced in the oligomeric state and study them using cryo-electron microscopy. The structures of the cytoplasmic domains from both FlhA and SctV are in the open state and we observe a conserved interaction between a short stretch of residues at the N-terminus of the cytoplasmic domain, known as FlhAL/SctVL, with a groove on the adjacent protomer's cytoplasmic domain, which stabilises the nonameric ring assembly. | ||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_11820.map.gz emd_11820.map.gz | 478.2 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-11820-v30.xml emd-11820-v30.xml emd-11820.xml emd-11820.xml | 15.2 KB 15.2 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_11820_fsc.xml emd_11820_fsc.xml | 18.1 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_11820.png emd_11820.png | 165.4 KB | ||
| マスクデータ |  emd_11820_msk_1.map emd_11820_msk_1.map | 512 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-11820.cif.gz emd-11820.cif.gz | 5.7 KB | ||
| その他 |  emd_11820_half_map_1.map.gz emd_11820_half_map_1.map.gz emd_11820_half_map_2.map.gz emd_11820_half_map_2.map.gz | 410.6 MB 410.8 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-11820 http://ftp.pdbj.org/pub/emdb/structures/EMD-11820 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-11820 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-11820 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_11820_validation.pdf.gz emd_11820_validation.pdf.gz | 1.1 MB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_11820_full_validation.pdf.gz emd_11820_full_validation.pdf.gz | 1.1 MB | 表示 | |
| XML形式データ |  emd_11820_validation.xml.gz emd_11820_validation.xml.gz | 26.1 KB | 表示 | |
| CIF形式データ |  emd_11820_validation.cif.gz emd_11820_validation.cif.gz | 34.6 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-11820 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-11820 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-11820 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-11820 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_11820.map.gz / 形式: CCP4 / 大きさ: 512 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_11820.map.gz / 形式: CCP4 / 大きさ: 512 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Structure of the SctV cytoplasmic domain | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.822 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-マスク #1
| ファイル |  emd_11820_msk_1.map emd_11820_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
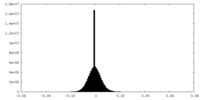
| 密度ヒストグラム |
-ハーフマップ: half map 2
| ファイル | emd_11820_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | half map 2 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
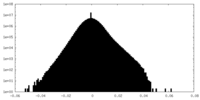
| 密度ヒストグラム |
-ハーフマップ: half map 1
| ファイル | emd_11820_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | half map 1 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
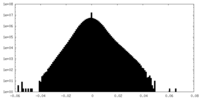
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Double nonamer of the SctV cytoplasmic domain from Yersinia enter...
| 全体 | 名称: Double nonamer of the SctV cytoplasmic domain from Yersinia enterocolitica |
|---|---|
| 要素 |
|
-超分子 #1: Double nonamer of the SctV cytoplasmic domain from Yersinia enter...
| 超分子 | 名称: Double nonamer of the SctV cytoplasmic domain from Yersinia enterocolitica タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  Yersinia enterocolitica (腸炎エルシニア) Yersinia enterocolitica (腸炎エルシニア) |
| 分子量 | 理論値: 1.4 MDa |
-分子 #1: Low calcium response protein
| 分子 | 名称: Low calcium response protein / タイプ: protein_or_peptide / ID: 1 / コピー数: 18 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Yersinia enterocolitica (腸炎エルシニア) Yersinia enterocolitica (腸炎エルシニア) |
| 分子量 | 理論値: 78.667281 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MNPHDLEWLN RIGERKDIML AVLLLAVVFM MVLPLPPIVL DILIAVNMTI SVVLLMIAIY INSPLQFSAF PAVLLVTTLF RLALSVSTT RMILLQADAG QIVYTFGNFV VGGNLIVGIV IFLIITIVQF LVITKGSERV AEVSARFSLD AMPGKQMSID G DMRAGVID ...文字列: MNPHDLEWLN RIGERKDIML AVLLLAVVFM MVLPLPPIVL DILIAVNMTI SVVLLMIAIY INSPLQFSAF PAVLLVTTLF RLALSVSTT RMILLQADAG QIVYTFGNFV VGGNLIVGIV IFLIITIVQF LVITKGSERV AEVSARFSLD AMPGKQMSID G DMRAGVID VNEARERRAT IEKESQMFGS MDGAMKFVKG DAIAGLIIIF VNILGGVTIG VTQKGLAAAE ALQLYSILTV GD GMVSQVP ALLIAITAGI IVTRVSSEDS SDLGSDIGKQ VVAQPKAMLI GGVLLLLFGL IPGFPTVTFL ILALLVGCGG YML SRKQSR NDEANQDLQS ILTSGSGAPA ARTKAKTSGA NKGRLGEQEA FAMTVPLLID VDSSQQEALE AIALNDELVR VRRA LYLDL GVPFPGIHLR FNEGMGEGEY LISLQEVPVA RGELKAGYLL VRESVSQLEL LGIPYEKGEH LLPDQETFWV SVEYE ERLE KSQLEFFSHS QVLTWHLSHV LREYAEDFIG IQETRYLLEQ MEGGYGELIK EVQRIVPLQR MTEILQRLVG EDISIR NMR SILEAMVEWG QKEKDVVQLT EYIRSSLKRY ICYKYANGNN ILPAYLFDQE VEEKIRSGVR QTSAGSYLAL DPAVTES LL EQVRKTIGDL SQIQSKPVLI VSMDIRRYVR KLIESEYYGL PVLSYQELTQ QINIQPLGRV CLENLYFQ UniProtKB: Low calcium response protein |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 8 |
|---|---|
| グリッド | モデル: Quantifoil / 前処理 - タイプ: GLOW DISCHARGE |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 平均電子線量: 48.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー











 Z
Z Y
Y X
X