+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-0272 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | F97L Hepatitis B core protein capsid | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報microtubule-dependent intracellular transport of viral material towards nucleus / T=4 icosahedral viral capsid / viral penetration into host nucleus / host cell / host cell cytoplasm / symbiont entry into host cell / structural molecule activity / DNA binding / RNA binding 類似検索 - 分子機能 | |||||||||
| 生物種 |   Hepatitis B virus (B 型肝炎ウイルス) Hepatitis B virus (B 型肝炎ウイルス) | |||||||||
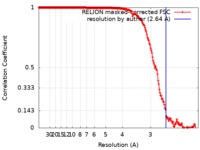
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.64 Å | |||||||||
 データ登録者 データ登録者 | Bottcher B / Nassal M | |||||||||
| 資金援助 |  ドイツ, 1件 ドイツ, 1件
| |||||||||
 引用 引用 |  ジャーナル: J Mol Biol / 年: 2018 ジャーナル: J Mol Biol / 年: 2018タイトル: Structure of Mutant Hepatitis B Core Protein Capsids with Premature Secretion Phenotype. 著者: Bettina Böttcher / Michael Nassal /  要旨: Hepatitis B virus is a major human pathogen that consists of a viral genome surrounded by an icosahedrally ordered core protein and a polymorphic, lipidic envelope that is densely packed with surface ...Hepatitis B virus is a major human pathogen that consists of a viral genome surrounded by an icosahedrally ordered core protein and a polymorphic, lipidic envelope that is densely packed with surface proteins. A point mutation in the core protein in which a phenylalanine at position 97 is exchanged for a smaller leucine leads to premature envelopment of the capsid before the genome maturation is fully completed. We have used electron cryo-microscopy and image processing to investigate how the point mutation affects the structure of the capsid at 2.6- to 2.8 Å-resolution. We found that in the mutant the smaller side chain at position 97 is displaced, increasing the size of an adjacent pocket in the center of the spikes of the capsid. In the mutant, this pocket is filled with an unknown density. Phosphorylation of serine residues in the unresolved C-terminal domain of the mutant leaves the structure of the ordered capsid largely unchanged. However, we were able to resolve several previously unresolved residues downstream of proline 144 that precede the phosphorylation-sites. These residues pack against the neighboring subunits and increase the inter-dimer contact suggesting that the C-termini play an important role in capsid stabilization and provide a much larger interaction interface than previously observed. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_0272.map.gz emd_0272.map.gz | 480.4 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-0272-v30.xml emd-0272-v30.xml emd-0272.xml emd-0272.xml | 19.7 KB 19.7 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_0272_fsc.xml emd_0272_fsc.xml | 18 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_0272.png emd_0272.png | 428.5 KB | ||
| マスクデータ |  emd_0272_msk_1.map emd_0272_msk_1.map | 512 MB |  マスクマップ マスクマップ | |
| その他 |  emd_0272_half_map_1.map.gz emd_0272_half_map_1.map.gz emd_0272_half_map_2.map.gz emd_0272_half_map_2.map.gz | 409.1 MB 409.2 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-0272 http://ftp.pdbj.org/pub/emdb/structures/EMD-0272 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-0272 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-0272 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_0272_validation.pdf.gz emd_0272_validation.pdf.gz | 418.7 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_0272_full_validation.pdf.gz emd_0272_full_validation.pdf.gz | 417.8 KB | 表示 | |
| XML形式データ |  emd_0272_validation.xml.gz emd_0272_validation.xml.gz | 23.3 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0272 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0272 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0272 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-0272 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_0272.map.gz / 形式: CCP4 / 大きさ: 512 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_0272.map.gz / 形式: CCP4 / 大きさ: 512 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.053 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
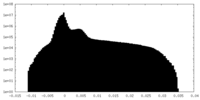
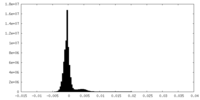
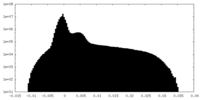
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-マスク #1
| ファイル |  emd_0272_msk_1.map emd_0272_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
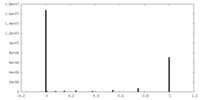
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_0272_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
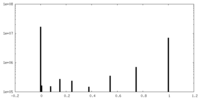
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_0272_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
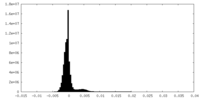
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Hepatitis B virus
| 全体 | 名称:   Hepatitis B virus (B 型肝炎ウイルス) Hepatitis B virus (B 型肝炎ウイルス) |
|---|---|
| 要素 |
|
-超分子 #1: Hepatitis B virus
| 超分子 | 名称: Hepatitis B virus / タイプ: virus / ID: 1 / 親要素: 0 / 含まれる分子: all / NCBI-ID: 10407 / 生物種: Hepatitis B virus / ウイルスタイプ: VIRUS-LIKE PARTICLE / ウイルス・単離状態: STRAIN / ウイルス・エンベロープ: No / ウイルス・中空状態: No |
|---|---|
| 宿主 | 生物種:   Hepatitis B virus (B 型肝炎ウイルス) / 株: ayw Hepatitis B virus (B 型肝炎ウイルス) / 株: ayw |
| Host system | 生物種:  |
| 分子量 | 理論値: 4.8 MDa |
| ウイルス殻 | Shell ID: 1 / 名称: WT Hbc / 直径: 340.0 Å / T番号(三角分割数): 4 |
-分子 #1: Capsid protein
| 分子 | 名称: Capsid protein / タイプ: protein_or_peptide / ID: 1 詳細: Hepatitis B core protein premature envelopment mutant F97L コピー数: 8 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:   Hepatitis B virus (B 型肝炎ウイルス) Hepatitis B virus (B 型肝炎ウイルス) |
| 分子量 | 理論値: 21.112199 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MDIDPYKEFG ATVELLSFLP SDFFPSVRDL LDTASALYRE ALESPEHCSP HHTALRQAIL CWGELMTLAT WVGVNLEDPA SRDLVVSYV NTNMGLKLRQ LLWFHISCLT FGRETVIEYL VSFGVWIRTP PAYRPPNAPI LSTLPETTVV RRRGRSPRRR T PSPRRRRS QSPRRRRSQS RESQC |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 5 mg/mL | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.7 構成要素:
詳細: 25 mM Tris pH 7.7, 150 mM NaCl | |||||||||
| グリッド | モデル: Quantifoil, UltrAuFoil, R1.2/1.3 / 材質: GOLD / メッシュ: 300 / 支持フィルム - トポロジー: HOLEY ARRAY / 支持フィルム - Film thickness: 50.0 nm / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 雰囲気: AIR | |||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 4 K / 装置: FEI VITROBOT MARK IV 詳細: Samples were vitrified with an FEI Vitrobot IV, which was operated at 100% humidity at 4C. 2.5-3.5 ul of sample were applied to grids (Quantifoil UltrAuFoil R1.3/1.2 300 mesh gold grids ) ...詳細: Samples were vitrified with an FEI Vitrobot IV, which was operated at 100% humidity at 4C. 2.5-3.5 ul of sample were applied to grids (Quantifoil UltrAuFoil R1.3/1.2 300 mesh gold grids ) that were glow discharged in air for 1-2 min. The sample was incubated for 30 s before blotting for 3 s with a blot force between 0 and 5.. | |||||||||
| 詳細 | sample is purified from e.coli via sucrose density gradient. sucrose is removed via buffer exchange on a concentrator |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 特殊光学系 | エネルギーフィルター - 名称: GIF Quantum LS / エネルギーフィルター - スリット幅: 20 eV |
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: COUNTING / デジタル化 - 画像ごとのフレーム数: 1-28 / 撮影したグリッド数: 1 / 実像数: 1948 / 平均電子線量: 28.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 70.0 µm / 最大 デフォーカス(補正後): 2.56 µm / 最小 デフォーカス(補正後): 0.37 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 倍率(公称値): 75000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー




















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)