+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-6393 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Structural basis for TBC-DEG assembly with TBCC and soluble tubulin dimer | |||||||||
 マップデータ マップデータ | Reconstruction of TBC-DEG:TBCC:tubulin complex | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Tubulin cofactors / Microtubule dynamics / Chaperones / tubulin biogenesis or degradation / tubulin dimer / TBC-DEG / TBCC | |||||||||
| 生物種 |  | |||||||||
| 手法 | 単粒子再構成法 / ネガティブ染色法 / 解像度: 24.0 Å | |||||||||
 データ登録者 データ登録者 | Nithianantham S / Le S / Seto E / Jia W / Leary J / Corbett KD / Moore JK / Al-Bassam J | |||||||||
 引用 引用 |  ジャーナル: Elife / 年: 2015 ジャーナル: Elife / 年: 2015タイトル: Tubulin cofactors and Arl2 are cage-like chaperones that regulate the soluble αβ-tubulin pool for microtubule dynamics. 著者: Stanley Nithianantham / Sinh Le / Elbert Seto / Weitao Jia / Julie Leary / Kevin D Corbett / Jeffrey K Moore / Jawdat Al-Bassam /  要旨: Microtubule dynamics and polarity stem from the polymerization of αβ-tubulin heterodimers. Five conserved tubulin cofactors/chaperones and the Arl2 GTPase regulate α- and β-tubulin assembly into ...Microtubule dynamics and polarity stem from the polymerization of αβ-tubulin heterodimers. Five conserved tubulin cofactors/chaperones and the Arl2 GTPase regulate α- and β-tubulin assembly into heterodimers and maintain the soluble tubulin pool in the cytoplasm, but their physical mechanisms are unknown. Here, we reconstitute a core tubulin chaperone consisting of tubulin cofactors TBCD, TBCE, and Arl2, and reveal a cage-like structure for regulating αβ-tubulin. Biochemical assays and electron microscopy structures of multiple intermediates show the sequential binding of αβ-tubulin dimer followed by tubulin cofactor TBCC onto this chaperone, forming a ternary complex in which Arl2 GTP hydrolysis is activated to alter αβ-tubulin conformation. A GTP-state locked Arl2 mutant inhibits ternary complex dissociation in vitro and causes severe defects in microtubule dynamics in vivo. Our studies suggest a revised paradigm for tubulin cofactors and Arl2 functions as a catalytic chaperone that regulates soluble αβ-tubulin assembly and maintenance to support microtubule dynamics. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_6393.map.gz emd_6393.map.gz | 7.2 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-6393-v30.xml emd-6393-v30.xml emd-6393.xml emd-6393.xml | 13.3 KB 13.3 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  400_6393.gif 400_6393.gif 80_6393.gif 80_6393.gif | 24.9 KB 3.4 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-6393 http://ftp.pdbj.org/pub/emdb/structures/EMD-6393 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-6393 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-6393 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_6393_validation.pdf.gz emd_6393_validation.pdf.gz | 78.2 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_6393_full_validation.pdf.gz emd_6393_full_validation.pdf.gz | 77.3 KB | 表示 | |
| XML形式データ |  emd_6393_validation.xml.gz emd_6393_validation.xml.gz | 495 B | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-6393 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-6393 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-6393 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-6393 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  6390C  6391C  6392C  5cyaC C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | |
| 電子顕微鏡画像生データ |  EMPIAR-10034 (タイトル: Tubulin Chaperone complexes TBC-DEG Q73L: alpha beta-tubulin:TBCC complex EMPIAR-10034 (タイトル: Tubulin Chaperone complexes TBC-DEG Q73L: alpha beta-tubulin:TBCC complexData size: 1.0 Data #1: CTF-corrected particle images of tubulin chaperone complexes TBC-DEG Q73L: alpha beta-tubulin:TBCC complex [picked particles - multiframe - processed]) |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_6393.map.gz / 形式: CCP4 / 大きさ: 7.8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_6393.map.gz / 形式: CCP4 / 大きさ: 7.8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Reconstruction of TBC-DEG:TBCC:tubulin complex | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 2 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
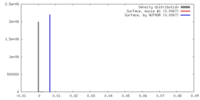
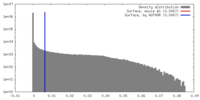
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Tubulin cofactor complex (TBC-DEG) with TBCC and tubulin dimer
| 全体 | 名称: Tubulin cofactor complex (TBC-DEG) with TBCC and tubulin dimer |
|---|---|
| 要素 |
|
-超分子 #1000: Tubulin cofactor complex (TBC-DEG) with TBCC and tubulin dimer
| 超分子 | 名称: Tubulin cofactor complex (TBC-DEG) with TBCC and tubulin dimer タイプ: sample / ID: 1000 詳細: TBC-DEG:TBCC:tubulin complex behaves as a single biochemical entity. 集合状態: One heterotrimer of TBC-DEG binds to TBCC and tubulin dimer Number unique components: 6 |
|---|---|
| 分子量 | 実験値: 340 KDa / 理論値: 345 KDa / 手法: SEC-MALS |
-分子 #1: tubulin folding cofactor D
| 分子 | 名称: tubulin folding cofactor D / タイプ: protein_or_peptide / ID: 1 / Name.synonym: TBCD / コピー数: 1 / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  |
| 組換発現 | 生物種:  |
-分子 #2: tubulin folding cofactor E
| 分子 | 名称: tubulin folding cofactor E / タイプ: protein_or_peptide / ID: 2 / Name.synonym: TBCE / コピー数: 1 / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  |
| 組換発現 | 生物種:  |
-分子 #3: ARL2 GTPase, Q73L mutant
| 分子 | 名称: ARL2 GTPase, Q73L mutant / タイプ: protein_or_peptide / ID: 3 / Name.synonym: DEG(Q73L) / 詳細: Arl2 locked mutant (Q73L) in a GTP-like state / コピー数: 1 / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  |
| 組換発現 | 生物種:  |
-分子 #4: tubulin binding cofactor C
| 分子 | 名称: tubulin binding cofactor C / タイプ: protein_or_peptide / ID: 4 / Name.synonym: TBCC / コピー数: 1 / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  |
| 組換発現 | 生物種:  |
-分子 #5: alpha tubulin
| 分子 | 名称: alpha tubulin / タイプ: protein_or_peptide / ID: 5 / 組換発現: No / データベース: NCBI |
|---|---|
| 由来(天然) | 生物種: unidentified (未定義) |
-分子 #6: beta tubulin
| 分子 | 名称: beta tubulin / タイプ: protein_or_peptide / ID: 6 / 組換発現: No / データベース: NCBI |
|---|---|
| 由来(天然) | 生物種: unidentified (未定義) |
-実験情報
-構造解析
| 手法 | ネガティブ染色法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.5 mg/mL |
|---|---|
| 緩衝液 | pH: 7 詳細: 50 mM HEPES, 100 mM KCl, 0.1 mM GTP, 3 mM b-mercaptoethanol |
| 染色 | タイプ: NEGATIVE 詳細: The proteins were incubated on carbon-coated grids, briefly washed, and stained with 1% uranyl formate. |
| グリッド | 詳細: glow-discharged 200 mesh gold grid with thin carbon support |
| 凍結 | 凍結剤: NONE / 装置: OTHER |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | JEOL 2100F |
|---|---|
| 日付 | 2014年7月25日 |
| 撮影 | カテゴリ: FILM / フィルム・検出器のモデル: KODAK SO-163 FILM / デジタル化 - スキャナー: PRIMESCAN / デジタル化 - サンプリング間隔: 3.7 µm / 実像数: 100 / 平均電子線量: 9 e/Å2 / ビット/ピクセル: 5 |
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 倍率(補正後): 50050 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.7 µm / 最小 デフォーカス(公称値): 1.1 µm / 倍率(公称値): 50000 |
| 試料ステージ | 試料ホルダーモデル: JEOL |
- 画像解析
画像解析
| 詳細 | TBC-DEG:TBCC:tubulin complex particles were picked semi-automatically using e2boxer.py. |
|---|---|
| CTF補正 | 詳細: Each particle |
| 最終 再構成 | アルゴリズム: OTHER / 解像度のタイプ: BY AUTHOR / 解像度: 24.0 Å / 解像度の算出法: OTHER / ソフトウェア - 名称: Spider, EMAN2 / 使用した粒子像数: 19500 |
| 最終 2次元分類 | クラス数: 400 |
 ムービー
ムービー コントローラー
コントローラー










 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)