+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-9834 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Structure of RyR2 (F/A/C/L-Ca2+/apo-CaM-M dataset) | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | cryo-EM / MEMBRANE PROTEIN | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報: / negative regulation of calcium-mediated signaling / negative regulation of insulin secretion involved in cellular response to glucose stimulus / neuronal action potential propagation / insulin secretion involved in cellular response to glucose stimulus / negative regulation of release of sequestered calcium ion into cytosol / response to redox state / CaM pathway / Cam-PDE 1 activation / Sodium/Calcium exchangers ...: / negative regulation of calcium-mediated signaling / negative regulation of insulin secretion involved in cellular response to glucose stimulus / neuronal action potential propagation / insulin secretion involved in cellular response to glucose stimulus / negative regulation of release of sequestered calcium ion into cytosol / response to redox state / CaM pathway / Cam-PDE 1 activation / Sodium/Calcium exchangers / Calmodulin induced events / negative regulation of heart rate / Reduction of cytosolic Ca++ levels / 'de novo' protein folding / Activation of Ca-permeable Kainate Receptor / CREB1 phosphorylation through the activation of CaMKII/CaMKK/CaMKIV cascasde / Loss of phosphorylation of MECP2 at T308 / CREB1 phosphorylation through the activation of Adenylate Cyclase / negative regulation of high voltage-gated calcium channel activity / PKA activation / CaMK IV-mediated phosphorylation of CREB / Glycogen breakdown (glycogenolysis) / CLEC7A (Dectin-1) induces NFAT activation / FK506 binding / Activation of RAC1 downstream of NMDARs / negative regulation of ryanodine-sensitive calcium-release channel activity / organelle localization by membrane tethering / mitochondrion-endoplasmic reticulum membrane tethering / autophagosome membrane docking / negative regulation of calcium ion export across plasma membrane / regulation of ryanodine-sensitive calcium-release channel activity / regulation of cardiac muscle cell action potential / presynaptic endocytosis / Synthesis of IP3 and IP4 in the cytosol / Phase 0 - rapid depolarisation / Negative regulation of NMDA receptor-mediated neuronal transmission / Unblocking of NMDA receptors, glutamate binding and activation / RHO GTPases activate PAKs / calcineurin-mediated signaling / regulation of cell communication by electrical coupling involved in cardiac conduction / Ion transport by P-type ATPases / smooth muscle contraction / Uptake and function of anthrax toxins / protein phosphatase activator activity / Long-term potentiation / Calcineurin activates NFAT / Regulation of MECP2 expression and activity / DARPP-32 events / T cell proliferation / Smooth Muscle Contraction / detection of calcium ion / regulation of cardiac muscle contraction / catalytic complex / RHO GTPases activate IQGAPs / calcium channel inhibitor activity / presynaptic cytosol / Activation of AMPK downstream of NMDARs / cellular response to interferon-beta / Protein methylation / Ion homeostasis / regulation of release of sequestered calcium ion into cytosol by sarcoplasmic reticulum / eNOS activation / Tetrahydrobiopterin (BH4) synthesis, recycling, salvage and regulation / titin binding / regulation of calcium-mediated signaling / release of sequestered calcium ion into cytosol / regulation of cardiac muscle contraction by regulation of the release of sequestered calcium ion / voltage-gated potassium channel complex / FCERI mediated Ca+2 mobilization / sarcoplasmic reticulum membrane / calcium channel complex / substantia nigra development / FCGR3A-mediated IL10 synthesis / regulation of heart rate / Antigen activates B Cell Receptor (BCR) leading to generation of second messengers / Ras activation upon Ca2+ influx through NMDA receptor / calyx of Held / adenylate cyclase activator activity / VEGFR2 mediated cell proliferation / VEGFR2 mediated vascular permeability / regulation of cytokinesis / protein serine/threonine kinase activator activity / sarcomere / spindle microtubule / peptidylprolyl isomerase / positive regulation of receptor signaling pathway via JAK-STAT / peptidyl-prolyl cis-trans isomerase activity / Translocation of SLC2A4 (GLUT4) to the plasma membrane / calcium channel regulator activity / calcium-mediated signaling / Transcriptional activation of mitochondrial biogenesis / RAF activation / protein maturation / response to calcium ion / cellular response to type II interferon / G2/M transition of mitotic cell cycle / Stimuli-sensing channels / Z disc / spindle pole / Signaling by RAF1 mutants 類似検索 - 分子機能 | |||||||||
| 生物種 |   Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 4.2 Å | |||||||||
 データ登録者 データ登録者 | Gong DS / Chi XM | |||||||||
 引用 引用 |  ジャーナル: Nature / 年: 2019 ジャーナル: Nature / 年: 2019タイトル: Modulation of cardiac ryanodine receptor 2 by calmodulin. 著者: Deshun Gong / Ximin Chi / Jinhong Wei / Gewei Zhou / Gaoxingyu Huang / Lin Zhang / Ruiwu Wang / Jianlin Lei / S R Wayne Chen / Nieng Yan /    要旨: The high-conductance intracellular calcium (Ca) channel RyR2 is essential for the coupling of excitation and contraction in cardiac muscle. Among various modulators, calmodulin (CaM) regulates RyR2 ...The high-conductance intracellular calcium (Ca) channel RyR2 is essential for the coupling of excitation and contraction in cardiac muscle. Among various modulators, calmodulin (CaM) regulates RyR2 in a Ca-dependent manner. Here we reveal the regulatory mechanism by which porcine RyR2 is modulated by human CaM through the structural determination of RyR2 under eight conditions. Apo-CaM and Ca-CaM bind to distinct but overlapping sites in an elongated cleft formed by the handle, helical and central domains. The shift in CaM-binding sites on RyR2 is controlled by Ca binding to CaM, rather than to RyR2. Ca-CaM induces rotations and intradomain shifts of individual central domains, resulting in pore closure of the PCB95 and Ca-activated channel. By contrast, the pore of the ATP, caffeine and Ca-activated channel remains open in the presence of Ca-CaM, which suggests that Ca-CaM is one of the many competing modulators of RyR2 gating. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_9834.map.gz emd_9834.map.gz | 226.4 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-9834-v30.xml emd-9834-v30.xml emd-9834.xml emd-9834.xml | 17.3 KB 17.3 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_9834_fsc.xml emd_9834_fsc.xml | 14.1 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_9834.png emd_9834.png | 211 KB | ||
| Filedesc metadata |  emd-9834.cif.gz emd-9834.cif.gz | 9 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-9834 http://ftp.pdbj.org/pub/emdb/structures/EMD-9834 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-9834 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-9834 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  6jiiMC  9831C  9833C  9836C  9837C  9879C  9880C  9889C  6ji0C  6ji8C  6jiuC  6jiyC  6jrrC  6jrsC  6jv2C M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_9834.map.gz / 形式: CCP4 / 大きさ: 244.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_9834.map.gz / 形式: CCP4 / 大きさ: 244.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.091 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : RyR2 in complex with FKBP12.6 and apo-Calmodulin-mimicking mutant
| 全体 | 名称: RyR2 in complex with FKBP12.6 and apo-Calmodulin-mimicking mutant |
|---|---|
| 要素 |
|
-超分子 #1: RyR2 in complex with FKBP12.6 and apo-Calmodulin-mimicking mutant
| 超分子 | 名称: RyR2 in complex with FKBP12.6 and apo-Calmodulin-mimicking mutant タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1-#3 |
|---|---|
| 由来(天然) | 生物種:  |
-分子 #1: Peptidyl-prolyl cis-trans isomerase FKBP1B
| 分子 | 名称: Peptidyl-prolyl cis-trans isomerase FKBP1B / タイプ: protein_or_peptide / ID: 1 / コピー数: 4 / 光学異性体: LEVO / EC番号: peptidylprolyl isomerase |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 11.798501 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MGVEIETISP GDGRTFPKKG QTCVVHYTGM LQNGKKFDSS RDRNKPFKFR IGKQEVIKGF EEGAAQMSLG QRAKLTCTPD VAYGATGHP GVIPPNATLI FDVELLNLE UniProtKB: Peptidyl-prolyl cis-trans isomerase FKBP1B |
-分子 #2: Ryr2
| 分子 | 名称: Ryr2 / タイプ: protein_or_peptide / ID: 2 / コピー数: 4 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 564.905625 KDa |
| 配列 | 文字列: MADGGEGEDE IQFLRTDDEV VLQCTATIHK EQQKLCLAAE GFGNRLCFLE STSNSKNVPP DLSICTFVLE QSLSVRALQE MLANTVEKS EGQVDVEKWK FMMKTAQGGG HRTLLYGHAI LLRHSYSGMY LCCLSTSRSS TDKLAFDVGL QEDTTGEACW W TIHPASKQ ...文字列: MADGGEGEDE IQFLRTDDEV VLQCTATIHK EQQKLCLAAE GFGNRLCFLE STSNSKNVPP DLSICTFVLE QSLSVRALQE MLANTVEKS EGQVDVEKWK FMMKTAQGGG HRTLLYGHAI LLRHSYSGMY LCCLSTSRSS TDKLAFDVGL QEDTTGEACW W TIHPASKQ RSEGEKVRVG DDLILVSVSS ERYLHLSYGN VSLHVDAAFQ QTLWSVAPIS SGSEAAQGYL IGGDVLRLLH GH MDECLTV PSGEHGEEQR RTVHYEGGAV SVHARSLWRL ETLRVAWSGS HIRWGQPFRL RHVTTGKYLS LMEDKSLLLM DKE KADVKS TAFTFRSSKE KLDVGVRKEV DGMGTSEIKY GDSVCFIQHI GTGLWLTYQS VDVKSVRMGS IQRKAIMHHE GHMD DGLNL SRSQHEESRT ARVIRSTVFL FNRFIRGLDA LSKKAKASTV DLPIESVSLS LQDLIGYFHP PDEHLEHEDK QNRLR ALKN RQNLFQEEGM INLVLECIDR LHVYSSAAHF ADVAGREAGE SWKSILNSLY ELLAALIRGN RKNCAQFSGS LDWLIS RLE RLEASSGILE VLHCVLVESP EALNIIKEGH IKSIISLLDK HGRNHKVLDV LCSLCVCHGV AVRSNQHLIC DNLLPGR DL LLQTRLVNHV SSMRPNIFLG VSEGSAQYKK WYYELMVDHT EPFVTAEATH LRVGWASTEG YSPYPGGGEE WGGNGVGD D LFSYGFDGLH LWSGCIARTV SSPNQHLLRT DDVISCCLDL SAPSISFRIN GQPVQGMFEN FNIDGLFFPV VSFSAGIKV RFLLGGRHGE FKFLPPPGYA PCYEAVLPKE KLKVEHSREY KQERTYTRDL LGPTVSLTQA AFTPIPVDTS QIVLPPHLER IREKLAENI HELWVMNKIE LGWQYGPVRD DNKRQHPCLV EFSKLPEQER NYNLQMSLET LKTLLALGCH VGISDEHAEE K VKKMKLPK NYQLTSGYKP APMDLSFIKL TPSQEAMVDK LAENAHNVWA RDRIRQGWTY GIQQDVKNRR NPRLVPYALL DD RTKKSNK DSLREAVRTL LGYGYNLEAP DQDHAARAEV CSGTGERFRI FRAEKTYAVK AGRWYFEFEA VTAGDMRVGW SRP GCQPDQ ELGSDERAFA FDGFKAQRWH QGNEHYGRSW QAGDVVGCMV DMTEHTMMFT LNGEILLDDS GSELAFKDFD VGDG FIPVC SLGVAQVGRM NFGKDVSTLK YFTICGLQEG YEPFAVNTNR DITMWLSKRL PQFLQVPSSH EHIEVTRIDG TIDSS PCLK VTQKSFGSQN SSTDIMFYRL SMPIECAEVF SKTSAGGIPG ASLFGPKNDL EDYDADSDFE VLMKTAHGHL VPDRVD KDK EATKPEFNNH KDYAQEKPSR LKQRFLLRRT KPDYSTSHSA RLTEDVLADD RDDYDYLMQT STYYYSVRIF PGQEPAN VW VGWITSDFHQ YDTAFDLDRV RTVTVTLGDE KGKVHESIKR SNCYMVCAGE SMSPGQGRNN NGLEIGCVVD AASGLLTF T ANGKDLSTYY QVEPSTKLFP AVFAQATSPN VFQFELGRIK NVMPLSAGLF KSEHKNPVPQ CPPRLHVQFL SHVLWSRMP NQFLKVDVSR ISERQGWLVQ CLEPLQFMSL HIPEENRSVD ILELTEQEEL LKFHYHTLRL YSAVCALGNH RVAHALCSHV DEPQLLYAI ENKYMPGLLR AGYYDLLIDI HLSSYATARL MMNNEFIVPM TEETKSITLF PDENKKHGLP GIGLSTSLRP R MQFSSPSF VSINNECYQY SPEFPLDILK AKTIQMLTEA VQEGSLHARD PVGGTTEFLF VPLIKLFYTL LIMGIFHNED LK HILQLIE PSVFKEAAGP EEESDTLEKE PCASEDSRLE GPAEEESKGG KRPKEGLLQM KLPEPVKLQM CLLLQYLCDC QVR HRIEAI VAFSDDFVAK LQDNQRFRYN EVMQALNMSA ALTARKTKEF RSPPQEQINM LLNFKDDKSE CPCPEEIRDQ LLDF HEDLM THCGIELDED GSLDGNSDLT IRGRLLSLVE KVTYLKKKQA EKLVESDSKK SSTLQQLISE TMVRWAQESV IEDPE LVRA MFVLLHRQYD GIGGLVRALP KTYTINGVSV EDTINLLASL GQIRSLLSVR MGKEEEKLMI RGLGDIMNNK VFYQHP NLM RALGMHETVM EVMVNVLGGG ESKEITFPKM VANCCRFLCY FCRISRQNQK AMFDHLSYLL ENSSVGLASP AMRGSTP LD VAAASVMDNN ELALALREPD LEKVVRYLAG CGLQSCQMLV SKGYPDIGWN PVEGERYLDF LRFAVFCNGE SVEENANV V VRLLIRRPEC FGPALRGEGG NGLLAAMEEA IKIAEDPSRD GPSPTSGSSK MPDTEGEEDD TIHMGNAIMT FYAALIDLL GRCAPEMHLI HAAKGEAIRI RSILRSLIPL GDLVGVISIA FQMPTIAKDG NVVEPDMSAG FCPDHKAAMV LFLDRVYGIE VQDFLLHLL EVGFLPDLRA AASLDTAALS ATDMALALNR YLCTAVLPLL TRCAPLFAGT EHHASLIDSL LHTVYRLSKG C SLTKAQRD SIEVCLLSIC GQLRPSMMQH LLRRLVFDVP LLNEHAKMPL KLLTNHYERC WKYYCLPGGW GNFGAASEEE LH LSRKLFW GIFDALSQKK YEQELFKLAL PCLSAVAGAL PPDYMESNYV SMMEKQSSMD SEGNFNPQPV DTSNITIPEK LEY FINKYA EHSHDKWSMD KLANGWIYGE IYSDSSKVQP LMKPYKLLSE KEKEIYRWPI KESLKTMLAW GWRIERTREG DSMA LYNRT RRISQTSQVS VDAAHGYSPR AIDMSNVTLS RDLHAMAEMM AENYHNIWAK KKKLELESKG GGNHPLLVPY DTLTA KEKA KDREKAQDIL KFLQINGYAV SRGFKDLELD TPSIEKRFAY SFLQQLIRYV DEAHQYILEF DGGSRSKGEH FPYEQE IKF FAKVVLPLID QYFKNHRLYF LSAASRPLCS GGHASNKEKE MVTSLFCKLG VLVRHRISLF GNDATSIVNC LHILGQT LD ARTVMKTGLE SVKSALRAFL DNAAEDLEKT MENLKQGQFT HTRNQPKGVT QIINYTTVAL LPMLSSLFEH IGQHQFGE D LILEDVQVSC YRILTSLYAL GTSKSIYVER QRSALGECLA AFAGAFPVAF LETHLDKHNI YSIYNTKSSR ERAALNLPT NVEDVCPNIP SLEKLMEEIV DLAESGIRYT QMPHVMEVVL PMLCSYMSRW WEHGPENNPG RAEMCCTALN SEHMNTLLGN ILKIIYNNL GIDEGAWMKR LAVFSQPIIN KVKPQLLKTH FLPLMEKLKK KAAMVVSEED HLKSEVRGDM SEAELLILDE F TTLARDLY AFYPLLIRFV DYNRAKWLKE PNPEAEDLFR MVAEVFIYWS KSHNFKREEQ NFVVQNEINN MSFLITDTKS KM SKAAVSD QERKKMKRKG DRYSMQTSLI VAALKRLLPI GLNICAPGDQ ELIALAKNRF SLKDTEDEVR DIIRSNIHLQ GKL EDPAIR WQMALYKDLP NRTEDTSDPE KTVERVLDIA NVLFHLEQKS TCMRRRYYSL VEHPQRSKKA VWHKLLSKQR KRAV VACFR MAPLYNLPRH RAVNLFLQGY EKSWIETEEH YFEDKLIEDL AKPGAVPPEE DEGTKRVDPL HQLILLFSRT ALTEK CKLE EDFLYMAYAD IMAKSCHDEE DDDGEEEVKS FEEKEMEKQK LLYQQARLHD RGAAEMVLQT ISASKGETGP MVAATL KLG IAILNGGNST VQQKMLEYLK EKKDVGFFQS LAGLMQSCSV LDLNAFERQN KAEGLGMVTE EGSGEKVLQD DEFTCDL FR FLQLLCEGHN SDFQNYLRTQ TGNNTTVNII ISTVDYLLRV QESISDFYWY YSGKDVIDEQ GQRNFSKAIQ VAKQVFNT L TEYIQGPCTG NQQSLAHSRL WDAVVGFLHV FAHMQMKLSQ DSSQIELLKE LMDLQKDMVV MLLSMLEGNV VNGTIGKQM VDMLVESSNN VEMILKFFDM FLKLKDLTSS DTFKEYDPDG KGVISKRDFH KAMESHKHYT QSETEFLLSC AETDENETLD YEEFVKRFH EPAKDIGFNV AVLLTNLSEH MPNDTRLQTF LELAESVLNY FQPFLGRIEI MGSAKRIERV YFEISESSRT Q WEKPQVKE SKRQFIFDVV NEGGEKEKME LFVNFCEDTI FEMQLAAQIS ESDLNERSAN KEESEKEKPE EQGPRMGFFS LV TVRSALL ALRYNVLTLM RMLSLKSLKK QMKKVKKMTV RDMVTAFFTS YWSVFMTLLH FAASVSRGFS RIIGGLLLGG SLV EGAKKI KVAELLANMP DPTQDEVRGD GDEGERKVLE GTLPSEDLTD LKELTEESDL LSDIFGLDLK REGGQYKLIP HNPN AGLSD LMSSPAPIPE VQEKFQEQKA KEEEKEEKEE NKSEPEKAEG EDGEKEEKAK EDKGKQKLRQ LHTHRYGEPE VPESA FWKK IIAYQQKLLN YFARNFYNMR MLALFVAFAI NFILLFYKVS TSSVVEGKEL PTRSSSENAN FGSLDSSSPR IIAVHY VLE ESSGYMEPTL RILAILHTVI SFFCIIGYYC LKVPLVIFKR EKEVARKLEF DGLYITEQPS EDDIKGQWDR LVINTQS FP NNYWDKFVKR KVMDKYGEFY GRDRISELLG MDKAALDFSD AREKKKPKKD SSLSAVLNSI DVKYQMWKLG VVFTDNSF L YLAWYMTMSV LGHYNNFFFA AHLLDIAMGF KTLRTILSSV THNGKQLVLT VGLLAVVVYL YTVVAFNFFR KFYNKSEDG DTPDMKCDDM LTCYMFHMYV GVRAGGGIGD EIEDPAGDEY EIYRIIFDIT FFFFVIVILL AIIQGLIIDA FGELRDQQEQ VKEDMETKC FICGIGNDYF DTVPHGFETH TLQEHNLANY LFFLMYLINK DETEHTGQES YVWKMYQERC WEFFPAGDCF R KQYEDQLN |
-分子 #3: Calmodulin-1
| 分子 | 名称: Calmodulin-1 / タイプ: protein_or_peptide / ID: 3 / コピー数: 4 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 16.620402 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MADQLTEEQI AEFKEAFSLF DKDGDGTITT KALGTVMRSL GQNPTEAELQ DMINEVDADG NGTIDFPAFL TMMARKMKDT DSEEEIREA FRVFDKDGNG YISAAALRHV MTNLGEKLTD EEVDEMIREA DIDGDGQVNY EAFVQMMTAK UniProtKB: Calmodulin-1 |
-分子 #4: ZINC ION
| 分子 | 名称: ZINC ION / タイプ: ligand / ID: 4 / コピー数: 4 / 式: ZN |
|---|---|
| 分子量 | 理論値: 65.409 Da |
-分子 #5: CALCIUM ION
| 分子 | 名称: CALCIUM ION / タイプ: ligand / ID: 5 / コピー数: 4 / 式: CA |
|---|---|
| 分子量 | 理論値: 40.078 Da |
-分子 #6: CAFFEINE
| 分子 | 名称: CAFFEINE / タイプ: ligand / ID: 6 / コピー数: 4 / 式: CFF |
|---|---|
| 分子量 | 理論値: 194.191 Da |
| Chemical component information | 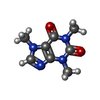 ChemComp-CFF: |
-分子 #7: ADENOSINE-5'-TRIPHOSPHATE
| 分子 | 名称: ADENOSINE-5'-TRIPHOSPHATE / タイプ: ligand / ID: 7 / コピー数: 4 / 式: ATP |
|---|---|
| 分子量 | 理論値: 507.181 Da |
| Chemical component information |  ChemComp-ATP: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.4 |
|---|---|
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 平均電子線量: 50.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー




























 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)






















