+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-8898 | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Clostridioides difficileC toxinB with DLD-4 darpin | ||||||||||||
 マップデータ マップデータ | Clostridioides difficileC toxinB with DLD-4 darpin | ||||||||||||
 試料 試料 |
| ||||||||||||
 キーワード キーワード | TOXIN-PROTEIN BINDING complex | ||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報symbiont-mediated perturbation of host actin cytoskeleton via filamentous actin depolymerization / glucosyltransferase activity / 転移酵素; グリコシル基を移すもの; 六炭糖残基を移すもの / host cell cytosol / cysteine-type peptidase activity / host cell endosome membrane / toxin activity / 加水分解酵素; プロテアーゼ; ペプチド結合加水分解酵素; システインプロテアーゼ / lipid binding / host cell plasma membrane ...symbiont-mediated perturbation of host actin cytoskeleton via filamentous actin depolymerization / glucosyltransferase activity / 転移酵素; グリコシル基を移すもの; 六炭糖残基を移すもの / host cell cytosol / cysteine-type peptidase activity / host cell endosome membrane / toxin activity / 加水分解酵素; プロテアーゼ; ペプチド結合加水分解酵素; システインプロテアーゼ / lipid binding / host cell plasma membrane / proteolysis / extracellular region / metal ion binding 類似検索 - 分子機能 | ||||||||||||
| 生物種 |  Clostridioides difficile (バクテリア) / Clostridioides difficile (バクテリア) /  | ||||||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 9.0 Å | ||||||||||||
 データ登録者 データ登録者 | Zhang J / Jiang M | ||||||||||||
| 資金援助 |  米国, 3件 米国, 3件
| ||||||||||||
 引用 引用 |  ジャーナル: PLoS Biol / 年: 2019 ジャーナル: PLoS Biol / 年: 2019タイトル: Selection and characterization of ultrahigh potency designed ankyrin repeat protein inhibitors of C. difficile toxin B. 著者: Rudo Simeon / Mengqiu Jiang / Ana M Chamoun-Emanuelli / Hua Yu / Yongrong Zhang / Ran Meng / Zeyu Peng / Joanita Jakana / Junjie Zhang / Hanping Feng / Zhilei Chen /  要旨: Clostridium difficile infection (CDI) is a major nosocomial disease associated with significant morbidity and mortality. The pathology of CDI stems primarily from the 2 C. difficile-secreted ...Clostridium difficile infection (CDI) is a major nosocomial disease associated with significant morbidity and mortality. The pathology of CDI stems primarily from the 2 C. difficile-secreted exotoxins-toxin A (TcdA) and toxin B (TcdB)-that disrupt the tight junctions between epithelial cells leading to the loss of colonic epithelial barrier function. Here, we report the engineering of a series of monomeric and dimeric designed ankyrin repeat proteins (DARPins) for the neutralization of TcdB. The best dimeric DARPin, DLD-4, inhibited TcdB with a half maximal effective concentration (EC50) of 4 pM in vitro, representing an approximately 330-fold higher potency than the Food and Drug Administration (FDA)-approved anti-TcdB monoclonal antibody bezlotoxumab in the same assay. DLD-4 also protected mice from a toxin challenge in vivo. Cryo-electron microscopy (cryo-EM) studies revealed that the 2 constituent DARPins of DLD-4-1.4E and U3-bind the central and C-terminal regions of the delivery domain of TcdB. Competitive enzyme-linked immunosorbent assay (ELISA) studies showed that the DARPins 1.4E and U3 interfere with the interaction between TcdB and its receptors chondroitin sulfate proteoglycan 4 (CSPG4) and frizzled class receptor 2 (FZD2), respectively. Our cryo-EM studies revealed a new conformation of TcdB (both apo- and DARPin-bound at pH 7.4) in which the combined repetitive oligopeptides (CROPS) domain points away from the delivery domain. This conformation of the CROPS domain is in stark contrast to that seen in the negative-stain electron microscopy (EM) structure of TcdA and TcdB at the same pH, in which the CROPS domain bends toward and "kisses" the delivery domain. The ultrapotent anti-TcdB molecules from this study serve as candidate starting points for CDI drug development and provide new biological tools for studying the pathogenicity of C. difficile. The structural insights regarding both the "native" conformation of TcdB and the putative sites of TcdB interaction with the FZD2 receptor, in particular, should help accelerate the development of next-generation anti-C. difficile toxin therapeutics. | ||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_8898.map.gz emd_8898.map.gz | 479.2 KB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-8898-v30.xml emd-8898-v30.xml emd-8898.xml emd-8898.xml | 12.8 KB 12.8 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_8898.png emd_8898.png | 36.7 KB | ||
| Filedesc metadata |  emd-8898.cif.gz emd-8898.cif.gz | 6.2 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-8898 http://ftp.pdbj.org/pub/emdb/structures/EMD-8898 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-8898 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-8898 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_8898.map.gz / 形式: CCP4 / 大きさ: 4.8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_8898.map.gz / 形式: CCP4 / 大きさ: 4.8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Clostridioides difficileC toxinB with DLD-4 darpin | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 3 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
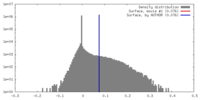
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : ternary complex of tcdB and DLD-4 darpin
| 全体 | 名称: ternary complex of tcdB and DLD-4 darpin |
|---|---|
| 要素 |
|
-超分子 #1: ternary complex of tcdB and DLD-4 darpin
| 超分子 | 名称: ternary complex of tcdB and DLD-4 darpin / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  Clostridioides difficile (バクテリア) Clostridioides difficile (バクテリア) |
-分子 #1: Toxin B
| 分子 | 名称: Toxin B / タイプ: protein_or_peptide / ID: 1 / コピー数: 1 / 光学異性体: LEVO EC番号: 加水分解酵素; プロテアーゼ; ペプチド結合加水分解酵素; システインプロテアーゼ |
|---|---|
| 由来(天然) | 生物種:  Clostridioides difficile (バクテリア) Clostridioides difficile (バクテリア) |
| 分子量 | 理論値: 235.481438 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: VNRKQLEKMA NVRFRTQEDE YVAILDALEE YHNMSENTVV EKYLKLKDIN SLTDIYIDTY KKSGRNKALK KFKEYLVTEV LELKNNNLT PVEKNLHFVW IGGQINDTAI NYINQWKDVN SDYNVNVFYD SNAFLINTLK KTVVESAIND TLESFRENLN D PRFDYNKF ...文字列: VNRKQLEKMA NVRFRTQEDE YVAILDALEE YHNMSENTVV EKYLKLKDIN SLTDIYIDTY KKSGRNKALK KFKEYLVTEV LELKNNNLT PVEKNLHFVW IGGQINDTAI NYINQWKDVN SDYNVNVFYD SNAFLINTLK KTVVESAIND TLESFRENLN D PRFDYNKF FRKRMEIIYD KQKNFINYYK AQREENPELI IDDIVKTYLS NEYSKEIDEL NTYIEESLNK ITQNSGNDVR NF EEFKNGE SFNLYEQELV ERWNLAAASD ILRISALKEI GGMYLDVDML PGIQPDLFES IEKPSSVTVD FWEMTKLEAI MKY KEYIPE YTSEHFDMLD EEVQSSFESV LASKSDKSEI FSSLGDMEAS PLEVKIAFNS KGIINQGLIS VKDSYCSNLI VKQI ENRYK ILNNSLNPAI SEDNDFNTTT NTFIDSIMAE ANADNGRFMM ELGKYLRVGF FPDVKTTINL SGPEAYAAAY QDLLM FKEG SMNIHLIEAD LRNFEISKTN ISQSTEQEMA SLWSFDDARA KAQFEEYKRN YFEGSLGEDD NLDFSQNIVV DKEYLL EKI SSLARSSERG YIHYIVQLQG DKISYEAACN LFAKTPYDSV LFQKNIEDSE IAYYYNPGDG EIQEIDKYKI PSIISDR PK IKLTFIGHGK DEFNTDIFAG FDVDSLSTEI EAAIDLAKED ISPKSIEINL LGCNMFSYSI NVEETYPGKL LLKVKDKI S ELMPSISQDS IIVSANQYEV RINSEGRREL LDHSGEWINK EESIIKDISS KEYISFNPKE NKITVKSKNL PELSTLLQE IRNNSNSSDI ELEEKVMLTE CEINVISNID TQIVEERIEE AKNLTSDSIN YIKDEFKLIE SISDALCDLK QQNELEDSHF ISFEDISET DEGFSIRFIN KETGESIFVE TEKTIFSEYA NHITEEISKI KGTIFDTVNG KLVKKVNLDT THEVNTLNAA F FIQSLIEY NSSKESLSNL SVAMKVQVYA QLFSTGLNTI TDAAKVVELV STALDETIDL LPTLSEGLPI IATIIDGVSL GA AIKELSE TSDPLLRQEI EAKIGIMAVN LTTATTAIIT SSLGIASGFS ILLVPLAGIS AGIPSLVNNE LVLRDKATKV VDY FKHVSL VETEGVFTLL DDKIMMPQDD LVISEIDFNN NSIVLGKCEI WRMEGGSGHT VTDDIDHFFS APSITYREPH LSIY DVLEV QKEELDLSKD LMVLPNAPNR VFAWETGWTP GLRSLENDGT KLLDRIRDNY EGEFYWRYFA FIADALITTL KPRYE DTNI RINLDSNTRS FIVPIITTEY IREKLSYSFY GSGGTYALSL SQYNMGINIE LSESDVWIID VDNVVRDVTI ESDKIK KGD LIEGILSTLS IEENKIILNS HEINFSGEVN GSNGFVSLTF SILEGINAII EVDLLSKSYK LLISGELKIL MLNSNHI QQ KIDYIGFNSE LQKNIPYSFV DSEGKENGFI NGSTKEGLFV SELPDVVLIS KVYMDDSKPS FGYYSNNLKD VKVITKDN V NILTGYYLKD DIKISLSLTL QDEKTIKLNS VHLDESGVAE ILKFMNRKGN TNTSDSLMSF LESMNIKSIF VNFLQSNIK FILDANFIIS GTTSIGQFEF ICDENDNIQP YFIKFNTLET NYTLYVGNRQ NMIVEPNYDL DDSGDISSTV INFSQKYLYG IDSCVNKVV ISPNIYTDEI NITPVYETNN TYPEVIVLDA NYINEKINVN INDLSIRYVW SNDGNDFILM STSEENKVSQ V KIRFVNVF KDKTLANKLS FNFSDKQDVP VSEIILSFGL IYINDSLYYF KPPVNNLITG FVTVGDDKYY FNPINGGAAS IG ETIIDDK NYYFNQSGVL QTGVFSTEDG FKYFAPANTL DENLEGEAID FTGKLIIDEN IYYFDDNYRG AVEWKELDGE MHY FSPETG KAFKGLNQIG DYKYYFNSDG VMQKGFVSIN DNKHYFDDSG VMKVGYTEID GKHFYFAENG EMQIGVFNTE DGFK YFAHH NEDLGNEEGE EISYSGILNF NNKIYYFDDS FTAVVGWKDL EDGSKYYFDE DTAEAYILEH HH UniProtKB: Toxin B, Toxin B |
-分子 #2: DLD-4 darpin
| 分子 | 名称: DLD-4 darpin / タイプ: protein_or_peptide / ID: 2 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 34.299195 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: SDLGKKLLEA ARAGQDDEVR ILMANGADVN ADDRIGMTPL HLAAIGGHLE IVEVLLKNGA DVNADDVHGR TPLHLAAGRG HLEIVEVLH GADVNAPDRW GRTPLHLAAH HGHLEIVEVL LKYGADVNAQ DKFGKTAFDI SIDSGNEDLA EILQSSSEFG G GGSGGGGS ...文字列: SDLGKKLLEA ARAGQDDEVR ILMANGADVN ADDRIGMTPL HLAAIGGHLE IVEVLLKNGA DVNADDVHGR TPLHLAAGRG HLEIVEVLH GADVNAPDRW GRTPLHLAAH HGHLEIVEVL LKYGADVNAQ DKFGKTAFDI SIDSGNEDLA EILQSSSEFG G GGSGGGGS GGGGSASDLG KKLLEAARAG QDDEVRILMA NGADVNATDH LGVTPLHLAA VLGHLEIVEV LLKHGADVNA YD ILGRTPL HLAAWRGHLE IVEVLLKYGA DVNADDTSGT TPLHLAAGEG HLEIVEVLLK YGADVNAQDK FGKTAFDISI DNG NEDLAE IL |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.4 |
|---|---|
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法 #1
電子顕微鏡法 #1
| Microscopy ID | 1 |
|---|---|
| 顕微鏡 | JEOL 3200FSC |
| 撮影 | Image recording ID: 1 フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 平均電子線量: 30.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD |
- 電子顕微鏡法 #1~
電子顕微鏡法 #1~
| Microscopy ID | 1 |
|---|---|
| 顕微鏡 | FEI TECNAI F20 |
| 撮影 | Image recording ID: 2 フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 平均電子線量: 30.0 e/Å2 |
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD |
| 実験機器 |  モデル: Tecnai F20 / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)