+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-4118 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | CryoEM structure of the membrane pore complex of Pneumolysin at 4.5A | |||||||||
 マップデータ マップデータ | PLY pore complex | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Bacterial toxins / pore complex / cryoEM structure / cholesterol-dependent cytolysin / Pneumolysin / membrane pore / TOXIN | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報cholesterol binding / toxin activity / killing of cells of another organism / host cell plasma membrane / extracellular region / membrane 類似検索 - 分子機能 | |||||||||
| 生物種 |   Streptococcus pneumoniae serotype 2 (strain D39 / NCTC 7466) (肺炎レンサ球菌) Streptococcus pneumoniae serotype 2 (strain D39 / NCTC 7466) (肺炎レンサ球菌) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 4.5 Å | |||||||||
 データ登録者 データ登録者 | van Pee K / Neuhaus A | |||||||||
| 資金援助 |  ドイツ, 1件 ドイツ, 1件
| |||||||||
 引用 引用 |  ジャーナル: Elife / 年: 2017 ジャーナル: Elife / 年: 2017タイトル: CryoEM structures of membrane pore and prepore complex reveal cytolytic mechanism of Pneumolysin. 著者: Katharina van Pee / Alexander Neuhaus / Edoardo D'Imprima / Deryck J Mills / Werner Kühlbrandt / Özkan Yildiz /  要旨: Many pathogenic bacteria produce pore-forming toxins to attack and kill human cells. We have determined the 4.5 Å structure of the ~2.2 MDa pore complex of pneumolysin, the main virulence factor of ...Many pathogenic bacteria produce pore-forming toxins to attack and kill human cells. We have determined the 4.5 Å structure of the ~2.2 MDa pore complex of pneumolysin, the main virulence factor of , by cryoEM. The pneumolysin pore is a 400 Å ring of 42 membrane-inserted monomers. Domain 3 of the soluble toxin refolds into two ~85 Å β-hairpins that traverse the lipid bilayer and assemble into a 168-strand β-barrel. The pore complex is stabilized by salt bridges between β-hairpins of adjacent subunits and an internal α-barrel. The apolar outer barrel surface with large sidechains is immersed in the lipid bilayer, while the inner barrel surface is highly charged. Comparison of the cryoEM pore complex to the prepore structure obtained by electron cryo-tomography and the x-ray structure of the soluble form reveals the detailed mechanisms by which the toxin monomers insert into the lipid bilayer to perforate the target membrane. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_4118.map.gz emd_4118.map.gz | 19.1 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-4118-v30.xml emd-4118-v30.xml emd-4118.xml emd-4118.xml | 11.3 KB 11.3 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
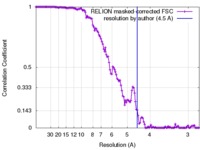
| FSC (解像度算出) |  emd_4118_fsc.xml emd_4118_fsc.xml | 12.4 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_4118.png emd_4118.png | 148.8 KB | ||
| Filedesc metadata |  emd-4118.cif.gz emd-4118.cif.gz | 5.4 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-4118 http://ftp.pdbj.org/pub/emdb/structures/EMD-4118 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-4118 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-4118 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_4118_validation.pdf.gz emd_4118_validation.pdf.gz | 265.1 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_4118_full_validation.pdf.gz emd_4118_full_validation.pdf.gz | 264.2 KB | 表示 | |
| XML形式データ |  emd_4118_validation.xml.gz emd_4118_validation.xml.gz | 12.4 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-4118 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-4118 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-4118 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-4118 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_4118.map.gz / 形式: CCP4 / 大きさ: 178 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_4118.map.gz / 形式: CCP4 / 大きさ: 178 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | PLY pore complex | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.4 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Pneumolysin pore complex
| 全体 | 名称: Pneumolysin pore complex |
|---|---|
| 要素 |
|
-超分子 #1: Pneumolysin pore complex
| 超分子 | 名称: Pneumolysin pore complex / タイプ: organelle_or_cellular_component / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 2.2 MDa |
-分子 #1: Pneumolysin
| 分子 | 名称: Pneumolysin / タイプ: protein_or_peptide / ID: 1 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Streptococcus pneumoniae serotype 2 (strain D39 / NCTC 7466) (肺炎レンサ球菌) Streptococcus pneumoniae serotype 2 (strain D39 / NCTC 7466) (肺炎レンサ球菌) |
| 分子量 | 理論値: 52.866066 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MANKAVNDFI LAMNYDKKKL LTHQGESIEN RFIKEGNQLP DEFVVIERKK RSLSTNTSDI SVTATNDSRL YPGALLVVDE TLLENNPTL LAVDRAPMTY SIDLPGLASS DSFLQVEDPS NSSVRGAVND LLAKWHQDYG QVNNVPARMQ YEKITAHSME Q LKVKFGSD ...文字列: MANKAVNDFI LAMNYDKKKL LTHQGESIEN RFIKEGNQLP DEFVVIERKK RSLSTNTSDI SVTATNDSRL YPGALLVVDE TLLENNPTL LAVDRAPMTY SIDLPGLASS DSFLQVEDPS NSSVRGAVND LLAKWHQDYG QVNNVPARMQ YEKITAHSME Q LKVKFGSD FEKAANSLDI DFNAVHSGEK QIQIVNFKQI YYTVSVDAVK NPGDVFQDTV TVEDLKQRGI SAERPLVYIS SV AYGRQVY LKLETTSKSD EVQAAFEAAI LGVKVAPQTQ WKQILDNTEV KAVILGGDPS SGARVVTGKV DMVEDLIQEG SRF TADHPG LPISYTTSFL RDNVVATFQN STDYVETKVT AYRNGDLLLD HSGAYVAQYY ITWDELSYDH QGKEVLTPKA WDRN GQDLT AHFTTSIPLK GNVRNLSVKI RECTGLAWEW WRTVYEKTDL PLVRKRTISI WGTTLYPQVE DKVEND UniProtKB: Pneumolysin |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 1 mg/mL |
|---|---|
| 緩衝液 | pH: 7 |
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI POLARA 300 |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: COUNTING / 平均露光時間: 6.0 sec. / 平均電子線量: 1.02 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD |
| 実験機器 |  モデル: Tecnai Polara / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー








 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)