+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-3668 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Closed dimer (C2) of human ATM (Ataxia telangiectasia mutated) | |||||||||
 マップデータ マップデータ | Closed dimer (C2) of human ATM (Ataxia telangiectasia mutated) | |||||||||
 試料 試料 |
| |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
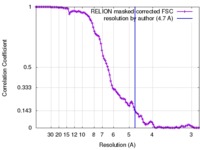
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 4.7 Å | |||||||||
 データ登録者 データ登録者 | Baretic D / Johnson CM / Santhanam B / Truman CM / Kouba T / Fersht AR / Phillips C / Williams RL / Pollard HK / Fisher DI | |||||||||
 引用 引用 |  ジャーナル: Sci Adv / 年: 2017 ジャーナル: Sci Adv / 年: 2017タイトル: Structures of closed and open conformations of dimeric human ATM. 著者: Domagoj Baretić / Hannah K Pollard / David I Fisher / Christopher M Johnson / Balaji Santhanam / Caroline M Truman / Tomas Kouba / Alan R Fersht / Christopher Phillips / Roger L Williams /  要旨: ATM (ataxia-telangiectasia mutated) is a phosphatidylinositol 3-kinase-related protein kinase (PIKK) best known for its role in DNA damage response. ATM also functions in oxidative stress response, ...ATM (ataxia-telangiectasia mutated) is a phosphatidylinositol 3-kinase-related protein kinase (PIKK) best known for its role in DNA damage response. ATM also functions in oxidative stress response, insulin signaling, and neurogenesis. Our electron cryomicroscopy (cryo-EM) suggests that human ATM is in a dynamic equilibrium between closed and open dimers. In the closed state, the PIKK regulatory domain blocks the peptide substrate-binding site, suggesting that this conformation may represent an inactive or basally active enzyme. The active site is held in this closed conformation by interaction with a long helical hairpin in the TRD3 (tetratricopeptide repeats domain 3) domain of the symmetry-related molecule. The open dimer has two protomers with only a limited contact interface, and it lacks the intermolecular interactions that block the peptide-binding site in the closed dimer. This suggests that the open conformation may be more active. The ATM structure shows the detailed topology of the regulator-interacting N-terminal helical solenoid. The ATM conformational dynamics shown by the structures represent an important step in understanding the enzyme regulation. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_3668.map.gz emd_3668.map.gz | 93.8 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-3668-v30.xml emd-3668-v30.xml emd-3668.xml emd-3668.xml | 20.4 KB 20.4 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_3668_fsc.xml emd_3668_fsc.xml | 10.5 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_3668.png emd_3668.png | 248.6 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-3668 http://ftp.pdbj.org/pub/emdb/structures/EMD-3668 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-3668 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-3668 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_3668_validation.pdf.gz emd_3668_validation.pdf.gz | 318.7 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_3668_full_validation.pdf.gz emd_3668_full_validation.pdf.gz | 317.8 KB | 表示 | |
| XML形式データ |  emd_3668_validation.xml.gz emd_3668_validation.xml.gz | 11.8 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3668 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3668 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3668 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3668 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_3668.map.gz / 形式: CCP4 / 大きさ: 103 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_3668.map.gz / 形式: CCP4 / 大きさ: 103 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Closed dimer (C2) of human ATM (Ataxia telangiectasia mutated) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.43 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
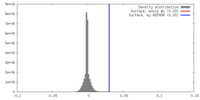
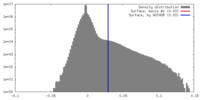
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Dimeric human ATM (Ataxia telangiectasia mutated) kinase
| 全体 | 名称: Dimeric human ATM (Ataxia telangiectasia mutated) kinase |
|---|---|
| 要素 |
|
-超分子 #1: Dimeric human ATM (Ataxia telangiectasia mutated) kinase
| 超分子 | 名称: Dimeric human ATM (Ataxia telangiectasia mutated) kinase タイプ: organelle_or_cellular_component / ID: 1 / 親要素: 0 / 含まれる分子: all 詳細: ATM was produced and imaged with the FLAG tag at the N-terminus. It is a homodimer. |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 実験値: 705 KDa |
| 組換発現 | 生物種:  Homo sapiens (ヒト) / 組換細胞: Expi293F Homo sapiens (ヒト) / 組換細胞: Expi293F |
-分子 #1: human ATM (Ataxia telangiectasia mutated)
| 分子 | 名称: human ATM (Ataxia telangiectasia mutated) / タイプ: protein_or_peptide / ID: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 組換発現 | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 配列 | 文字列: MDYKDDDDKH MS LVLNDLL ICCRQLEHDR ATE RKKEVE KFKRLIRDPE TIKH LDRHS DSKQGKYLNW DAVFR FLQK YIQKETECLR IAKPNV SAS TQASRQKKMQ EISSLVK YF IKCANRRAPR LKCQELLN Y IMDTVKDSSN GAIYGADCS NILLKDILSV ...文字列: MDYKDDDDKH MS LVLNDLL ICCRQLEHDR ATE RKKEVE KFKRLIRDPE TIKH LDRHS DSKQGKYLNW DAVFR FLQK YIQKETECLR IAKPNV SAS TQASRQKKMQ EISSLVK YF IKCANRRAPR LKCQELLN Y IMDTVKDSSN GAIYGADCS NILLKDILSV RKYWCEISQQ QWLELFSVY FRLYLKPSQD V HRVLVARI IHAVTKGCCS QT DGLNSKF LDFFSKAIQC ARQ EKSSSG LNHILAALTI FLKT LAVNF RIRVCELGDE ILPTL LYIW TQHRLNDSLK EVIIEL FQL QIYIHHPKGA KTQEKGA YE STKWRSILYN LYDLLVNE I SHIGSRGKYS SGFRNIAVK ENLIELMADI CHQVFNEDTR SLEISQSYT TTQRESSDYS V PCKRKKIE LGWEVIKDHL QK SQNDFDL VPWLQIATQL ISK YPASLP NCELSPLLMI LSQL LPQQR HGERTPYVLR CLTEV ALCQ DKRSNLESSQ KSDLLK LWN KIWCITFRGI SSEQIQA EN FGLLGAIIQG SLVEVDRE F WKLFTGSACR PSCPAVCCL TLALTTSIVP GTVKMGIEQN MCEVNRSFS LKESIMKWLL F YQLEGDLE NSTEVPPILH SN FPHLVLE KILVSLTMKN CKA AMNFFQ SVPECEHHQK DKEE LSFSE VEELFLQTTF DKMDF LTIV RECGIEKHQS SIGFSV HQN LKESLDRCLL GLSEQLL NN YSSEITNSET LVRCSRLL V GVLGCYCYMG VIAEEEAYK SELFQKAKSL MQCAGESITL FKNKTNEEF RIGSLRNMMQ L CTRCLSNC TKKSPNKIAS GF FLRLLTS KLMNDIADIC KSL ASFIKK PFDRGEVESM EDDT NGNLM EVEDQSSMNL FNDYP DSSV SDANEPGESQ STIGAI NPL AEEYLSKQDL LFLDMLK FL CLCVTTAQTN TVSFRAAD I RRKLLMLIDS STLEPTKSL HLHMYLMLLK ELPGEEYPLP MEDVLELLK PLSNVCSLYR R DQDVCKTI LNHVLHVVKN LG QSNMDSE NTRDAQGQFL TVI GAFWHL TKERKYIFSV RMAL VNCLK TLLEADPYSK WAILN VMGK DFPVNEVFTQ FLADNH HQV RMLAAESINR LFQDTKG DS SRLLKALPLK LQQTAFEN A YLKAQEGMRE MSHSAENPE TLDEIYNRKS VLLTLIAVVL SCSPICEKQ ALFALCKSVK E NGLEPHLV KKVLEKVSET FG YRRLEDF MASHLDYLVL EWL NLQDTE YNLSSFPFIL LNYT NIEDF YRSCYKVLIP HLVIR SHFD EVKSIANQIQ EDWKSL LTD CFPKILVNIL PYFAYEG TR DSGMAQQRET ATKVYDML K SENLLGKQID HLFISNLPE IVVELLMTLH EPANSSASQS TDLCDFSGD LDPAPNPPHF P SHVIKATF AYISNCHKTK LK SILEILS KSPDSYQKIL LAI CEQAAE TNNVYKKHRI LKIY HLFVS LLLKDIKSGL GGAWA FVLR DVIYTLIHYI NQRPSC IMD VSLRSFSLCC DLLSQVC QT AVTYCKDALE NHLHVIVG T LIPLVYEQVE VQKQVLDLL KYLVIDNKDN ENLYITIKLL DPFPDHVVF KDLRITQQKI K YSRGPFSL LEEINHFLSV SV YDALPLT RLEGLKDLRR QLE LHKDQM VDIMRASQDN PQDG IMVKL VVNLLQLSKM AINHT GEKE VLEAVGSCLG EVGPID FST IAIQHSKDAS YTKALKL FE DKELQWTFIM LTYLNNTL V EDCVKVRSAA VTCLKNILA TKTGHSFWEI YKMTTDPMLA YLQPFRTSR KKFLEVPRFD K ENPFEGLD DINLWIPLSE NH DIWIKTL TCAFLDSGGT KCE ILQLLK PMCEVKTDFC QTVL PYLIH DILLQDTNES WRNLL STHV QGFFTSCLRH FSQTSR STT PANLDSESEH FFRCCLD KK SQRTMLAVVD YMRRQKRP S SGTIFNDAFW LDLNYLEVA KVAQSCAAHF TALLYAEIYA DKKSMDDQE KRSLAFEEGS Q STTISSLS EKSKEETGIS LQ DLLLEIY RSIGEPDSLY GCG GGKMLQ PITRLRTYEH EAMW GKALV TYDLETAIPS STRQA GIIQ ALQNLGLCHI LSVYLK GLD YENKDWCPEL EELHYQA AW RNMQWDHCTS VSKEVEGT S YHESLYNALQ SLRDREFST FYESLKYARV KEVEEMCKRS LESVYSLYP TLSRLQAIGE L ESIGELFS RSVTHRQLSE VY IKWQKHS QLLKDSDFSF QEP IMALRT VILEILMEKE MDNS QRECI KDILTKHLVE LSILA RTFK NTQLPERAIF QIKQYN SVS CGVSEWQLEE AQVFWAK KE QSLALSILKQ MIKKLDAS C AANNPSLKLT YTECLRVCG NWLAETCLEN PAVIMQTYLE KAVEVAGNY DGESSDELRN G KMKAFLSL ARFSDTQYQR IE NYMKSSE FENKQALLKR AKE EVGLLR EHKIQTNRYT VKVQ RELEL DELALRALKE DRKRF LCKA VENYINCLLS GEEHDM WVF RLCSLWLENS GVSEVNG MM KRDGMKIPTY KFLPLMYQ L AARMGTKMMG GLGFHEVLN NLISRISMDH PHHTLFIILA LANANRDEF LTKPEVARRS R ITKNVPKQ SSQLDEDRTE AA NRIICTI RSRRPQMVRS VEA LCDAYI ILANLDATQW KTQR KGINI PADQPITKLK NLEDV VVPT MEIKVDHTGE YGNLVT IQS FKAEFRLAGG VNLPKII DC VGSDGKERRQ LVKGRDDL R QDAVMQQVFQ MCNTLLQRN TETRKRKLTI CTYKVVPLSQ RSGVLEWCT GTVPIGEFLV N NEDGAHKR YRPNDFSAFQ CQ KKMMEVQ KKSFEEKYEV FMD VCQNFQ PVFRYFCMEK FLDP AIWFE KRLAYTRSVA TSSIV GYIL GLGDRHVQNI LINEQS AEL VHIDLGVAFE QGKILPT PE TVPFRLTRDI VDGMGITG V EGVFRRCCEK TMEVMRNSQ ETLLTIVEVL LYDPLFDWTM NPLKALYLQ QRPEDETELH P TLNADDQE CKRNLSDIDQ SF NKVAERV LMRLQEKLKG VEE GTVLSV GGQVNLLIQQ AIDP KNLSR LFPGWKAWV |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製 #1
試料調製 #1
| Preparation ID | 1 | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 濃度 | 0.6 mg/mL | ||||||||||||||||||
| 緩衝液 | pH: 8 構成要素:
| ||||||||||||||||||
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: GOLD / メッシュ: 300 / 支持フィルム - Film type ID: 1 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: PLASMA CLEANING / 前処理 - 雰囲気: OTHER | ||||||||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277.15 K / 装置: HOMEMADE PLUNGER 詳細: 3uL of sample/grid blotted for 12 s before plunge-freezing. | ||||||||||||||||||
| 詳細 | The sample was purified by anti-FLAG affinity chromatography followed by overnight dialysis and a final size-exclusion chromatography. |
- 試料調製 #2
試料調製 #2
| Preparation ID | 2 | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 8 構成要素:
| ||||||||||||||||||
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: GOLD / メッシュ: 300 / 支持フィルム - Film type ID: 1 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: PLASMA CLEANING / 前処理 - 雰囲気: OTHER | ||||||||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277.15 K / 装置: HOMEMADE PLUNGER 詳細: 3uL of sample/grid blotted for 12 s before plunge-freezing. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 温度 | 最低: 80.15 K |
| 特殊光学系 | エネルギーフィルター - 名称: GIF エネルギーフィルター - エネルギー下限: 0 eV エネルギーフィルター - エネルギー上限: 20 eV |
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: SUPER-RESOLUTION / デジタル化 - 画像ごとのフレーム数: 1-20 / 撮影したグリッド数: 4 / 実像数: 2720 / 平均露光時間: 0.8 sec. / 平均電子線量: 2.1 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 70.0 µm / 倍率(補正後): 35714 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 4.0 µm / 最小 デフォーカス(公称値): 2.5 µm / 倍率(公称値): 97902 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー


















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)