+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Human ATP synthase state 3b subregion 2 | |||||||||||||||
 マップデータ マップデータ | ||||||||||||||||
 試料 試料 |
| |||||||||||||||
 キーワード キーワード | MEMBRANE PROTEIN | |||||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報Formation of ATP by chemiosmotic coupling / Cristae formation / proton-transporting ATP synthase complex / : / : / : / proton motive force-driven ATP synthesis / proton transmembrane transporter activity / proton motive force-driven mitochondrial ATP synthesis / Mitochondrial protein degradation ...Formation of ATP by chemiosmotic coupling / Cristae formation / proton-transporting ATP synthase complex / : / : / : / proton motive force-driven ATP synthesis / proton transmembrane transporter activity / proton motive force-driven mitochondrial ATP synthesis / Mitochondrial protein degradation / substantia nigra development / mitochondrial inner membrane / mitochondrial matrix / mitochondrion / membrane / nucleus 類似検索 - 分子機能 | |||||||||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.97 Å | |||||||||||||||
 データ登録者 データ登録者 | Lai Y / Zhang Y / Liu F / Gao Y / Gong H / Rao Z | |||||||||||||||
| 資金援助 |  中国, 4件 中国, 4件
| |||||||||||||||
 引用 引用 |  ジャーナル: Mol Cell / 年: 2023 ジャーナル: Mol Cell / 年: 2023タイトル: Structure of the human ATP synthase. 著者: Yuezheng Lai / Yuying Zhang / Shan Zhou / Jinxu Xu / Zhanqiang Du / Ziyan Feng / Long Yu / Ziqing Zhao / Weiwei Wang / Yanting Tang / Xiuna Yang / Luke W Guddat / Fengjiang Liu / Yan Gao / ...著者: Yuezheng Lai / Yuying Zhang / Shan Zhou / Jinxu Xu / Zhanqiang Du / Ziyan Feng / Long Yu / Ziqing Zhao / Weiwei Wang / Yanting Tang / Xiuna Yang / Luke W Guddat / Fengjiang Liu / Yan Gao / Zihe Rao / Hongri Gong /   要旨: Biological energy currency ATP is produced by FF-ATP synthase. However, the molecular mechanism for human ATP synthase action remains unknown. Here, we present snapshot images for three main ...Biological energy currency ATP is produced by FF-ATP synthase. However, the molecular mechanism for human ATP synthase action remains unknown. Here, we present snapshot images for three main rotational states and one substate of human ATP synthase using cryoelectron microscopy. These structures reveal that the release of ADP occurs when the β subunit of FF-ATP synthase is in the open conformation, showing how ADP binding is coordinated during synthesis. The accommodation of the symmetry mismatch between F and F motors is resolved by the torsional flexing of the entire complex, especially the γ subunit, and the rotational substep of the c subunit. Water molecules are identified in the inlet and outlet half-channels, suggesting that the proton transfer in these two half-channels proceed via a Grotthus mechanism. Clinically relevant mutations are mapped to the structure, showing that they are mainly located at the subunit-subunit interfaces, thus causing instability of the complex. | |||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_34578.map.gz emd_34578.map.gz | 483.7 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-34578-v30.xml emd-34578-v30.xml emd-34578.xml emd-34578.xml | 17.2 KB 17.2 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_34578.png emd_34578.png | 75.6 KB | ||
| Filedesc metadata |  emd-34578.cif.gz emd-34578.cif.gz | 5.6 KB | ||
| その他 |  emd_34578_half_map_1.map.gz emd_34578_half_map_1.map.gz emd_34578_half_map_2.map.gz emd_34578_half_map_2.map.gz | 474.6 MB 474.6 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-34578 http://ftp.pdbj.org/pub/emdb/structures/EMD-34578 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-34578 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-34578 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_34578_validation.pdf.gz emd_34578_validation.pdf.gz | 1.2 MB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_34578_full_validation.pdf.gz emd_34578_full_validation.pdf.gz | 1.2 MB | 表示 | |
| XML形式データ |  emd_34578_validation.xml.gz emd_34578_validation.xml.gz | 18.8 KB | 表示 | |
| CIF形式データ |  emd_34578_validation.cif.gz emd_34578_validation.cif.gz | 22.2 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-34578 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-34578 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-34578 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-34578 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8h9rMC  8h9eC  8h9fC  8h9gC  8h9iC  8h9jC  8h9kC  8h9lC  8h9mC  8h9nC  8h9pC  8h9qC  8h9sC  8h9tC  8h9uC  8h9vC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_34578.map.gz / 形式: CCP4 / 大きさ: 512 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_34578.map.gz / 形式: CCP4 / 大きさ: 512 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.73 Å | ||||||||||||||||||||||||||||||||||||
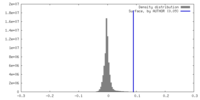
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: #1
| ファイル | emd_34578_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
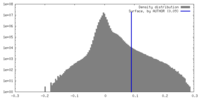
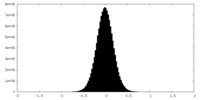
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_34578_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
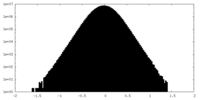
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Human ATP synthase
| 全体 | 名称: Human ATP synthase |
|---|---|
| 要素 |
|
-超分子 #1: Human ATP synthase
| 超分子 | 名称: Human ATP synthase / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 600 KDa |
-分子 #1: ATP synthase F(0) complex subunit B1, mitochondrial
| 分子 | 名称: ATP synthase F(0) complex subunit B1, mitochondrial / タイプ: protein_or_peptide / ID: 1 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 24.658586 KDa |
| 配列 | 文字列: PVPPLPEYGG KVRYGLIPEE FFQFLYPKTG VTGPYVLGTG LILYALSKEI YVISAETFTA LSVLGVMVYG IKKYGPFVAD FADKLNEQK LAQLEEAKQA SIQHIQNAID TEKSQQALVQ KRHYLFDVQR NNIAMALEVT YRERLYRVYK EVKNRLDYHI S VQNMMRRK ...文字列: PVPPLPEYGG KVRYGLIPEE FFQFLYPKTG VTGPYVLGTG LILYALSKEI YVISAETFTA LSVLGVMVYG IKKYGPFVAD FADKLNEQK LAQLEEAKQA SIQHIQNAID TEKSQQALVQ KRHYLFDVQR NNIAMALEVT YRERLYRVYK EVKNRLDYHI S VQNMMRRK EQEHMINWVE KHVVQSISTQ QEKETIAKCI ADLKLLAKKA QAQPVM UniProtKB: ATP synthase F(0) complex subunit B1, mitochondrial |
-分子 #2: ATP synthase-coupling factor 6, mitochondrial
| 分子 | 名称: ATP synthase-coupling factor 6, mitochondrial / タイプ: protein_or_peptide / ID: 2 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 12.606499 KDa |
| 配列 | 文字列: MILQRLFRFS SVIRSAVSVH LRRNIGVTAV AFNKELDPIQ KLFVDKIREY KSKRQTSGGP VDASSEYQQE LERELFKLKQ MFGNADMNT FPTFKFEDPK FEVIEKPQA UniProtKB: ATP synthase-coupling factor 6, mitochondrial |
-分子 #3: ATP synthase subunit d, mitochondrial
| 分子 | 名称: ATP synthase subunit d, mitochondrial / タイプ: protein_or_peptide / ID: 3 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 18.383982 KDa |
| 配列 | 文字列: AGRKLALKTI DWVAFAEIIP QNQKAIASSL KSWNETLTSR LAALPENPPA IDWAYYKANV AKAGLVDDFE KKFNALKVPV PEDKYTAQV DAEEKEDVKS CAEWVSLSKA RIVEYEKEME KMKNLIPFDQ MTIEDLNEAF PETKLDKKKY PYWPHQPIEN L UniProtKB: ATP synthase subunit d, mitochondrial |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.4 |
|---|---|
| グリッド | モデル: Quantifoil R1.2/1.3 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY |
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 特殊光学系 | エネルギーフィルター - 名称: TFS Selectris X / エネルギーフィルター - スリット幅: 10 eV |
| 撮影 | フィルム・検出器のモデル: FEI FALCON IV (4k x 4k) 平均電子線量: 50.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.4 µm / 最小 デフォーカス(公称値): 1.2 µm |
| 試料ステージ | ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 初期モデル | モデルのタイプ: OTHER / 詳細: AlphaFold |
|---|---|
| 最終 再構成 | 解像度のタイプ: BY AUTHOR / 解像度: 3.97 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 使用した粒子像数: 23272 |
| 初期 角度割当 | タイプ: MAXIMUM LIKELIHOOD / ソフトウェア - 名称: cryoSPARC |
| 最終 角度割当 | タイプ: MAXIMUM LIKELIHOOD / ソフトウェア - 名称: cryoSPARC |
 ムービー
ムービー コントローラー
コントローラー





















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)