+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-3202 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of the E. coli replicative DNA polymerase complex bound to DNA (DNA polymerase III alpha, beta, and epsilon subunits) | |||||||||
 マップデータ マップデータ | E. coli replicative DNA polymerase complex bound to DNA (DNA polymerase III alpha, beta, and epsilon subunits) | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | DNA replication / DNA polymerase III alpha / DNA polymerase III beta / DNA polymerase III epsilon | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報DNA polymerase III, core complex / Hda-beta clamp complex / bacterial-type DNA replication / replication inhibiting complex / DNA polymerase III complex / lagging strand elongation / replisome / exonuclease activity / regulation of DNA-templated DNA replication initiation / DNA replication proofreading ...DNA polymerase III, core complex / Hda-beta clamp complex / bacterial-type DNA replication / replication inhibiting complex / DNA polymerase III complex / lagging strand elongation / replisome / exonuclease activity / regulation of DNA-templated DNA replication initiation / DNA replication proofreading / DNA strand elongation involved in DNA replication / leading strand elongation / error-prone translesion synthesis / negative regulation of DNA-templated DNA replication initiation / 3'-5' exonuclease activity / DNA-templated DNA replication / DNA replication / DNA-directed DNA polymerase / DNA-directed DNA polymerase activity / DNA damage response / protein homodimerization activity / DNA binding / identical protein binding / metal ion binding / cytoplasm / cytosol 類似検索 - 分子機能 | |||||||||
| 生物種 |  | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 7.3 Å | |||||||||
 データ登録者 データ登録者 | Fernandez-Leiro R / Conrad J / Scheres HWS / Lamers MH | |||||||||
 引用 引用 |  ジャーナル: Elife / 年: 2015 ジャーナル: Elife / 年: 2015タイトル: cryo-EM structures of the replicative DNA polymerase reveal its dynamic interactions with the DNA sliding clamp, exonuclease and . 著者: Rafael Fernandez-Leiro / Julian Conrad / Sjors Hw Scheres / Meindert H Lamers /  要旨: The replicative DNA polymerase PolIIIα from is a uniquely fast and processive enzyme. For its activity it relies on the DNA sliding clamp β, the proofreading exonuclease ε and the C-terminal ...The replicative DNA polymerase PolIIIα from is a uniquely fast and processive enzyme. For its activity it relies on the DNA sliding clamp β, the proofreading exonuclease ε and the C-terminal domain of the clamp loader subunit τ. Due to the dynamic nature of the four-protein complex it has long been refractory to structural characterization. Here we present the 8 Å resolution cryo-electron microscopy structures of DNA-bound and DNA-free states of the PolIII-clamp-exonuclease-τ complex. The structures show how the polymerase is tethered to the DNA through multiple contacts with the clamp and exonuclease. A novel contact between the polymerase and clamp is made in the DNA bound state, facilitated by a large movement of the polymerase tail domain and τ. These structures provide crucial insights into the organization of the catalytic core of the replisome and form an important step towards determining the structure of the complete holoenzyme. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_3202.map.gz emd_3202.map.gz | 7.4 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-3202-v30.xml emd-3202-v30.xml emd-3202.xml emd-3202.xml | 16.4 KB 16.4 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_3202_fsc.xml emd_3202_fsc.xml | 4.6 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  EMD-3202.png EMD-3202.png emd_3202.png emd_3202.png | 284.5 KB 284.5 KB | ||
| マスクデータ |  emd_3202_msk_1.map emd_3202_msk_1.map | 8 MB |  マスクマップ マスクマップ | |
| その他 |  emd_3202_half_map_1.map.gz emd_3202_half_map_1.map.gz emd_3202_half_map_2.map.gz emd_3202_half_map_2.map.gz | 6 MB 6 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-3202 http://ftp.pdbj.org/pub/emdb/structures/EMD-3202 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-3202 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-3202 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_3202_validation.pdf.gz emd_3202_validation.pdf.gz | 312.9 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_3202_full_validation.pdf.gz emd_3202_full_validation.pdf.gz | 312 KB | 表示 | |
| XML形式データ |  emd_3202_validation.xml.gz emd_3202_validation.xml.gz | 7.8 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3202 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3202 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3202 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-3202 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_3202.map.gz / 形式: CCP4 / 大きさ: 7.8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_3202.map.gz / 形式: CCP4 / 大きさ: 7.8 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | E. coli replicative DNA polymerase complex bound to DNA (DNA polymerase III alpha, beta, and epsilon subunits) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.76 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-セグメンテーションマップ: mask for reconstructions
| 注釈 | mask for reconstructions | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ファイル |  emd_3202_msk_1.map emd_3202_msk_1.map | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
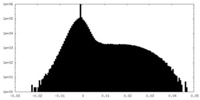
| 密度ヒストグラム |
-添付マップデータ: emd 3202 half map 1.map
| ファイル | emd_3202_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-添付マップデータ: emd 3202 half map 2.map
| ファイル | emd_3202_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : DNA polymerase III catalytic complex
| 全体 | 名称: DNA polymerase III catalytic complex |
|---|---|
| 要素 |
|
-超分子 #1000: DNA polymerase III catalytic complex
| 超分子 | 名称: DNA polymerase III catalytic complex / タイプ: sample / ID: 1000 詳細: Individual proteins purified individually and the complex was later assembled in vitro and purified over gel filtration DNA polymerase subunit tau is not visible in this map due to comformational heterogeneity 集合状態: 1 DNA polymerase III alpha : 2 DNA polymerase III beta: 1 DNA polymerase III epsilon : 1 dsDNA Number unique components: 5 |
|---|---|
| 分子量 | 理論値: 256 KDa |
-分子 #1: DNA polymerase III alpha
| 分子 | 名称: DNA polymerase III alpha / タイプ: protein_or_peptide / ID: 1 / Name.synonym: dnaE 詳細: amino acid residues 920-924 of E. coli PolIII alpha were changed by site directed mutagenesis from QADMF to QLDLF コピー数: 1 / 集合状態: 1 / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 132 KDa |
| 組換発現 | 生物種:  |
| 配列 | UniProtKB: DNA polymerase III subunit alpha GO: DNA replication, DNA binding, DNA-directed DNA polymerase activity InterPro: DNA polymerase III, alpha subunit |
-分子 #2: DNA polymerase III beta
| 分子 | 名称: DNA polymerase III beta / タイプ: protein_or_peptide / ID: 2 / Name.synonym: DNA clamp / コピー数: 1 / 集合状態: 2 / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 81 KDa |
| 組換発現 | 生物種:  |
| 配列 | UniProtKB: Beta sliding clamp / GO: DNA strand elongation involved in DNA replication / InterPro: DNA polymerase III, beta sliding clamp |
-分子 #3: DNA polymerase III epsilon
| 分子 | 名称: DNA polymerase III epsilon / タイプ: protein_or_peptide / ID: 3 / Name.synonym: dnaQ 詳細: amino acid residues 182-187 of E. coli PolIII epsilon were changed by site directed mutagenesis from QTSMAF to QLSLPL コピー数: 1 / 集合状態: 1 / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 27.3762 KDa |
| 組換発現 | 生物種:  |
| 配列 | UniProtKB: DNA polymerase III subunit epsilon / GO: exonuclease activity / InterPro: DNA polymerase 3, epsilon subunit |
-分子 #4: primer-template duplex DNA
| 分子 | 名称: primer-template duplex DNA / タイプ: dna / ID: 4 / Name.synonym: dsDNA 詳細: template strans has a 4 nucleotide overhang, sequence as follows: TCAGGAGTCCTTCGTCCTAGTACTACTCC 分類: DNA / Structure: DOUBLE HELIX / Synthetic?: Yes |
|---|---|
| 由来(天然) | 生物種: unidentified (未定義) |
| 分子量 | 理論値: 15.5 KDa |
| 配列 | 文字列: GGAGTAGTAC TAGGACGAAG GACTC |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 1 mg/mL |
|---|---|
| 緩衝液 | pH: 7.5 詳細: 25 mM Hepes pH 7.5, 50 mM Potassium Glutamate, 3 mM Magnesium Acetate, 2 mM DTT |
| グリッド | 詳細: glow-discharged holey carbon cryo-EM grids (Quantifoil Cu R1.2/1.3 400 mesh) |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 110 K / 装置: FEI VITROBOT MARK III 手法: Prior to sample preparation 0.1 volumes of 0.05% Tween 20 were added to the sample 3 microliters were pipetted onto the grid and blotted for 4 seconds |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 温度 | 最低: 80 K / 最高: 90 K / 平均: 85 K |
| アライメント法 | Legacy - 非点収差: Objective lens astigmatism was corrected at 64,000 times magnification |
| 日付 | 2014年5月12日 |
| 撮影 | カテゴリ: CCD フィルム・検出器のモデル: GATAN K2 QUANTUM (4k x 4k) デジタル化 - サンプリング間隔: 5 µm / 実像数: 1350 / 平均電子線量: 40 e/Å2 / 詳細: 20 frames/micrograph / ビット/ピクセル: 32 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 倍率(補正後): 28409 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 4.0 µm / 最小 デフォーカス(公称値): 2.0 µm / 倍率(公称値): 64000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー






















 Z
Z Y
Y X
X