+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | CryoEM structure of the A. aeolicus WzmWzt transporter bound to ADP | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | O antigen / ABC transporter / CBD-dependent / TRANSLOCASE | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報lipopolysaccharide transport / ABC-type transporter activity / ATP hydrolysis activity / ATP binding / membrane / plasma membrane 類似検索 - 分子機能 | |||||||||
| 生物種 |   Aquifex aeolicus (バクテリア) / Aquifex aeolicus (バクテリア) /   Aquifex aeolicus VF5 (バクテリア) Aquifex aeolicus VF5 (バクテリア) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.54 Å | |||||||||
 データ登録者 データ登録者 | Gorniak I / Zimmer J / Vlach J | |||||||||
| 資金援助 |  米国, 1件 米国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2022 ジャーナル: Nat Commun / 年: 2022タイトル: Molecular basis for polysaccharide recognition and modulated ATP hydrolysis by the O antigen ABC transporter. 著者: Nicholas Spellmon / Artur Muszyński / Ireneusz Górniak / Jiri Vlach / David Hahn / Parastoo Azadi / Jochen Zimmer /  要旨: O antigens are ubiquitous protective extensions of lipopolysaccharides in the extracellular leaflet of the Gram-negative outer membrane. Following biosynthesis in the cytosol, the lipid-linked ...O antigens are ubiquitous protective extensions of lipopolysaccharides in the extracellular leaflet of the Gram-negative outer membrane. Following biosynthesis in the cytosol, the lipid-linked polysaccharide is transported to the periplasm by the WzmWzt ABC transporter. Often, O antigen secretion requires the chemical modification of its elongating terminus, which the transporter recognizes via a carbohydrate-binding domain (CBD). Here, using components from A. aeolicus, we identify the O antigen structure with methylated mannose or rhamnose as its cap. Crystal and cryo electron microscopy structures reveal how WzmWzt recognizes this cap between its carbohydrate and nucleotide-binding domains in a nucleotide-free state. ATP binding induces drastic conformational changes of its CBD, terminating interactions with the O antigen. ATPase assays and site directed mutagenesis reveal reduced hydrolytic activity upon O antigen binding, likely to facilitate polymer loading into the ABC transporter. Our results elucidate critical steps in the recognition and translocation of polysaccharides by ABC transporters. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_27623.map.gz emd_27623.map.gz | 59.6 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-27623-v30.xml emd-27623-v30.xml emd-27623.xml emd-27623.xml | 18.6 KB 18.6 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_27623.png emd_27623.png | 53 KB | ||
| Filedesc metadata |  emd-27623.cif.gz emd-27623.cif.gz | 6.1 KB | ||
| その他 |  emd_27623_half_map_1.map.gz emd_27623_half_map_1.map.gz emd_27623_half_map_2.map.gz emd_27623_half_map_2.map.gz | 59.3 MB 59.3 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-27623 http://ftp.pdbj.org/pub/emdb/structures/EMD-27623 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-27623 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-27623 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_27623_validation.pdf.gz emd_27623_validation.pdf.gz | 748.4 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_27623_full_validation.pdf.gz emd_27623_full_validation.pdf.gz | 747.9 KB | 表示 | |
| XML形式データ |  emd_27623_validation.xml.gz emd_27623_validation.xml.gz | 12.2 KB | 表示 | |
| CIF形式データ |  emd_27623_validation.cif.gz emd_27623_validation.cif.gz | 14.3 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-27623 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-27623 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-27623 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-27623 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8douMC  8dkuC  8dkyC  8dl0C  8dn8C  8dncC  8dneC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_27623.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_27623.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.12 Å | ||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
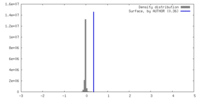
-ハーフマップ: #1
| ファイル | emd_27623_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
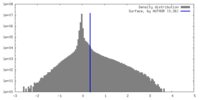
-ハーフマップ: #2
| ファイル | emd_27623_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : O antigen ABC transporter
| 全体 | 名称: O antigen ABC transporter |
|---|---|
| 要素 |
|
-超分子 #1: O antigen ABC transporter
| 超分子 | 名称: O antigen ABC transporter / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1-#2 |
|---|---|
| 由来(天然) | 生物種:   Aquifex aeolicus (バクテリア) / 株: VF5 Aquifex aeolicus (バクテリア) / 株: VF5 |
-分子 #1: ABC transporter
| 分子 | 名称: ABC transporter / タイプ: protein_or_peptide / ID: 1 / コピー数: 2 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:   Aquifex aeolicus VF5 (バクテリア) / 株: VF5 Aquifex aeolicus VF5 (バクテリア) / 株: VF5 |
| 分子量 | 理論値: 46.28441 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MGIRVFDVWK KYKYYKKPQD RLKEIIFRKP FHEELWVLKG INLEIEKGEV LGIVGPNGAG KSTLLKVITG VTEPDKGFVE RSGKVVGLL ELGTGFNYEL SGLENIYVNA SLLGLSRREI DEKLESIIEF SELDDFINKP LKTYSSGMIM RLAFSIAIHT E PECFIIDE ...文字列: MGIRVFDVWK KYKYYKKPQD RLKEIIFRKP FHEELWVLKG INLEIEKGEV LGIVGPNGAG KSTLLKVITG VTEPDKGFVE RSGKVVGLL ELGTGFNYEL SGLENIYVNA SLLGLSRREI DEKLESIIEF SELDDFINKP LKTYSSGMIM RLAFSIAIHT E PECFIIDE ALAVGDAHFQ QKCFRKLKEH KQKGGSIIFV SHDMNAVKIL CDRAILLHKG EIIEEGSPET VTQAYYKLMA SL ENKEGIT FLQNGYGNFK AVIKEVRLKS EHGYTNNFPS GDTLFIELDV EAKEDLQDVV AGILIRDRFG QDIFGINTYL MEK KVELKK GKYLFTFKMP LNLAPGKYTL TVALHKGMDH AQECYHWIDN VCNFEVNGFK KEQFVGVCYL PTEFNYRKIP KLHH HHHH UniProtKB: ABC transporter |
-分子 #2: Transport permease protein
| 分子 | 名称: Transport permease protein / タイプ: protein_or_peptide / ID: 2 / コピー数: 2 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:   Aquifex aeolicus VF5 (バクテリア) / 株: VF5 Aquifex aeolicus VF5 (バクテリア) / 株: VF5 |
| 分子量 | 理論値: 30.027871 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MNLSLILELV RQEIKNRYAD TVLGIWWAFL WPILLVLIYT LIFSHLIGAK LGHENTVYAY SIYLSSGIFP WFFFSNSLSR ITGIFTEKK FLFTKIPIRL EVFPVVVIIS ELINYLIGIS LVTLISFITL GFEGIKYFYL FPVALYLMIV YSFSIGMVLG T LNVFFRDI ...文字列: MNLSLILELV RQEIKNRYAD TVLGIWWAFL WPILLVLIYT LIFSHLIGAK LGHENTVYAY SIYLSSGIFP WFFFSNSLSR ITGIFTEKK FLFTKIPIRL EVFPVVVIIS ELINYLIGIS LVTLISFITL GFEGIKYFYL FPVALYLMIV YSFSIGMVLG T LNVFFRDI KEIIGVFLQI FFWFTPIVYT LDILPPFVKK LIYYNPMYPV VSIHHLVFVN YLDLHLYSLL GFLLASPLVF FV SYYFFKK LEKDIKDFA UniProtKB: Transport permease protein |
-分子 #3: ADENOSINE-5'-DIPHOSPHATE
| 分子 | 名称: ADENOSINE-5'-DIPHOSPHATE / タイプ: ligand / ID: 3 / コピー数: 2 / 式: ADP |
|---|---|
| 分子量 | 理論値: 427.201 Da |
| Chemical component information |  ChemComp-ADP: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 1.0 mg/mL | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.5 構成要素:
| ||||||||||||
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: COPPER / メッシュ: 300 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 60 sec. / 前処理 - 雰囲気: AIR / 詳細: amylamine | ||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK IV | ||||||||||||
| 詳細 | WzmWzt nanodisc incubated with ADP/Mg (2.5mM each). |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 平均電子線量: 50.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 100.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 20.0 µm / 最小 デフォーカス(公称値): 10.0 µm / 倍率(公称値): 81000 |
| 試料ステージ | ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 精密化 | プロトコル: RIGID BODY FIT |
|---|---|
| 得られたモデル |  PDB-8dou: |
 ムービー
ムービー コントローラー
コントローラー











 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)