+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-25442 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of prestin from gerbil (Meriones unguiculatus) in the presence of NaCl | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Prestin (Slc26a5) / cochlear amplification / NonLinear Capacitance / MEMBRANE PROTEIN / MOTOR PROTEIN | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報oxalate transmembrane transporter activity / secondary active sulfate transmembrane transporter activity / chloride:bicarbonate antiporter activity / bicarbonate transport / chloride transport / lateral plasma membrane / sensory perception of sound / regulation of cell shape / basolateral plasma membrane / protein homodimerization activity 類似検索 - 分子機能 | |||||||||
| 生物種 |  Meriones unguiculatus (スナネズミ) / synthetic construct (人工物) Meriones unguiculatus (スナネズミ) / synthetic construct (人工物) | |||||||||
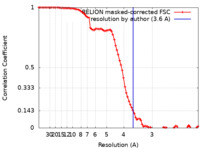
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.6 Å | |||||||||
 データ登録者 データ登録者 | Butan C / Santos-Sacchi J | |||||||||
| 資金援助 |  米国, 1件 米国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2022 ジャーナル: Nat Commun / 年: 2022タイトル: Single particle cryo-EM structure of the outer hair cell motor protein prestin. 著者: Carmen Butan / Qiang Song / Jun-Ping Bai / Winston J T Tan / Dhasakumar Navaratnam / Joseph Santos-Sacchi /  要旨: The mammalian outer hair cell (OHC) protein prestin (Slc26a5) differs from other Slc26 family members due to its unique piezoelectric-like property that drives OHC electromotility, the putative ...The mammalian outer hair cell (OHC) protein prestin (Slc26a5) differs from other Slc26 family members due to its unique piezoelectric-like property that drives OHC electromotility, the putative mechanism for cochlear amplification. Here, we use cryo-electron microscopy to determine prestin's structure at 3.6 Å resolution. Prestin is structurally similar to the anion transporter Slc26a9. It is captured in an inward-open state which may reflect prestin's contracted state. Two well-separated transmembrane (TM) domains and two cytoplasmic sulfate transporter and anti-sigma factor antagonist (STAS) domains form a swapped dimer. The transmembrane domains consist of 14 transmembrane segments organized in two 7+7 inverted repeats, an architecture first observed in the bacterial symporter UraA. Mutation of prestin's chloride binding site removes salicylate competition with anions while retaining the prestin characteristic displacement currents (Nonlinear Capacitance), undermining the extrinsic voltage sensor hypothesis for prestin function. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_25442.map.gz emd_25442.map.gz | 49.3 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-25442-v30.xml emd-25442-v30.xml emd-25442.xml emd-25442.xml | 11 KB 11 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_25442_fsc.xml emd_25442_fsc.xml | 8.6 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_25442.png emd_25442.png | 162.9 KB | ||
| Filedesc metadata |  emd-25442.cif.gz emd-25442.cif.gz | 5.9 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-25442 http://ftp.pdbj.org/pub/emdb/structures/EMD-25442 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-25442 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-25442 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_25442_validation.pdf.gz emd_25442_validation.pdf.gz | 637.2 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_25442_full_validation.pdf.gz emd_25442_full_validation.pdf.gz | 636.7 KB | 表示 | |
| XML形式データ |  emd_25442_validation.xml.gz emd_25442_validation.xml.gz | 10.4 KB | 表示 | |
| CIF形式データ |  emd_25442_validation.cif.gz emd_25442_validation.cif.gz | 13.6 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-25442 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-25442 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-25442 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-25442 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_25442.map.gz / 形式: CCP4 / 大きさ: 52.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_25442.map.gz / 形式: CCP4 / 大きさ: 52.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.068 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
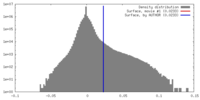
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Prestin dimer surrounded by a belt of detergent
| 全体 | 名称: Prestin dimer surrounded by a belt of detergent |
|---|---|
| 要素 |
|
-超分子 #1: Prestin dimer surrounded by a belt of detergent
| 超分子 | 名称: Prestin dimer surrounded by a belt of detergent / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  Meriones unguiculatus (スナネズミ) Meriones unguiculatus (スナネズミ) |
-分子 #1: Prestin, Enhanced Yellow Fluorescent Protein chimera
| 分子 | 名称: Prestin, Enhanced Yellow Fluorescent Protein chimera タイプ: protein_or_peptide / ID: 1 / コピー数: 2 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種: synthetic construct (人工物) |
| 分子量 | 理論値: 111.865805 KDa |
| 組換発現 | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 配列 | 文字列: MDHAEENEIP VATQKYHVER PIFSHPVLQE RLHVKDKVSE SIGDKLKQAF TCTPKKIRNI IYMFLPITKW LPAYKFKEYV LGDLVSGIS TGVLQLPQGL AFAMLAAVPP VFGLYSSFYP VIMYCFFGTS RHISIGPFAV ISLMIGGVAV RLVPDDIVIP G GVNATNGT ...文字列: MDHAEENEIP VATQKYHVER PIFSHPVLQE RLHVKDKVSE SIGDKLKQAF TCTPKKIRNI IYMFLPITKW LPAYKFKEYV LGDLVSGIS TGVLQLPQGL AFAMLAAVPP VFGLYSSFYP VIMYCFFGTS RHISIGPFAV ISLMIGGVAV RLVPDDIVIP G GVNATNGT EARDALRVKV AMSVTLLSGI IQFCLGVCRF GFVAIYLTEP LVRGFTTAAA VHVFTSMLKY LFGVKTKRYS GI FSVVYST VAVLQNVKNL NVCSLGVGLM VFGLLLGGKE FNERFKEKLP APIPLEFFAV VMGTGISAGF NLHESYSVDV VGT LPLGLL PPANPDTSLF HLVYVDAIAI AIVGFSVTIS MAKTLANKHG YQVDGNQELI ALGICNSIGS LFQTFSISCS LSRS LVQEG TGGKTQLAGC LASLMILLVI LATGFLFESL PQAVLSAIVI VNLKGMFMQF SDLPFFWRTS KIELTIWLTT FVSSL FLGL DYGLITAVII ALLTVIYRTQ SPSYKVLGQL PDTDVYIDID AYEEVKEIPG IKIFQINAPI YYANSDLYSN ALKRKT GVN PALIMGARRK AMRKYAKEVG NANIANAAVV KVDGEVDGEN ATKPEEEDDE VKYPPIVIKT TFPEELQRFM PQTENVH TI ILDFTQVNFI DSVGVKTLAV MVKEYGDVGI YVYLAGCSPQ VVNDLTRNRF FENPALKELL FHSIHDAVLG SHVREAMA E QEASAPPPQD DMEPNATPTT PEAARDPPVA TMVSKGEELF TGVVPILVEL DGDVNGHKFS VSGEGEGDAT YGKLTLKFI CTTGKLPVPW PTLVTTFGYG LQCFARYPDH MKQHDFFKSA MPEGYVQERT IFFKDDGNYK TRAEVKFEGD TLVNRIELKG IDFKEDGNI LGHKLEYNYN SHNVYIMADK QKNGIKVNFK IRHNIEDGSV QLADHYQQNT PIGDGPVLLP DNHYLSYQSA L SKDPNEKR DHMVLLEFVT AAGITLGMDE LYKEQKLISE EDLNMHTGHH HHHH UniProtKB: Prestin |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.4 / 詳細: 10 mM HEPES, 200 mM NaCl, 0.02% GDN, pH 7.4 |
|---|---|
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | TFS KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 平均電子線量: 54.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.15 µm 最小 デフォーカス(公称値): 1.1500000000000001 µm 倍率(公称値): 81000 |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー
















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)