+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-21385 | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Map of an acid-sensing ion channel in a resting state at high pH. | |||||||||||||||
 マップデータ マップデータ | Map of an acid-sensing ion channel in a resting state at high pH. | |||||||||||||||
 試料 試料 |
| |||||||||||||||
| 生物種 |  | |||||||||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 4.0 Å | |||||||||||||||
 データ登録者 データ登録者 | Yoder N / Jalali-Yazdi F / Gouaux E | |||||||||||||||
| 資金援助 |  米国, 4件 米国, 4件
| |||||||||||||||
 引用 引用 |  ジャーナル: J Struct Biol / 年: 2020 ジャーナル: J Struct Biol / 年: 2020タイトル: Light-coupled cryo-plunger for time-resolved cryo-EM. 著者: Nate Yoder / Farzad Jalali-Yazdi / Sigrid Noreng / Alexandra Houser / Isabelle Baconguis / Eric Gouaux /  要旨: Proteins are dynamic molecules that can undergo rapid conformational rearrangements in response to stimuli. These structural changes are often critical to protein function, and thus elucidating time- ...Proteins are dynamic molecules that can undergo rapid conformational rearrangements in response to stimuli. These structural changes are often critical to protein function, and thus elucidating time-dependent conformational landscapes has been a long-standing goal of structural biology. To harness the power of single particle cryo-EM methods to enable 'time-resolved' structure determination, we have developed a light-coupled cryo-plunger that pairs flash-photolysis of caged ligands with rapid sample vitrification. The 'flash-plunger' consists of a high-power ultraviolet LED coupled with focusing optics and a motorized linear actuator, enabling the user to immobilize protein targets in vitreous ice within a programmable time window - as short as tens of milliseconds - after stimulus delivery. The flash-plunger is a simple, inexpensive and flexible tool to explore short-lived conformational states previously unobtainable by conventional sample preparation methods. | |||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_21385.map.gz emd_21385.map.gz | 168.2 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-21385-v30.xml emd-21385-v30.xml emd-21385.xml emd-21385.xml | 12.5 KB 12.5 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_21385.png emd_21385.png | 39.7 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-21385 http://ftp.pdbj.org/pub/emdb/structures/EMD-21385 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-21385 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-21385 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_21385_validation.pdf.gz emd_21385_validation.pdf.gz | 78.5 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_21385_full_validation.pdf.gz emd_21385_full_validation.pdf.gz | 77.6 KB | 表示 | |
| XML形式データ |  emd_21385_validation.xml.gz emd_21385_validation.xml.gz | 493 B | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-21385 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-21385 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-21385 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-21385 | HTTPS FTP |
-関連構造データ
| 関連構造データ | C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_21385.map.gz / 形式: CCP4 / 大きさ: 178 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_21385.map.gz / 形式: CCP4 / 大きさ: 178 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Map of an acid-sensing ion channel in a resting state at high pH. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.83 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
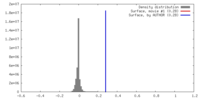
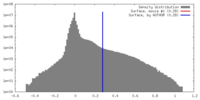
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Acid-sensing ion channel 1
| 全体 | 名称: Acid-sensing ion channel 1 |
|---|---|
| 要素 |
|
-超分子 #1: Acid-sensing ion channel 1
| 超分子 | 名称: Acid-sensing ion channel 1 / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  |
| 組換発現 | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 180 KDa |
-分子 #1: Acid-sensing ion channel 1
| 分子 | 名称: Acid-sensing ion channel 1 / タイプ: protein_or_peptide / ID: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 組換発現 | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 配列 | 文字列: MMDLKVDEEE VDSGQPVSIQ AFASSSTLHG ISHIFSYERL SLKRVVWALC FMGSLALLAL VCTNRIQYY FLYPHVTKLD EVAATRLTFP AVTFCNLNEF RFSRVTKNDL YHAGELLALL N NRYEIPDT QTADEKQLEI LQDKANFRNF KPKPFNMLEF YDRAGHDIRE ...文字列: MMDLKVDEEE VDSGQPVSIQ AFASSSTLHG ISHIFSYERL SLKRVVWALC FMGSLALLAL VCTNRIQYY FLYPHVTKLD EVAATRLTFP AVTFCNLNEF RFSRVTKNDL YHAGELLALL N NRYEIPDT QTADEKQLEI LQDKANFRNF KPKPFNMLEF YDRAGHDIRE MLLSCFFRGE QC SPEDFKV VFTRYGKCYT FNAGQDGKPR LITMKGGTGN GLEIMLDIQQ DEYLPVWGET DET SFEAGI KVQIHSQDEP PLIDQLGFGV APGFQTFVSC QEQRLIYLPP PWGDCKATTG DSEF YDTYS ITACRIDCET RYLVENCNCR MVHMPGDAPY CTPEQYKECA DPALDFLVEK DNEYC VCEM PCNVTRYGKE LSMVKIPSKA SAKYLAKKYN KSEQYIGENI LVLDIFFEAL NYETIE QKK AYEVAGLLGD IGGQMGLFIG ASILTVLELF DYAYEVIKHR LCRRGKCRKN HKRNNTD KG VALSMDDVKR HNPCESLRGH PAGMTYAANI LPHHPARGTF EDFTC |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 1.00 mg/mL |
|---|---|
| 緩衝液 | pH: 8 |
| グリッド | モデル: Quantifoil R2/2 / 材質: GOLD / メッシュ: 200 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY |
| 凍結 | 凍結剤: ETHANE-PROPANE / チャンバー内湿度: 70 % / チャンバー内温度: 277.15 K / 装置: HOMEMADE PLUNGER 詳細: Specimen was frozen on a custom-made manual plunge apparatus in a cold room environment maintained at high humidity. Vitrification occurred following 25 ms of exposure to low power UV irradiation.. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 検出モード: SUPER-RESOLUTION / 平均電子線量: 50.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| CTF補正 | ソフトウェア - 名称: Gctf |
|---|---|
| 最終 再構成 | 想定した対称性 - 点群: C3 (3回回転対称) / 解像度のタイプ: BY AUTHOR / 解像度: 4.0 Å / 解像度の算出法: FSC 0.143 CUT-OFF / ソフトウェア - 名称: cryoSPARC (ver. 2) / 使用した粒子像数: 16673 |
| 初期 角度割当 | タイプ: RANDOM ASSIGNMENT / ソフトウェア - 名称: cryoSPARC (ver. 2) |
| 最終 角度割当 | タイプ: MAXIMUM LIKELIHOOD / ソフトウェア - 名称: cryoSPARC (ver. 2) |
 ムービー
ムービー コントローラー
コントローラー













 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)