+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-21099 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | CYP102A1-A82F-D12-open-state | |||||||||
 マップデータ マップデータ | Deletion variant of CYP102A1 in open state | |||||||||
 試料 試料 |
| |||||||||
| 生物種 |  | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 7.9 Å | |||||||||
 データ登録者 データ登録者 | Su M / Chakraborty S / Osawa Y / Zhang H | |||||||||
| 資金援助 |  米国, 1件 米国, 1件
| |||||||||
 引用 引用 |  ジャーナル: J Biol Chem / 年: 2020 ジャーナル: J Biol Chem / 年: 2020タイトル: Cryo-EM reveals the architecture of the dimeric cytochrome P450 CYP102A1 enzyme and conformational changes required for redox partner recognition. 著者: Min Su / Sumita Chakraborty / Yoichi Osawa / Haoming Zhang /  要旨: Cytochrome P450 family 102 subfamily A member 1 (CYP102A1) is a self-sufficient flavohemeprotein and a highly active bacterial enzyme capable of fatty acid hydroxylation at a >3,000 min turnover rate. ...Cytochrome P450 family 102 subfamily A member 1 (CYP102A1) is a self-sufficient flavohemeprotein and a highly active bacterial enzyme capable of fatty acid hydroxylation at a >3,000 min turnover rate. The CYP102A1 architecture has been postulated to be responsible for its extraordinary catalytic prowess. However, the structure of a functional full-length CYP102A1 enzyme remains to be determined. Herein, we used a cryo-EM single-particle approach, revealing that full-length CYP102A1 forms a homodimer in which both the heme and FAD domains contact each other. The FMN domain of one monomer was located close to the heme domain of the other monomer, exhibiting a configuration. Moreover, full-length CYP102A1 is highly dynamic, existing in multiple conformational states, including open and closed states. In the closed state, the FMN domain closely contacts the FAD domain, whereas in the open state, one of the FMN domains rotates away from its FAD domain and traverses to the heme domain of the other monomer. This structural arrangement and conformational dynamics may facilitate rapid intraflavin and FMN-to-heme electron transfers (ETs). Results with a variant having a 12-amino-acid deletion in the CYP102A1 linker region, connecting the catalytic heme and the diflavin reductase domains, further highlighted the importance of conformational dynamics in the ET process. Cryo-EM revealed that the Δ12 variant homodimer is conformationally more stable and incapable of FMN-to-heme ET. We conclude that closed-to-open alternation is crucial for redox partner recognition and formation of an active ET complex for CYP102A1 catalysis. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_21099.map.gz emd_21099.map.gz | 167.2 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-21099-v30.xml emd-21099-v30.xml emd-21099.xml emd-21099.xml | 10.4 KB 10.4 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_21099.png emd_21099.png | 36 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-21099 http://ftp.pdbj.org/pub/emdb/structures/EMD-21099 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-21099 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-21099 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_21099_validation.pdf.gz emd_21099_validation.pdf.gz | 78.3 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_21099_full_validation.pdf.gz emd_21099_full_validation.pdf.gz | 77.4 KB | 表示 | |
| XML形式データ |  emd_21099_validation.xml.gz emd_21099_validation.xml.gz | 494 B | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-21099 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-21099 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-21099 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-21099 | HTTPS FTP |
-関連構造データ
| 関連構造データ | C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_21099.map.gz / 形式: CCP4 / 大きさ: 178 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_21099.map.gz / 形式: CCP4 / 大きさ: 178 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Deletion variant of CYP102A1 in open state | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.01 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
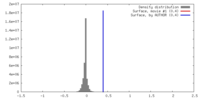
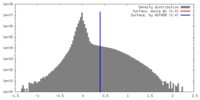
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Deletion variant of cytochrome P450 CYP102A1 enzyme
| 全体 | 名称: Deletion variant of cytochrome P450 CYP102A1 enzyme |
|---|---|
| 要素 |
|
-超分子 #1: Deletion variant of cytochrome P450 CYP102A1 enzyme
| 超分子 | 名称: Deletion variant of cytochrome P450 CYP102A1 enzyme / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all / 詳細: recombinant deletion variant |
|---|---|
| 由来(天然) | 生物種:  |
| 組換発現 | 生物種:  |
| 分子量 | 実験値: 238.8 KDa |
-分子 #1: Cytochrome P450 102A1 (BM3)
| 分子 | 名称: Cytochrome P450 102A1 (BM3) / タイプ: protein_or_peptide / ID: 1 / 光学異性体: LEVO |
|---|---|
| 配列 | 文字列: MHHHHHHIKE MPQPKTFGEL KNLPLLNTDK PVQALMKIAD ELGEIFKFEA PGRVTRYLSS QRLIKEACDE SRFDKNLSQA LKFVRDFFG DGLFTSWTHE KNWKKAHNIL LPSFSQQAMK GYHAMMVDIA VQLVQKWERL NADEHIEVPE DMTRLTLDTI G LCGFNYRF ...文字列: MHHHHHHIKE MPQPKTFGEL KNLPLLNTDK PVQALMKIAD ELGEIFKFEA PGRVTRYLSS QRLIKEACDE SRFDKNLSQA LKFVRDFFG DGLFTSWTHE KNWKKAHNIL LPSFSQQAMK GYHAMMVDIA VQLVQKWERL NADEHIEVPE DMTRLTLDTI G LCGFNYRF NSFYRDQPHP FITSMVRALD EAMNKLQRAN PDDPAYDENK RQFQEDIKVM NDLVDKIIAD RKASGEQSDD LL THMLNGK DPETGEPLDD ENIRYQIITF LIAGHETTSG LLSFALYFLV KNPHVLQKAA EEAARVLVDP VPSYKQVKQL KYV GMVLNE ALRLWPTAPA FSLYAKEDTV LGGEYPLEKG DELMVLIPQL HRDKTIWGDD VEEFRPERFE NPSAIPQHAF KPFG NGQRA CIGQQFALHE ATLVLGMMLK HFDFEDHTNY ELDIKETLTL KPEGFVVKAK SKKIPLAENA HNTPLLVLYG SNMGT AEGT ARDLADIAMS KGFAPQVATL DSHAGNLPRE GAVLIVTASY NGHPPDNAKQ FVDWLDQASA DEVKGVRYSV FGCGDK NWA TTYQKVPAFI DETLAAKGAE NIADRGEADA SDDFEGTYEE WREHMWSDVA AYFNLDIENS EDNKSTLSLQ FVDSAAD MP LAKMHGAFST NVVASKELQQ PGSARSTRHL EIELPKEASY QEGDHLGVIP RNYEGIVNRV TARFGLDASQ QIRLEAEE E KLAHLPLAKT VSVEELLQYV ELQDPVTRTQ LRAMAAKTVC PPHKVELEAL LEKQAYKEQV LAKRLTMLEL LEKYPACEM KFSEFIALLP SIRPRYYSIS SSPRVDEKQA SITVSVVSGE AWSGYGEYKG IASNYLAELQ EGDTITCFIS TPQSEFTLPK DPETPLIMV GPGTGVAPFR GFVQARKQLK EQGQSLGEAH LYFGCRSPHE DYLYQEELEN AQSEGIITLH TAFSRMPNQP K TYVQHVME QDGKKLIELL DQGAHFYICG DGSQMAPAVE ATLMKSYADV HQVSEADARL WLQQLEEKGR YAKDVWAG |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 3 mg/mL |
|---|---|
| 緩衝液 | pH: 7.4 / 詳細: phosphate-buffered saline |
| グリッド | 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 支持フィルム - Film thickness: 0.12 nm / 詳細: unspecified |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 298 K / 装置: FEI VITROBOT MARK I |
| 詳細 | The sample was monodisperse |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 平均電子線量: 48.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 最終 再構成 | 解像度のタイプ: BY AUTHOR / 解像度: 7.9 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 使用した粒子像数: 46150 |
|---|---|
| 初期 角度割当 | タイプ: MAXIMUM LIKELIHOOD |
| 最終 角度割当 | タイプ: MAXIMUM LIKELIHOOD |
 ムービー
ムービー コントローラー
コントローラー












 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)